Clear Sky Science · he
PDLIM5 באנדותל מקדם היווצרות פילופודיות בתאי הקצה ואנגיוגנזה של גידולים באמצעות ויסות ריכוזי ACTN1/ACTN4 באקטין
איך הסרטן מנצלת כלי דם
סרטן לא יכול לצמוח מעבר לקלאסטר קטן ללא שכנוע כלי הדם הסמוכים להביא חמצן ומזון. המחקר הזה חושף כיצד חלבון פחות מוכר ברירית הפנימית של כלי הדם מסייע לגידולים להניב הסתעפויות חדשות ולא תקינות. הבנת התהליך יכולה לפתוח דלת לטיפולים חכמים יותר שלא רק ימנעו אספקת דם לגידול אלא גם ישפרו את יעילות האימונותרפיה.
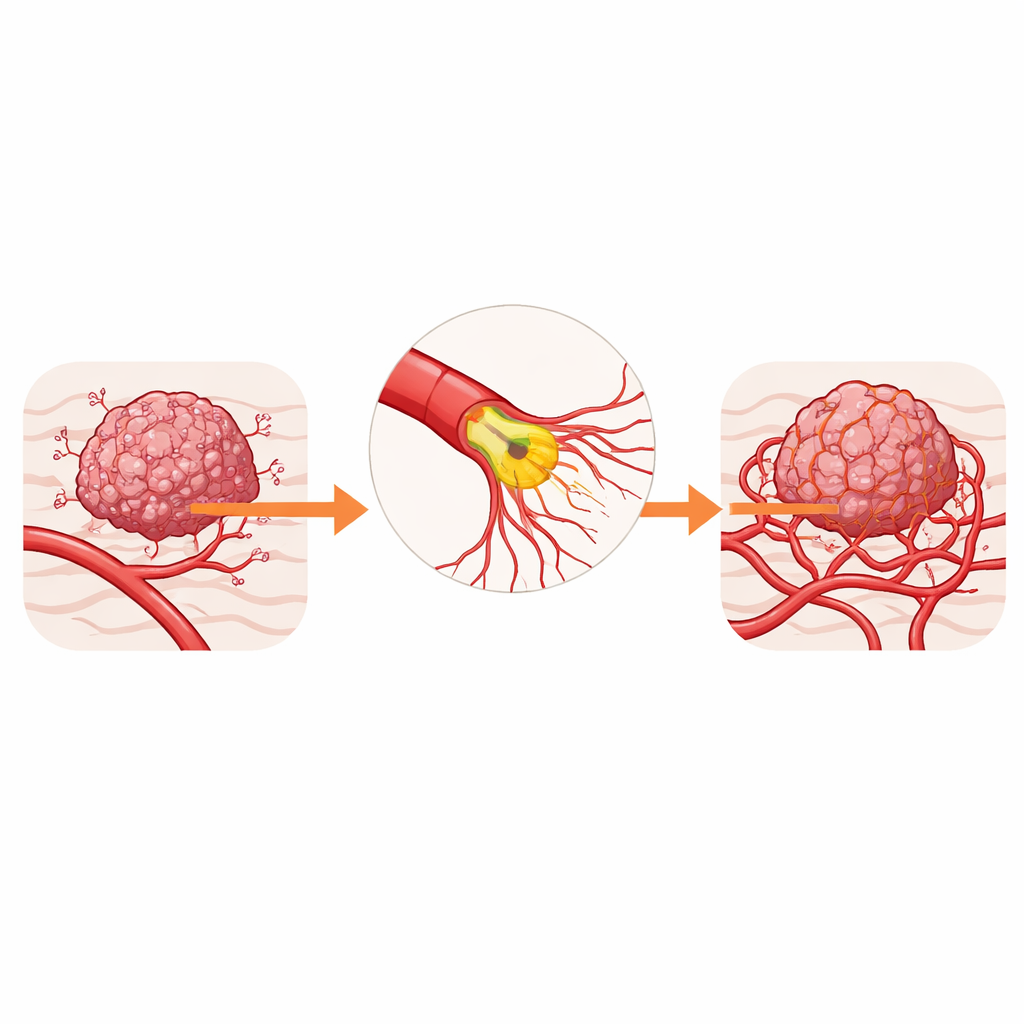
האדריכלים הנסתרים של אספקת הדם לגידול
כלי הדם שמספקים דם לגידול נבנים מתאים מיוחדים הנקראים תאי אנדותל שמצפים את חלל הכלי. בקדמת כל הסתעפות חדשה עומד "תא קצה" ששולח שלוחות ארוכות בצורת אצבעות המכונות פילופודיות. שלוחות אלה חשות רמזים כימיים מהגידול ומכווינות את ההתפתחות אל אזורים שסובלים ממחסור בחמצן. בהרבה סוגי סרטן תהליך הניצת ההסתעפות הזה משתולל, ויוצר כלי דם דולפים ומעוקלים שמחריפים את המצב ההיפוקסי ומקשים על הגעה של תרופות ותאי חיסון אל הגידול.
חלבון שמאיץ את הניצת ההסתעפויות
בנייתם של תאים בודדים מתוך גידולי ריאה אנושיים הראתה שתאי אנדותל הקשורים לגידול מפעילים באופן חזק קבוצה של גנים השולטים בשלד התא, ובעיקר חלבון בשם PDLIM5. PDLIM5 נמצא בריכוז גבוה יותר בכלי דם של גידולים מאשר בכלי דם נורמליים, ולחולים שבהם כלי הדם של הגידול הביעו יותר PDLIM5 נצפתה הישרדות קצרה יותר. במודלים בעכברים של כמה סוגי סרטן, הגדלת ביטוי PDLIM5 באפיתל הכלי גרמה לגידולים לצמוח מהר יותר ולפתח רשת כלי דם צפופה יותר, מה שמרמז שהחלבון פועל כמניע עוצמתי של התפתחות כלי דם בגידול.
כיצד PDLIM5 בונה "מיששים" תאיים
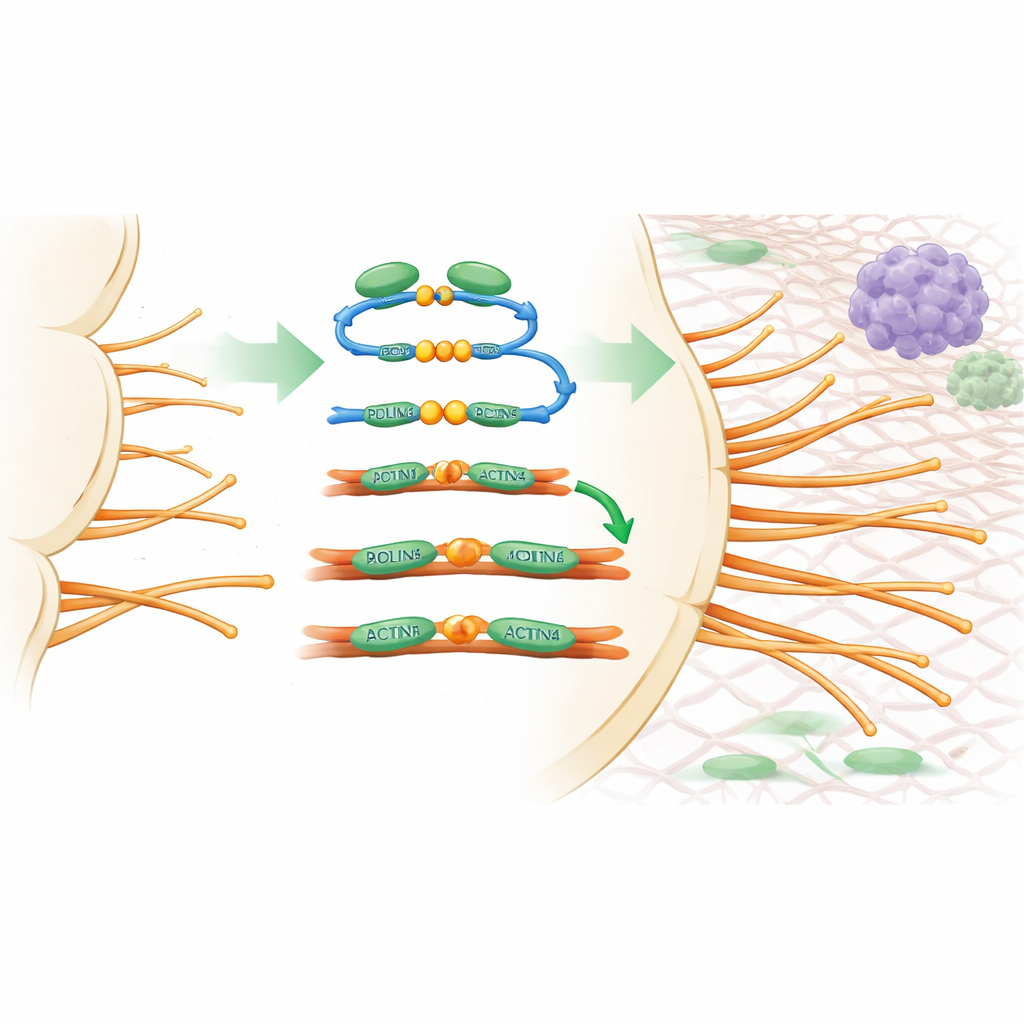
כדי להבין איך PDLIM5 משפיע על התנהגות הכלי, החוקרים השתמשו במערכות ניסיוניות שבהן ניתן לצפות בהשתלשלות הסתעפויות בפרוטרוט, כגון נשירת כלי דם ברשתית העכבר ותרביות תלת־ממדיות של תאי אנדותל. כאשר PDLIM5 הוסר באופן ספציפי מתאי אנדותל, ההסתעפויות התקדמו לאט יותר, היו בהן פחות תאי קצה ונוצרו פילופודיות במידה הרבה יותר נמוכה. במיקרוסקופ נמצא ש‑PDLIM5 מקשר בין שני חלבוני איגוד־אקטין מרכזיים, ACTN1 ו‑ACTN4, לבין סיבי אקטין ארוכים היוצרים את שלד התא. הפעולה הזאת גשרה את הסיבים לאלומת חבליות קשיחות שתומכות בפילופודיות. מוטציות בשני אתרים קריטיים ב‑PDLIM5 (מכונים S593 ו‑F596) שיבשו את הקשר הזה, החלישו את איגוד האקטין ומנעו מ‑PDLIM5 לשחזר את הניצת ההסתעפות לנורמה, והוכיחו שהאינטראקציה המולקולרית הזו חיונית לבניית ה"מיששים" של תא הקצה.
חיבור מחדש של כלי דם בגידול לטובת המערכת החיסונית
להפתעתם, חסימת PDLIM5 ברירית הכלי עשתה יותר מסתם להאטת גדילת הגידול. כלי הדם של הגידול הפכו לצורתיים יותר, פחות דולפים וטופלו טוב יותר על ידי תאי תמיכה המייצבים אותם. כתוצאה מכך שודרגה אספקת החמצן ואזורים של היפוקסיה חמורה הצטמצמו. כלי דם אלה, שה"נורמליזו", אפשרו כניסה מוגברת של תאי T החיסוניים אל הגידול. אובדן PDLIM5 גם שינה את הארגון של מולקולות ההידבקות על תאי האנדותל, מה שהקל על תאי T להיצמד לדופן כלי הדם ולחדור לרקמת הגידול. בעכברים עם גידולים שבדרך כלל עמידים לתרופות חוסמות־צ'קפוינט, מחיקה של PDLIM5 הפכה טיפול בנוגדן אנטי‑PD‑L1 ליעיל הרבה יותר, קמצה את הגידולים והגדילה הן את תאי ה‑helper והן את תאי ה‑killer בתוך הגידול.
מדוע זה חשוב לטיפולי סרטן עתידיים
סיכום הממצאים מראה כי PDLIM5 פועל כמארגן מרכזי של שלד האקטין בתא הקצה, ומאפשר היווצרות פילופודיות עוצמתית וניצת הסתעפויות מהירה כלפי הגידול. הסרה או נטרול של PDLIM5 בתאי אנדותל מאטה את התרחבות אספקת הדם לגידול, מעקמת ומייצבת את כלי הדם שנותרו, מקלה על הרעב לחמצן ומזמינה תאי חיסון אל תוך הגידול. עבור חולים, זה מצביע על כך שתרופות המיועדות לשבש את שותפות PDLIM5‑ACTN1/ACTN4 יכולות גם למנוע אספקת כלי דם חדשה לסרטן וגם להפוך את הווסקולריות הכאוטית של הגידול לרשת שתתמוך טוב יותר בכימותרפיה ובאימונותרפיה.
ציטוט: Xu, Z., Shi, Y., Yang, Y. et al. Endothelial PDLIM5 promotes tip cell filopodia formation and tumor angiogenesis by regulating ACTN1/ACTN4-dependent actin bundling. Nat Commun 17, 2103 (2026). https://doi.org/10.1038/s41467-026-68765-x
מילות מפתח: אנגיוגנזה של גידול, תאי קצה אנדותליאליים, PDLIM5, שלד האקטין, אימונותרפיה של סרטן