Clear Sky Science · he
כימרה אנטיגנית טנדמית מייצבת המעוררת פעילות חזקה להפחתת העברת המלריה
מדוע עצירת העברה על ידי יתושים חשובה
חיסוני מלריה המשמשים כיום יכולים להפחית במידה רבה מחלות קשות ותמותה בקרב ילדים קטנים, אך הם משאירים פירצה מרכזית: אנשים שאינם חולים עדיין יכולים לשאת פרזיטים שמדביקים יתושים וממשיכים את ההעברה. מחקר זה מציג עיצוב חיסון מהדור הבא שאינו מיועד להגן על אדם אחד בלבד, אלא לשבור את שרשרת ההדבקה בין בני אדם ליתושים. על‑ידי הנדסה מדויקת של האופן שבו חלבוני הפרזיט המרכזיים מוצגים למערכת החיסון, החוקרים שואפים לעורר נוגדנים שהופכים את היתושים למאכסנים לא מתאימים למלריה, וכך לסייע לקהילות להתקדם לעבר חיסול המחלה.
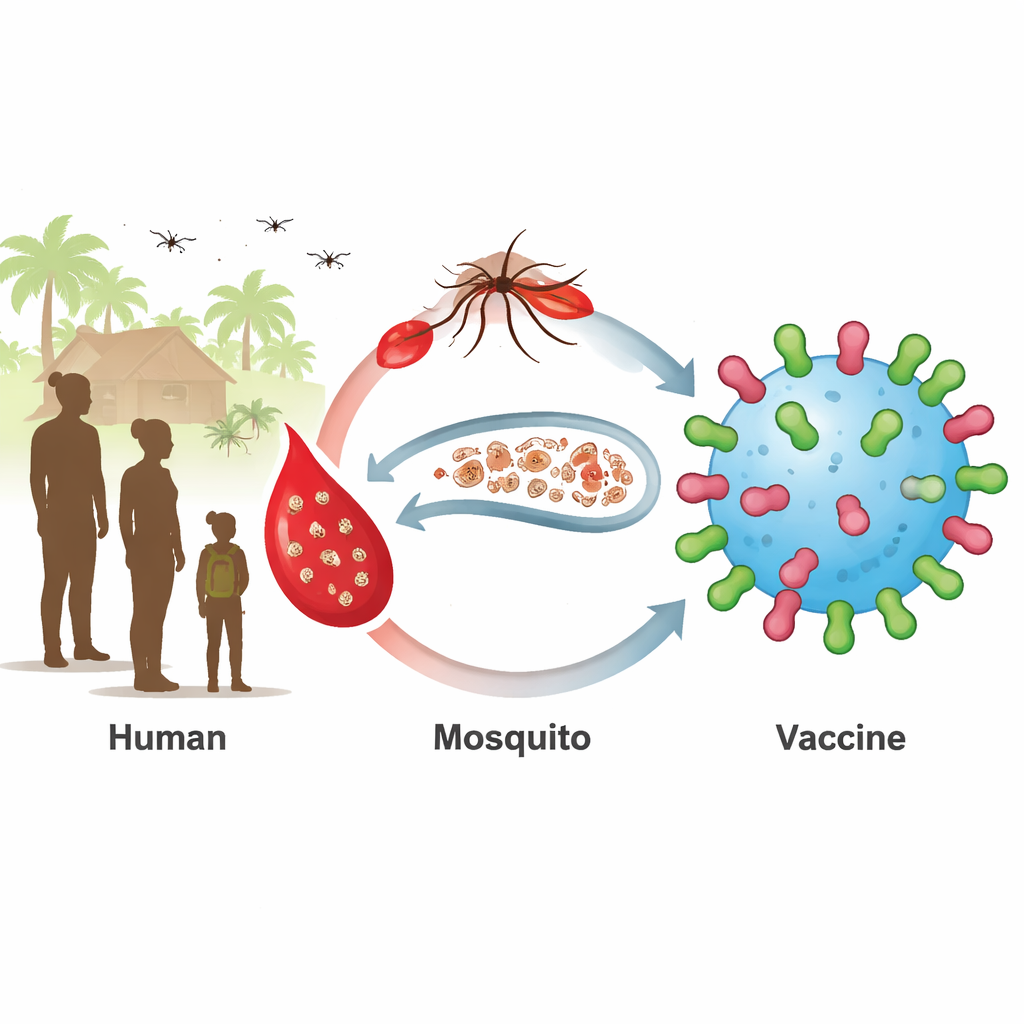
מאגר חבוי ששומר על המלריה בחיים
חיסוני המלריה הקיימים מתמקדים בשלב המוקדם של ההדבקה בכבד ובדמום. הם פועלים בצורה הטובה ביותר בילדים צעירים, אך ילדים בוגרים ומבוגרים לעתים קרובות נושאים שלבים מיניים בוגרים של הפרזיט, הנקראים גמטוציטים, ללא תסמינים. כאשר יתושים עוקצים אנשים אלה, הם קולטים את הפרזיטים ומפיצים אותם הלאה. שני חלבונים על פני הפרזיט, הידועים כ‑Pfs230 ו‑Pfs48/45, נמצאים על שלבים מיניים אלה והם מטרות אטרקטיביות לחיסוני 'חסימת העברה'. חיסונים נגד חלקים של חלבונים אלה נכנסו לניסויים קליניים, אך הם נאבקו בהשגת תגובות נוגדנים חזקות ועמידות בכל הנמענים.
בניית דמה חכמה יותר למערכת החיסון
כדי לשפר על עיצובים קודמים, החוקרים נקטו בגישה של ביולוגיה מבנית, ובחנו ברזולוציה אטומית כיצד נוגדנים אנושיים עוצמתיים נקשרים ל‑Pfs230 ול‑Pfs48/45. הם זיהו אזורים קטנים, או אפיטופים, שהן יעילים במיוחד בחסימת התפתחות הפרזיט בתוך היתושים. לא פחות חשוב, הם מיפו אפיטופים "לא פונקציונליים" שמושכים נוגדנים הקשורים אך שאינם עוצרים את ההעברה — מה שמבזבז למעשה את המשאבים החיסוניים. באמצעות מודלינג ממוחשב וכלי הנדסת חלבונים, הם חיברו את האזור העוצמתי ביותר מ‑Pfs230 (הדומיין הראשון שלו) לאזור המפתח מ‑Pfs48/45 (הדומיין השלישי שלו) בחלבון יחיד ומסודר בקפידה, אשר הם קוראים לו כימרה אנטיגנית טנדמית מייצבת, או STAC.
להסתיר את היעדים המיותרים, לשמור על אלה השימושיים
האתגר היה להציג את שני הדומיינים יחד בצורה המדמה את המיקום שלהם על הפרזיט, תוך הסתרה פיזית של משטחים לא‑פונקציונליים שבדרך כלל קבורים בחלבון השלם. הצוות עיצב מחדש באופן איטרטיבי את הקישור הקצר והממשק בין שני הדומיינים, ובדק כל גרסה לגבי יציבות, קיפולים נכונים והאם היא עדיין נקשרת ללוח של נוגדנים מאופיינים היטב. תוכנות עיצוב מתקדמות הציעו מוטציות שהדקנו את הממשק ושיפרו ביטוי בתאים מושרים. מחקרים מבניים באמצעות קריסטלוגרפיית רנטגן, פיזור קרני רנטגן בזווית קטנה ומיקרוסקופיה אלקטרונית קפואה אישרו שבמבנה ה‑STAC הסופי האפיטופים הרצויים מוצגים בנאמנות גבוהה, בעוד האתרים הלא מועילים הידועים חסומים סטרית.
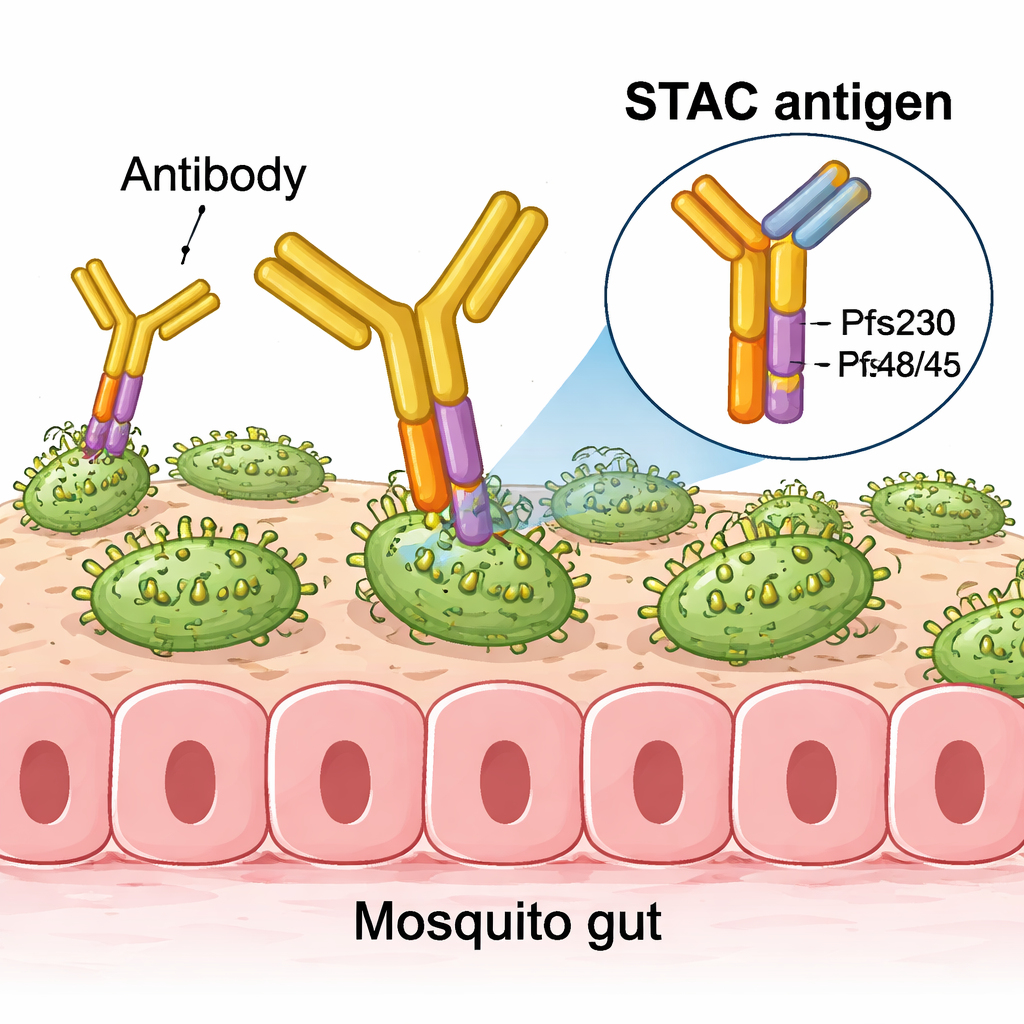
ממולקולות בודדות לננו‑חלקיקים רבי עוצמה
ניסויים בעכברים הראו שכאשר STAC הוצמד לליפוזומים ממוקדים או לננו‑חלקיקים חלבוניים שמתאספים עצמם, הוא עורר תגובות נוגדנים חזקות שהפחיתו באופן משמעותי את התפתחות הפרזיט במבחני האכלה סטנדרטיים של יתושים. במנות שוות או נמוכות יותר, STAC לעתים קרובות השווה או עלה על חיסונים שהשתמשו בפירוקי Pfs230 ו‑Pfs48/45 בנפרד, בין אם ניתנו לבדן, נערבו יחד או הוצגו במשותף על אותו חלקיק. במבחנים רגישים מאוד שבהם מדללים את סרום העכברים פעמים רבות, הנוגדנים שהופקו על ידי ננו‑חלקיקים מעוטרי STAC שמרו על פעילות מפחיתת‑העברה טוב יותר מאלה של ניסוחים אחרים, מה שמעיד על תגובות במיוחד עוצמתיות וממוקדות.
מה זה יכול להצביע לגבי שליטת המלריה
עבור לא‑מומחים, הרעיון המרכזי הוא ש‑STAC הוא דמה מותאמת שמראה למערכת החיסון בדיוק את חלקי הפרזיט החשובים ביותר לחסימת ההפצה, בעודו מסתיר אזורים מסיחי דעת שאינם תורמים. במודלים של בעלי חיים, עיצוב זה מייצר נוגדנים שמקשים על הפרזיטים להשלים את מחזור חייהם ביתושים, אפילו כאשר רמות הנוגדנים נמוכות יחסית. אם ממצאים דומים יאובחנו בבני אדם, STAC עלול להפוך לשותף עוצמתי לחיסוני המלריה הקיימים: להגן על המחוסנים מפני מחלה ובו‑זמנית לצמצם את מאגר המדביקים בקהילה. באופן רחב יותר, העבודה מדגימה כיצד תובנות מבניות מפורטות והנדסת חלבונים יכולות לשמש לעיצוב חיסונים מרובי רכיבים שעמידים, עוצמתיים ובעלי פוטנציאל להיות זולים יותר לייצור.
ציטוט: Ivanochko, D., Miura, K., Hailemariam, S. et al. A stabilized tandem antigen chimera that elicits potent malaria transmission-reducing activity. Nat Commun 17, 2010 (2026). https://doi.org/10.1038/s41467-026-68761-1
מילות מפתח: חיסוני מלריה, חסימת העברה, Pfs230, Pfs48/45, אימונוגן ננו-חלקיק