Clear Sky Science · he
בסיס מבני לגרירת מזלג והרגולציה של RAD51 על ידי קומפלקס ליגאז האוביקוויטין SCF של הליקאזת F-box 1
כיצד תאים מצילים את מכונת העתקת ה‑DNA התקועה
בכל חלוקת תא יש להעתיק במהירות ובדייקנות מיליארדי אותיות DNA. עם זאת, מכונת ההעתקה נתקלת לעתים קרובות בקשיים — נזק ב‑DNA, רצפים שקשה להעתיק או טיפולים תרופתיים עלולים לגרום לעצירת התהליך. כאשר זה קורה, התאים סומכים על צוותי חירום מולקולריים לייצב ולהפעיל מחדש את מזלגות ההעתקה. מאמר זה חושף, ברזולוציה מבנית חסרת תקדים, כיצד אחד מהמנהיגים בצוותים אלה — קומפלקס חלבוני המבוסס על ההליקאזת FBH1 — מעצב מחדש DNA תקוע ושומר על חלבון תיקון מרכזי נוסף, RAD51, תחת פיקוח הדוק. הבנת הכוריאוגרפיה הזו מסייעת להבהיר כיצד תאים נמנעים משבירה מסוכנת של הגנום ולמה שיבושים בגורמים אלה מקושרים לסרטן.
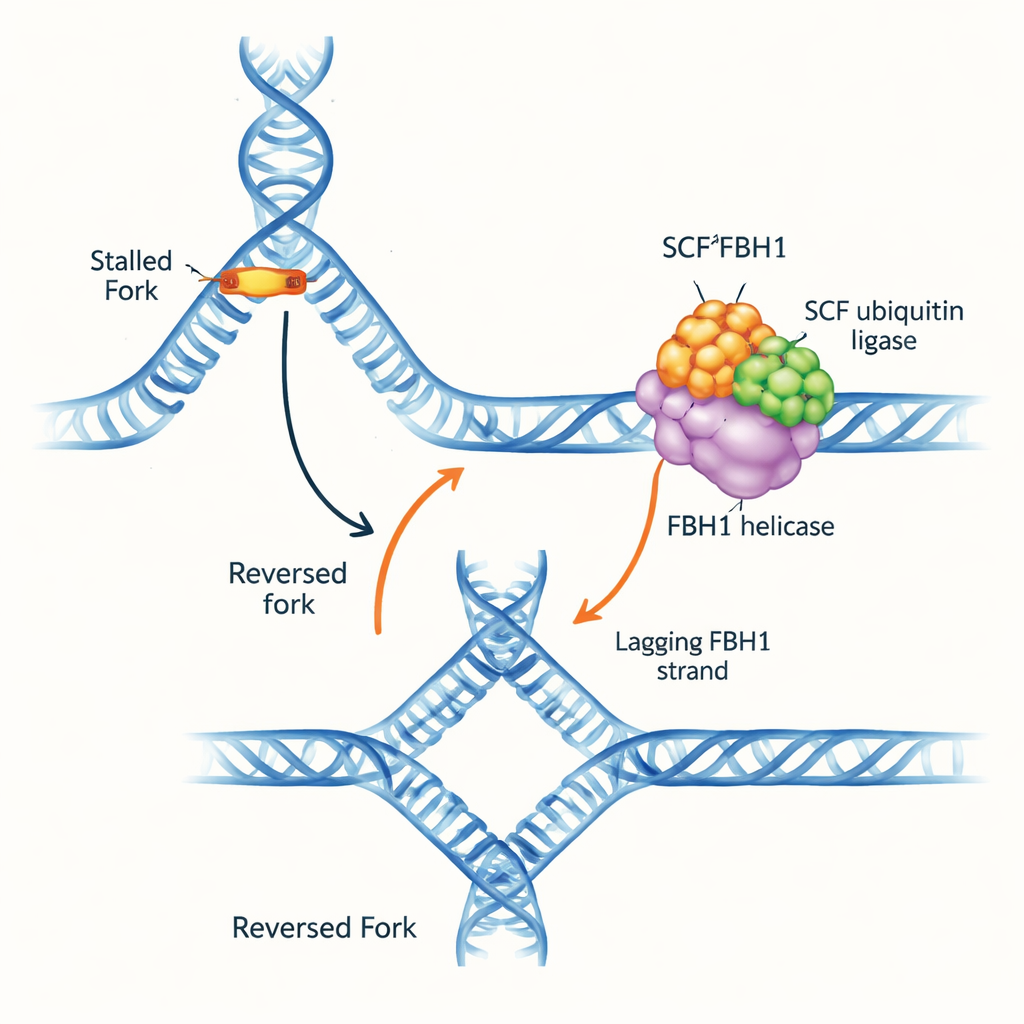
פקק תנועה בכביש ה‑DNA
מזלגות שכפול ה‑DNA הם מבנים בצורת Y שבהם הסליל הכפול מפורק ומועתק. כשהמזלג נתקל במכשולים הוא יכול להפוך כיוון: השרשורים ההוריים נזדקקים מחדש והשרשורים החדשים מתחברים זה לזה, ויוצרים צומת בעל ארבע זרועות. "היפוך המזלג" הזה יכול לקנות זמן לתיקון והפעלת ההעתקה מחדש בבטחה, אך אם הוא מנוהל בצורה לקויה הוא גם יוצר מקטעי DNA עדינים שנוטים לשבור. מספר מנופים מולקולריים ידועים שדוחפים מזלגות לאחור על ידי אחיזה ב‑DNA דו‑גדילי מול המזלג. FBH1 בולט, עם זאת, כי הוא מתנהג בצורה שונה ולעתים קרובות משתנה בגידולים, מה שמרמז שהוא פועל דרך נתיב מובחן ובעל חשיבות רפואית.
מומחה מזלג עם צד מועדף
המחברים טיהרו את קומפלקס ה‑SCFFBH1 האנושי, שמשלב את ההליקאזת FBH1 עם מודול תיוג האוביקוויטין (SCF). הם שאלו תחילה אילו צורות DNA FBH1 מעדיף. באמצעות ניסויי קשירה ופירוק הם הראו ש‑SCFFBH1 מעדיף בחדות מבני מזלג אמיתיים, במיוחד כאשר קיים קטע קצר של DNA חד‑גדילי על תבנית ה"עכב" — הצד שמועתק בחתיכות קטנות. על מבנים אלה FBH1 מפלש DNA במהירות גבוהה פי מאות מאשר בקצה רופף פשוט, מה שמעיד על כך שההשתלבות הנכונה בצומת המזג מאיצה מאוד את פעילות המנוע שלו. ניסויי ציפה מגנטיים חד‑מולקולריים אישרו שהקומפלקס יכול לפתוח ובהמשך לנוע לאורך DNA חד‑גדילי אלפי בסיסים ללא נפילה, ומתפקד כמנוע חזק ותהליךית.
היפוך המזלג על ידי משיכה מאחור
כדי לברר כיצד המנוע הזה למעשה הופך מזלגות, הצוות בחן תבניות מזלג מלאכותיות עם או בלי פערים חד‑גדיליים. בשונה ממעבדי מזלג אחרים, SCFFBH1 לא יכל לפעול על מזלג מזווג לחלוטין; הוא דרש פער על תבנית העכב ונע בכיוון 3′–5′ לאורך אותו גדיל חד־גדילי. תנועה זו של "משיכה מאחור" דוחפת את השרשורים ההוריים להתאחד מחדש בעוד האנזים נשאר מהודק בצומת המזג. מבנה קריו‑EM של SCFFBH1 קשור למזלג תקוע מראה כיצד: משטח חיובי מיוחד, "מוטיב קשירת הצומת", בתת‑תחום אחד של FBH1 יושב ממש בנקודת הפיצול שבה פוגשות שלוש זרועות ה‑DNA. כאשר החוקרים מוטטו שני חומצות אמינו מפתח במוטיב הזה, קצב היפוך המזלג ירד בכ‑25‑פעם בבדיקות מבחנה, בעוד שמכונת הפירוק הבסיסית עדיין עבדה במידה סבירה. בתאים אותה מוטציה מנעה את האטת נורמלית של מזלגות ההעתקה בתגובה לתרופה שיוצרת מתח — סימן מובהק לכישלון בהיפוך המזלג.
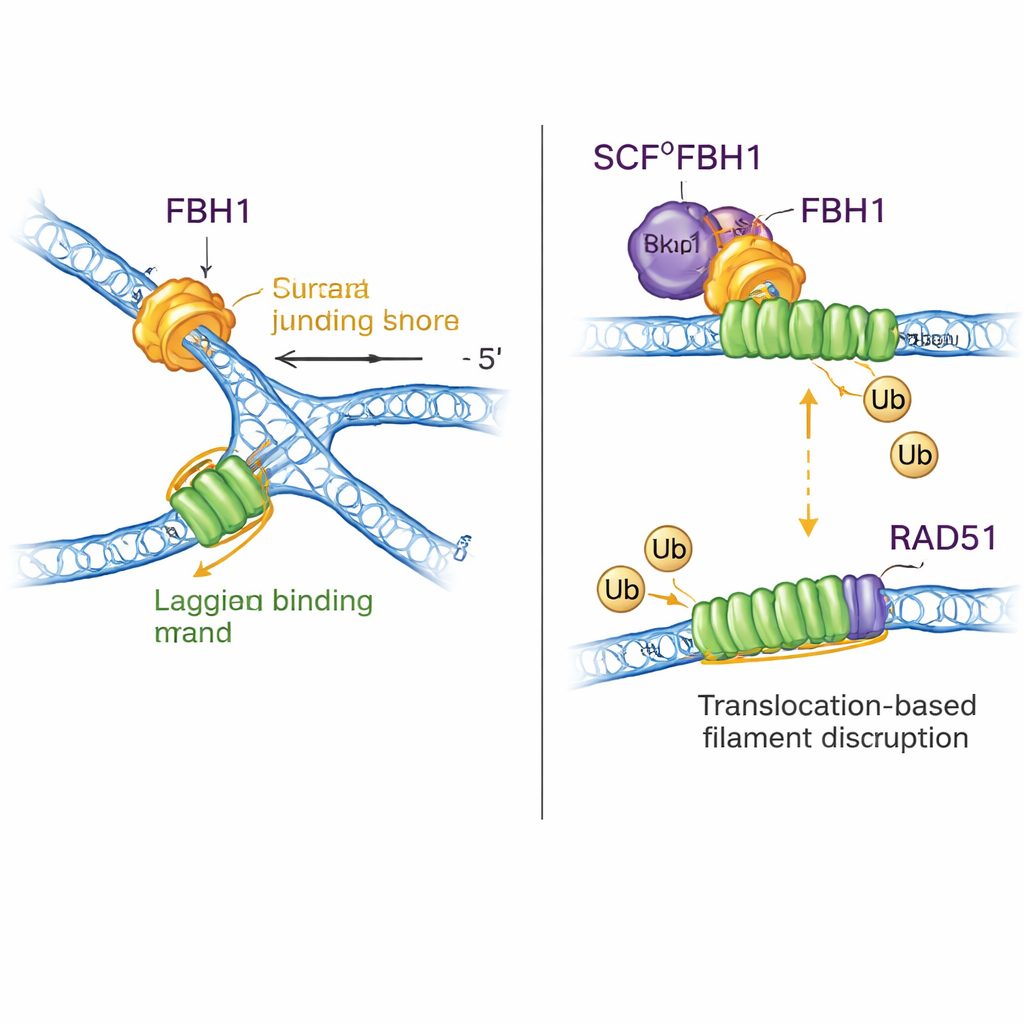
תפקיד כפול: עיצוב DNA והסרת RAD51
FBH1 אינו רק מנוע; דרך קומפלקס ה‑SCF הוא גם מסייע בהיצמדות תגיות אוביקוויטין קטנות לחלבונים. המבנים החדשים מרכיבים כמעט את קומפלקס ה‑SCFFBH1–DNA בשלמותו ומראים שראש העברת האוביקוויטין של הליגאז ממוקם פחות מ‑45 אנגסטרם מה‑DNA של גדיל העכב היוצא מ‑FBH1. על ידי עיגון במבנים ידועים של ליגאזים אחרים, המחברים מציעים שהגיאומטריה הזו ממקמת את RAD51 — אנזים היוצר פילמנטים על DNA לקידום רקומבינציה — ישירות בקו האש על גדיל העכב של מזלג תקוע. עבודה קודמת הראתה ש‑FBH1 יכול להסיר מכנית את RAD51 מ‑DNA וגם לתייג אותו באוביקוויטין כך שלא ישוב ויקשר בקלות. המודל החדש מאחד את הרעיונות הללו: בזמן ש‑FBH1 מושך לאורך גדיל העכב לצורך עיצוב מחדש של המזלג, מודול ה‑SCF הסמוך יכול לתייג תת‑יחידות של RAD51, וסייע לפרק או למנוע יצירת פילמנטים מופרזים של RAD51 שעלולים לחסום עיבוד תקין של המזג.
מה משמעות הדבר עבור יציבות הגנום וסרטן
במכלול, המחקר מראה כי SCFFBH1 הופך מזלגות שכפול תקועים באמצעות מנגנון המובחן ממעבדי מזלג אחרים: הוא אחיז בחוזקה בנקודת הפיצול תוך תנועה לאורך תבנית העכב מאחור, ומקדם השחלה בטוחה של ה‑DNA ההורי ללא יצירת צומת ארבע‑זרוע נאדית ניידת וארוכת זמן. במקביל, ליגאז האוביקוויטין המשולב שלו ממוקם בצורה אסטרטגית כדי להסיר RAD51 מאותו גדיל, ובכך למנוע רקומבינציה מופרזת במהלך מתח בשכפול. מאחר ש‑FBH1 נעלם או מוטנטי בתדירות גבוהה בסרטנים, התובנות המבניות והמכניסטיות הללו מסבירות כיצד גידולים כאלה צוברים נזקים ב‑DNA ולמה הם עשויים להגיב אחרת לתרופות שיוצרות מתח בשכפול או שמטרתן נתיבים קשורים.
ציטוט: Greer, B.H., Mendia-Garcia, J., Mullins, E.A. et al. Structural basis for fork reversal and RAD51 regulation by the SCF ubiquitin ligase complex of F-box helicase 1. Nat Commun 17, 2041 (2026). https://doi.org/10.1038/s41467-026-68752-2
מילות מפתח: מתח בשכפול ה‑DNA, היפוך מזלג, הליקאזת FBH1, וויסות RAD51, יציבות הגנום