Clear Sky Science · he
קינורנין מתווך את הטוקסיות של כימותרפיה במעי דרך מודולציה של המיקרוביום המעי
מדוע זה חשוב לאנשים שעוברים כימותרפיה
כימותרפיה מצילה חיים, אך לרוב מלווה בתופעות לוואי קשות במערכת העיכול—כאב, שלשולים, ירידה במשקל—שעשויות להכריח רופאים לצמצם מינונים או להפסיק טיפול מוקדם. מחקר זה חושף תגובת שרשרת נסתרת בין מולקולה בדם, תאי חיסון ומאקרוביוטה של המעי שמסבירה מדוע תרופה נפוצה לסרטן, אוקסליפלטין, יכולה לפגוע קשות במעיים, ומצביע על דרכים חדשות להגן על מטופלים מבלי לפגוע ביעילות האנטי‑סרטנית.
קישור כימי בין הטיפול לנזק במעי
החוקרים התחילו ממטופלים עם סרטן המעי הגס והרטום המקבלים כימותרפיה מבוססת אוקסליפלטין. הם השוו דגימות דם של אנשים שפיתחו תופעות לוואי מעיים קשות לאלה שסבלו פחות. באמצעות פרופיל כימי ממוקד הם מצאו שמספר תוצרי פירוק של חומצת האמינו טריפטופן היו גבוהים בקבוצת הרעילות הגבוהה, כאשר מולקולה אחת—ל‑קינורנין—בלטה כהגבוהה ביותר. מטופלים עם רמות גבוהות יותר של ל‑קינורנין בדם הראו גם יותר סימני דלקת וספירת תאי דם לבנים נמוכה יותר, מה שמעיד כי המולקולה עשויה להיות קשורה ישירות לנזק הקשור לטיפול.
הוכחת סיבה ותוצאה בעכברים
כדי לצאת מעבר לקורלציה, הצוות פנה לדגמי עכברים. כאשר עכברים בריאים קיבלו מינונים גבוהים של אוקסליפלטין, הם פיתחו תסמינים קלאסיים של פגיעה במעי: ירידה במשקל, קיצור המעי הגס, נפיחות בדופן המעי, פחות תאים מתחלקים ויותר תאים מתים ברירית המעי. בעכברים אלה נרשמה גם עלייה חדה בל‑קינורנין בדם, המשקפת את הנתונים האנושיים. כאשר החוקרים נתנו ל‑קינורנין נוסף לעכברים שקיבלו אוקסליפלטין, הנזק המעי החריף אף החמיר—אך עוצמת ההשפעה האנטי‑גידולית של התרופה נותרה ללא שינוי. לעומת זאת, כאשר הסירו או חסמו את האנזים IDO1, שאחראי על המרת טריפטופן לל‑קינורנין, העכברים הפגינו עמידות רבה יותר לטוקסיות מעי תוך שמירה על תועלת הכימותרפיה נגד הגידול.
תאי חיסון ומיקרובים במרכז הקרב
בהעמקה נוספת, המדענים חקרו אילו תאים אחראים לייצור ל‑קינורנין עודף במהלך הטיפול. הם מצאו שאוקסליפלטין מעורר תאי חיסון מסוימים (תאי CD8) לשחרר את חלבון הסיגנול אינטרפרון‑גאמה, שמפעיל את IDO1 בתאי מיואלואיד סמוכים—סוג של תאי דם לבנים. עכברים שמוּטו כך שרק תאי המיואלואיד שלהם חסרו IDO1 ייצרו הרבה פחות ל‑קינורנין והוגנו מפגיעה מעיים, בעוד שמחיקה של IDO1 רק בתאי רירית המעי השפיעה מעט. במקביל, הרכב מיקרוביום המעי השתנה. בעכברים רגילים, אוקסליפלטין ורמות גבוהות של ל‑קינורנין הקושרו לאובדן חיידק מועיל, Lactobacillus johnsonii. לעומת זאת, בעכברים עם רמות נמוכות של ל‑קינורנין נשמרו רמות גבוהות יותר של L. johnsonii. כאשר חיידקי המעי הושמדו באנטיביוטיקה, האפקט המגן של רמות נמוכות של ל‑קינורנין נעלם, וכאשר העבירו חיידקים מעכברים עם רמות נמוכות של ל‑קינורנין לעכברים רגילים, המוטב קיבל עמידות גבוהה יותר מפני נזק המעי שנגרם על ידי אוקסליפלטין.
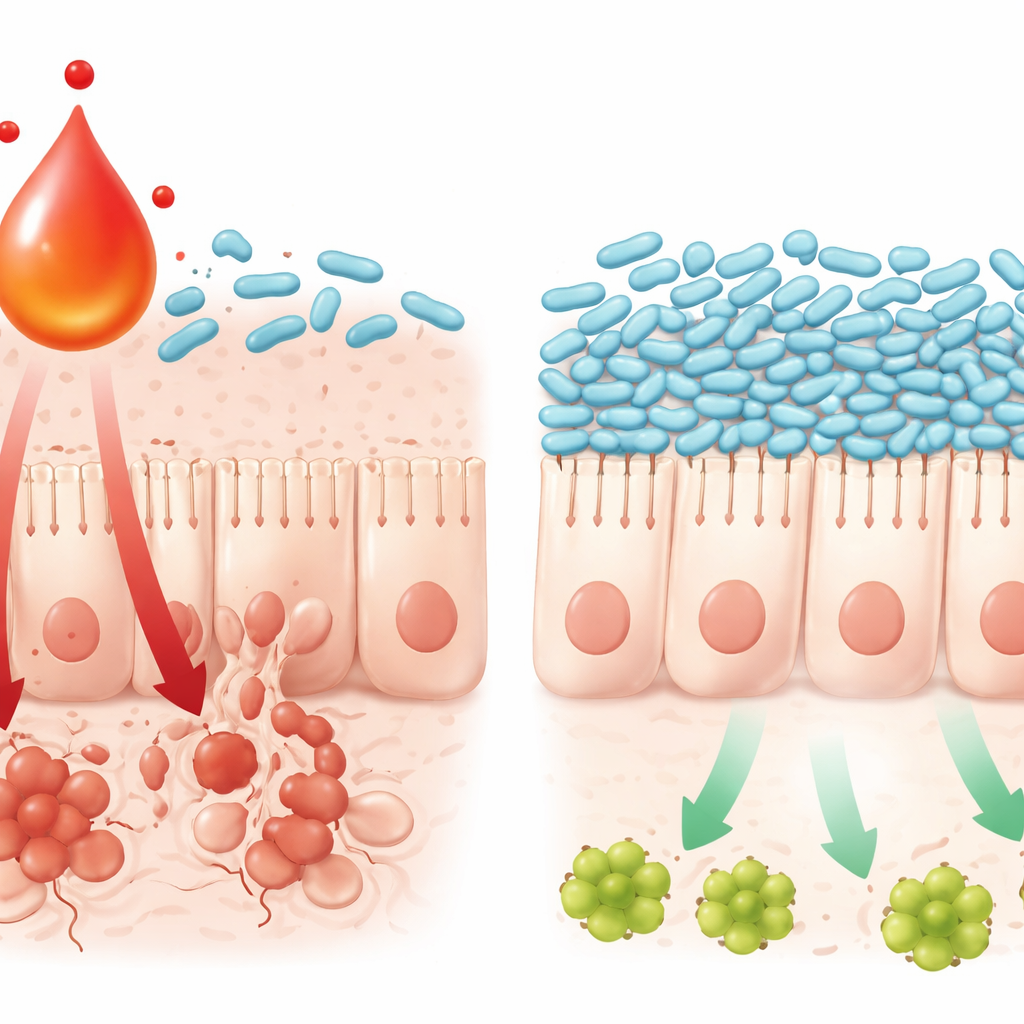
כיצד מטבוליט אחד מגרם למות תאים במעי
המחקר גם עקב אחרי האופן שבו האינטראקציה בין הכימיה לחיידקים פוגעת ברירית המעי. רמות גבוהות של ל‑קינורנין נקשרו לפעילות מוגברת של מסלול דלקתי ידוע ברקמת המעי, מסלול TNFα/JNK, שמניע את התאים לכיוון מוות מתוכנת. בעבודות בתרבית תאים, שילוב של אוקסליפלטין עם ל‑קינורנין גרם לתאי המעי להפעיל את המסלול הזה ולהיכנס למוות בתדירות גבוהה יותר, בעוד שהוספת חיידק L. johnsonii החלישה את האות ושמרה על הישרדות התא. ל‑קינורנין עצמו יכל לעכב גדילה ולפגוע במנגנוני הישרדות של L. johnsonii במבחנה, מה שמסייע להסביר מדוע החיידק נעלם כאשר המטבוליט מצטבר. יחד, הממצאים מתארים מערכת מחזקת עצמית: כימותרפיה מעוררת איתות חיסוני, תאי החיסון מייצרים יותר ל‑קינורנין, זה מפר את החיידקים המועילים כמו L. johnsonii, והקהילה המיקרוביאלית המשתנה בתורה מגבירה אותות דלקתיים שמובילים למות תאי המעי.
דרכים חדשות להגן על מטופלים במהלך הטיפול
באופן מעודד, העבודה מציעה גם אסטרטגיות מעשיות. טיפול בעכברים עם תרופה בשם Epacadostat, שמעכבת את IDO1, הוריד את רמות ל‑קינורנין והפחית באופן מובהק את הנזק המעי הנגרם מאוקסליפלטין מבלי להחליש את שליטת התרופה על הגידול. בגישה משלימה, הצוות מהנדס סטריין חסר בולט של E. coli כדי לייצר ביתר אנזים שמפרק ל‑קינורנין במעי. עכברים שקיבלו את החיידקים המונדסים הוגנו באותה מידה מפני טוקסיות המעי, שוב ללא פגיעה באפקט האנטי‑סרטני של הכימותרפיה. תוספת של L. johnsonii עצמה הקלה גם היא את הסימפטומים ושמרה על מבנה המעי.
מה משמעות הדבר לאנשים עם סרטן
בסך הכול, המחקר מגלה שמטבוליט יחיד המונע על ידי הטיפול—ל‑קינורנין—פועל כמתווך מרכזי בין כימותרפיה, מערכת החיסון, חיידקי המעי ונזק מעי. בכך שמראה שבלימת ייצורו, הגברת פירוקו או שיקום חיידקים מגן יכולות להקל על המכה של הכימותרפיה על המעי, המחקר פותח נתיב לטיפולים משלימים שישמרו על כוחם ונוחותם של החולים בזמן שהם נלחמים בסרטן.
ציטוט: Xie, H., Yang, J., Wu, J. et al. Kynurenine mediates the chemotherapy-induced intestinal toxicity through modulation of gut microbiota. Nat Commun 17, 2087 (2026). https://doi.org/10.1038/s41467-026-68741-5
מילות מפתח: תופעות לוואי של כימותרפיה, מיקרוביום המעי, מטבוליזם של טריפטופן, ל‑קינורנין, סרטן המעי הגס והרקטום