Clear Sky Science · he
הפעלה אלטרנטיבית של EGFR על‑ידי המוטציה R252C שמקורה בחולה מקדמת התקדמות סרטן
כשאנטנות התא משתוללות
מדוע חלק מהסרטן ממשיכים לגדול גם אחרי סבבי כימותרפיה וטיפולי אימונותרפיה מתקדמים? מחקר זה עוקב אחרי חולה שסבל מגידולים בריאה ובמוח ומאתר את מקור המחלה בשינוי זעיר ב"אנטנה" מרכזית על פני התא שנקראת EGFR. באמצעות גילוי הדרך שבה מוטציה אחת זו משחזרת מחדש אותות גדילה, החוקרים לא רק מסבירים את האגרסיביות של הסרטן במקרה הספציפי, אלא גם מראים כיצד תרופה קיימת, אפטיניב, יכולה לבלום זאת.
מוטציה נדירה עם השלכות גדולות
EGFR הוא קולטן החוצה את ממברנת התא ועוזר לתאים להגיב לאותות גדילה. סרטנים רבים של הריאה והמוח נושאים מוטציות ב‑EGFR, אך רוב השינויים המוכרים נמצאים בתוך התא, בחלק המתפקד כמתג אנזימטי. כאן, הצוות גילה שינוי יוצא דופן בחלק החיצוני של EGFR, זה שאחראי לקליטת גורמי גדילה. בחולה שהתגלה אצלו גם סרטן ריאה וגם גליאומה נמצא שעל חומצת אמינו במיקום 252 הוחלף ארגינין בציסטאין — שכונה EGFR R252C. חיפוש במאגרי סרטן גילה מוטציה זו אצל אחוז קטן מחולי גליומה וכמעט אף פעם לא בסרטני ריאה, רמז לכך שהיא נדירה אך קיימת. בעזרת כלים לעריכת גנים, המחברים שיחזרו בדיוק את המוטציה הזאת בכמה שורות תאים אנושיות של סרטן המוח והריאה כדי לבדוק מה היא עושה.
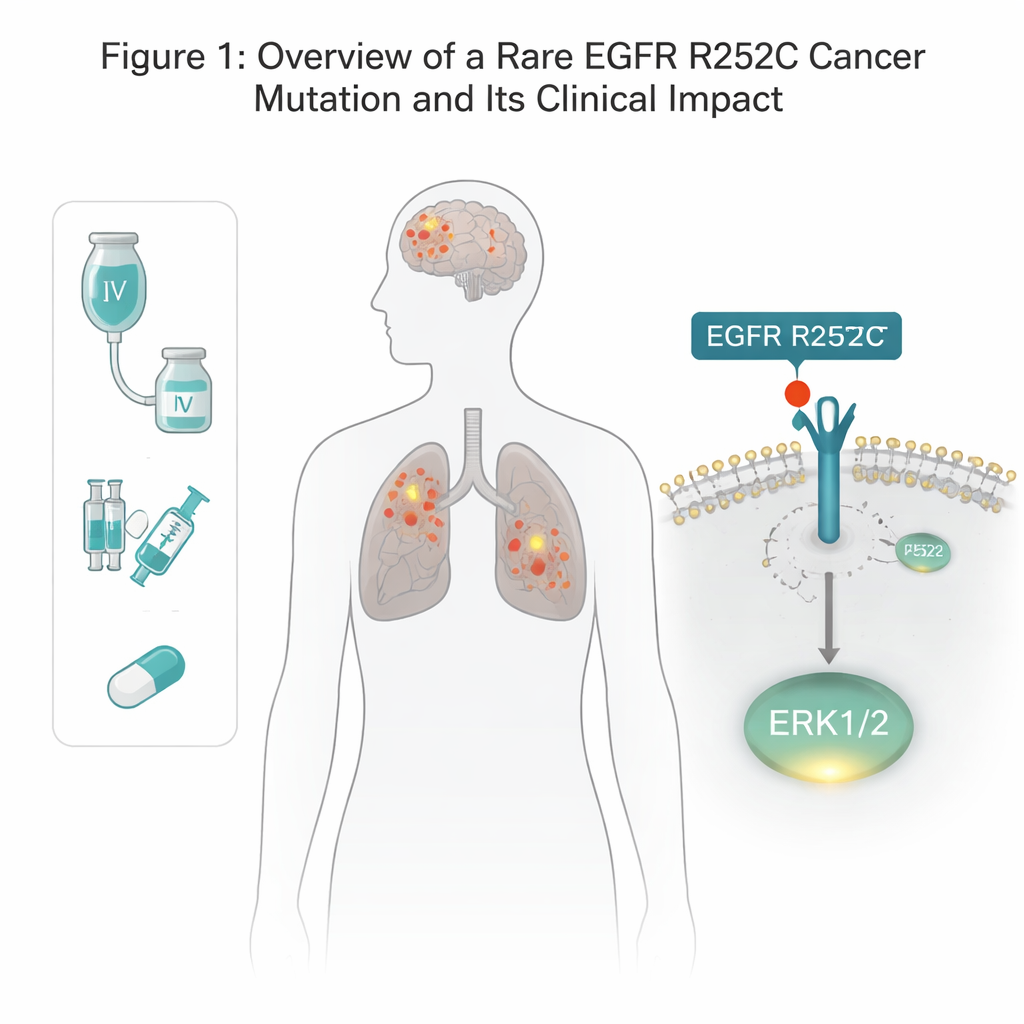
קיצור דרך חדש לאותות גדילה
במצב הרגיל, EGFR חייב להתחבר עם עותק נוסף ואז לתייג את הזנב הפנימי שלו בקבוצות זרחן כדי להפעיל מסלולי גדילה בהמשך. באופן מפתיע, הגרסה R252C לא הראתה את תיוג העצמי הזה. במקום זאת, תאים ששאתם EGFR R252C הפעילו באופן משמעותי מרכיב בקרה אחד ספציפי, ERK1/2, בעוצמה גבוהה בהרבה מהרגיל, בעוד שדרכים קלאסיות אחרות של EGFR — כגון AKT ו‑STAT3 — נותרו ברובן ללא שינוי. חסימת ERK1/2 בעזרת מעכב ייעודי מחקה את יתרון הגדילה המוגבר של תאי R252C, מה שמוכיח ש‑ERK1/2 הוא המנוע העיקרי מאחורי יכולת הנטייה הסרטנית של מוטציה זו.
נְעִילַת הקולטן במצב "דולק" קבוע
כדי להבין כיצד שינוי חיצוני יכול לגרום לעודף הפעלה כזה סלקטיבי, החוקרים שילבו מבחנים ביוכימיים עם סימולציות מחשב. החלפת R252C מכניסה ציסטאין חדשה בחלק החיצוני של EGFR. שני מוטנטים כאלה יכולים ליצור קשר דיסולפידי — מעין מהדק מולקולרי — בין שיירי C252 שלהם, וכך לנעול אותם יחד בזוג יציב. דגמי מבנה הראו שקשר זה מאלץ את החלק החיצוני של הקולטן להתייצב במישור "ב‑V" מסודר, דומה מאוד לצורה הפעילה כאשר קושר ליגנד, גם ללא נוכחות גורם גדילה. יישור זה מתפשט דרך מקטעי חציית הממברנה והאזורים הסמוכים מבפנים, ומסלסל את הדומיינים האנזימטיים הפנימיים לסידור יוצא דופן: אתרי הפעולה פונים פנימה אל התא אך מוחזקים במרחק גדול מדי כדי לתייג זה את זה ביעילות. במקום זאת, קונפורמציה זו יוצרת משטח העגינה חזק ל‑ERK1/2, ומאפשרת ל‑EGFR R252C לפעול ישירות ולזרחן את ERK1/2 תוך עקיפת ממסרת RAS–RAF–MEK הרגילה.
מדגמי עכבר ועד חולה יחיד
המחברים הראו שתאי סרטן מוח וריאה שנושאים EGFR R252C גדלו מהר יותר במעבדות ויצרו גידולים גדולים ואגרסיביים יותר כאשר הושתלו בעכברים, בהשוואה לתאים עם EGFR תקין. לאחר מכן הם בדקו כמה דורות של תרופות חוסמות EGFR. רק אפטיניב, מעכב מדור שני, השבית בעקביות את הפעלת ERK1/2 והקטין בחדות את גדילת תאי הגידול. במודלי עכבר של גידולים מוחיים וריאתיים מונעים על‑ידי R252C, אפטיניב האט את התפשטות הגידול והאריך את ההישרדות. באופן קריטי, כאשר החולה המקורי — שמצבו החמיר למרות כימותרפיה, תרופה המכוונת לכלי דם וטיפולי אימונותרפיה — הועבר לאפטיניב, סריקות של שני הריאה והמוח הראו כיווץ משמעותי בעומס הגידול והחולה נהנה ממספר שנים ללא התקדמות.
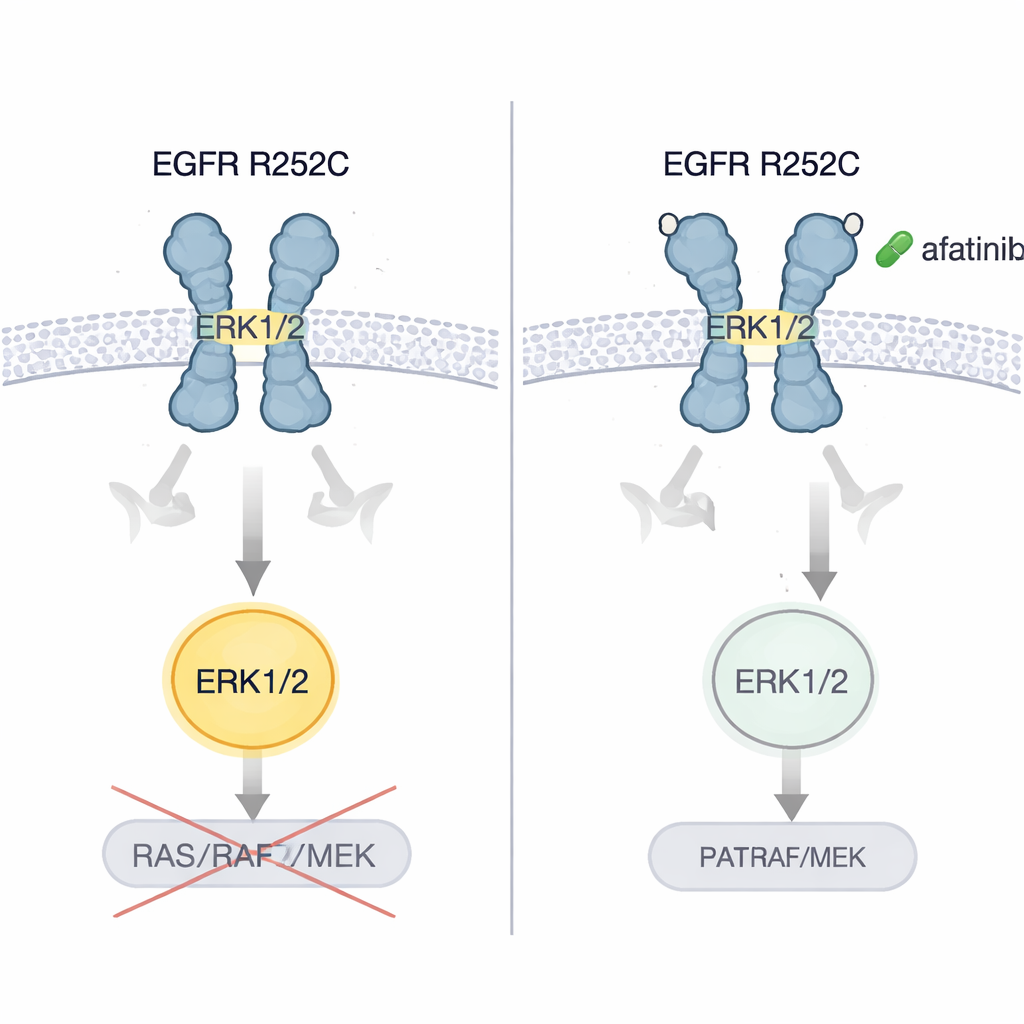
מה זה אומר עבור חולים
עבודה זו חושפת דרך שלא הוכרה קודם שבה מוטציה ממאירה ב‑EGFR יכולה לפעול: על‑ידי מהדק שני קולטנים יחד מחוץ לתא, לסלסל אותם לפוזת "פעילה" שמדליקה ישירות את ERK1/2 במקום ללכת אחרי שרשרת האיתות התיאורתית. לקורא שאינו מומחה, המסקנה המרכזית היא שלא כל המוטציות באותו גֵן מתנהגות זה כך, וכמה שינויים נדירים עשויים להגיב בצורה הטובה ביותר לתרופות קיימות מסוימות. נראה כי EGFR R252C יוצר סרטנים שבאופן מיוחד פגיעים לאפטיניב. למרות שמסקנה זו מסתמכת כיום על מקרה חולה מפורט אחד בתוספת עבודה מקיפה במעבדה, היא מצביעה על בדיקות מותאמות אישית יותר של מוטציות בתחום החיצוני של EGFR ומציעה שתרופות מכוונות נבחרות בקפידה עשויות להציע תקווה חדשה לחולים מסוימים עם גידולים קשים לטיפול במוח ובריאה.
ציטוט: Zhang, Y., Fei, Q., Li, Y. et al. An alternative EGFR activation by patient-derived R252C mutation promotes cancer progression. Nat Commun 17, 1902 (2026). https://doi.org/10.1038/s41467-026-68699-4
מילות מפתח: מוטציה ב‑EGFR, גליומה, סרטן הריאה, איתות ERK, אפטיניב