Clear Sky Science · he
תובנות תפקודיות ומבניות על האינטראקציות בין β-ארסטין 1 ל-Gαs או Gαi1
מדוע זה חשוב לבריאות ולרפואה
רבים מהתרופות של היום, מתרופות אלרגיה דרך תרופות למערכת הלב ועד טיפולים פסיכיאטריים, פועלות על משפחה רחבה של חלבונים על פני ממברנת התא הנקראים קולטני חלבון G‑מוצמדים (GPCRs). קולטנים אלה מעבירים מסרים לתוך התא באמצעות שני שותפים עיקריים: חלבוני G וחלבונים הנקראים בטא‑ארסטינים. המחקר הנוכחי בוחן כיצד אחד מבני משפחת הבטא‑ארסטינים (בטא‑ארסטין 1) מתקשר ישירות עם שני סוגים של חלבוני G בתוך התא. הבנת ה״שיחה״ הנסתרת הזו עשויה לעזור למדענים לעצב תרופות מדויקות יותר עם פחות תופעות לוואי על‑ידי כוונון האופן שבו אותות עוברים בתוך התאים שלנו.
שני שליחים מרכזיים בתוך התאים שלנו
כאשר הורמון או תרופה נקשרים ל‑GPCR על פני התא, זה מפעיל שתי מסלולי תקשורת כלליים. מסלול אחד משתמש בחלבוני G, שמתפתחים ומכבים כמו שעוני מולקולריים על ידי החלפת מולקולה קטנה (GDP) באחרת (GTP). המסלול השני משתמש בבטא‑ארסטינים, שיכולים גם לכבות את איתות חלבוני G וגם להפעיל מסלולי איתות משלהם. במשך זמן רב חקרו המדענים בעיקר כיצד הקולטנים מדברים בנפרד עם חלבוני G או עם בטא‑ארסטינים. עבודות מאוחרות יותר רמזו שחלבוני G ובטא‑ארסטינים עשויים גם לקשור זה את זה או אף ליצור "מגה‑קומפלקסים" גדולים עם הקולטן. עם זאת, הפרטים של איך חלבונים אלה מתחברים ומה משמעות הדבר לאיתות נשארו לא ברורים.
מדידת מי נקשר למי
במחקר זה התרכזו החוקרים בבטא‑ארסטין 1 ובשני תת‑יחידות ה"אלפא" של חלבוני G: Gαs, שלרוב מגביר פעילות תאית, ו‑Gαi1, שבאופן כללי מדכא אותה. באמצעות טכניקת קשירה רגישה הם בדקו עד כמה בטא‑ארסטין 1 מטוהרת וכל חלבון G נצמדים זה לזה בתנאים שונים. הם גילו שהגורם המרכזי אינו האם חלבון ה‑G נמצא במצב "דלק" או "כיבוי", אלא האם בטא‑ארסטין 1 נמצא בצורתו הפעילה והגמישה יותר. גרסה של בטא‑ארסטין 1 שחסרה את הזנב — שמתנהגת כמו אנסמבל רופף ופעיל של צורות — נקשרה בחוזקה ל‑Gαs ול‑Gαi1. לעומת זאת, הצורה המנוחה של בטא‑ארסטין 1, או צורה שננעלה על ידי פפטיד המדמה זנב של קולטן, נקשרה בחולשה או בכלל לא. ממצא זה מצביע שחלבוני G מזהים בעדיפות את בטא‑ארסטין 1 כאשר היא מדגמנת צורות דמויות‑פעילות שעשויות להופיע לאחר הפעלת הקולטן. 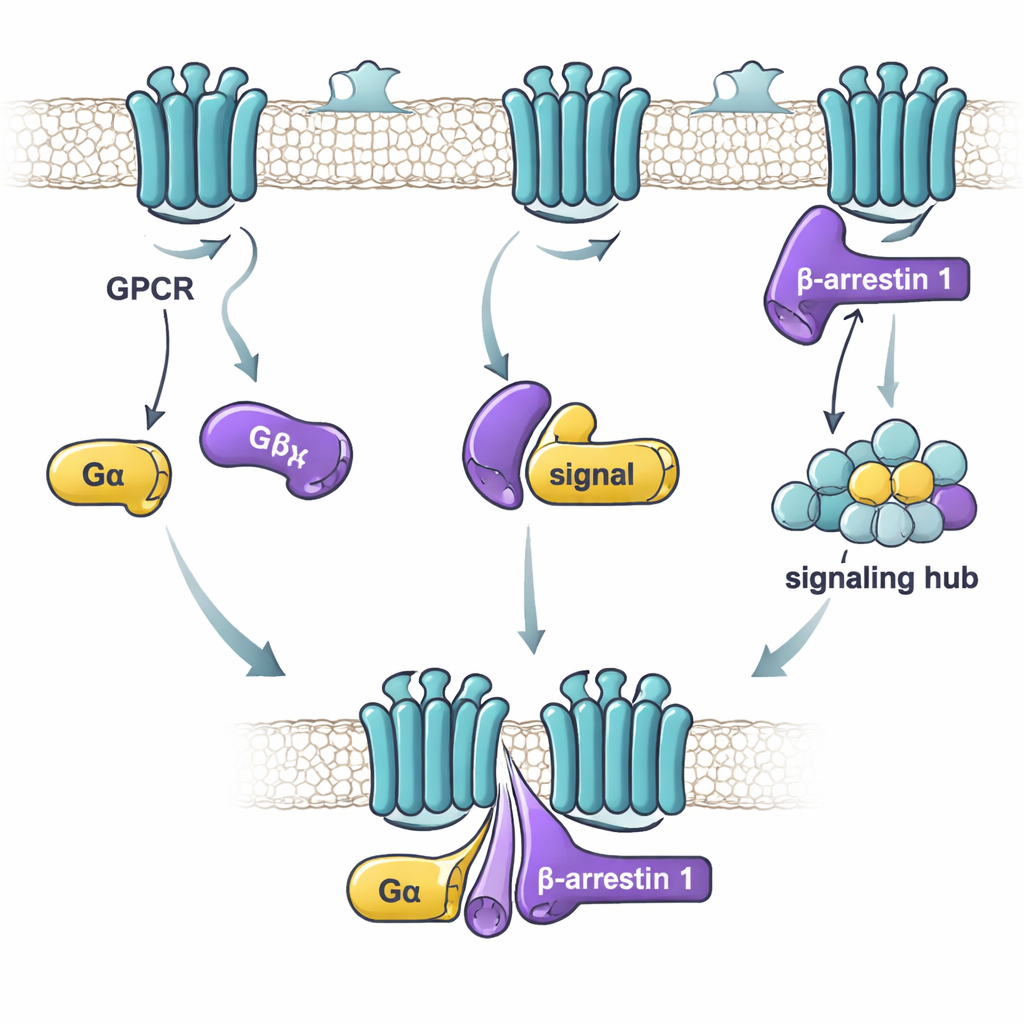
צפייה בשינויים צורתיים עדינים
כדי לראות כיצד קשירה משפיעה על הצורה של החלבונים, הצוות השתמש בשיטה שעוקבת אחרי קצב החלפת אטומי מימן על השלד החלבוני עם מימן כבד מהמסביבה. החלפה איטית יותר בדרך כלל מציינת שאזור הפך מוגן או נוקשה; החלפה מהירה יותר מצביעה על כך שהוא גמיש או חשוף יותר. כשהגרסה הדמוית‑פעילה של בטא‑ארסטין 1 נקשרה ל‑Gαs או ל‑Gαi1, שני חלבוני ה‑G הראו דפוסי שינוי ברורים במספר אזורים, מה שמרמז שהם משנים את צורתם סביב הקומפלקס. לעומת זאת, עצמה של בטא‑ארסטין 1 השתנתה רק במעט, בעיקר בלולאות הגמישות. בעבודה עם דומיינים מבודדים של חלבוני ה‑G, הראו החוקרים גם כי גם החלק הקטליטי הראשי "בדומה‑Ras" וגם האזור האלפא‑הילי (alpha‑helical) שסביבו תורמים לקשירה. אצל Gαs משחק האזור ההילי תפקיד בולט במיוחד; אצל Gαi1 שני האזורים חשובים בערך באותה מידה.
פעולה בלי הפעלת המתג הראשי
השאלה הבאה הייתה האם מגע ישיר זה משנה את אופן הפעלת חלבוני ה‑G. הצוות השתמש במטבע פלואורסצנטי המדמה GTP שמאיר כשהחלבון משנה מצב מ‑GDP ל‑GTP — קריאת סטנדרט להפעיל. באופן מפתיע, הוספת בטא‑ארסטין 1 לא שינתה את מהירות או היקף חילוף הנוקלאוטיד עבור אף אחד מ‑Gαs או Gαi1. במילים אחרות, בטא‑ארסטין 1 אינה פועלת כדוגמת אנזים "מפעיל" קלאסי של חלבוני G. במקום זאת, השפעתה מתבטאת במבנה שלה עצמה. בעזרת בטא‑ארסטין 1 מהונדסת שניתן היה לעקוב אחרי תנועת זנבה באמצעות פלואורסצנציה, הם מצאו ש‑Gαs בפורמה פעילה, אבל לא Gαi1, מאיץ את שחרור הזנב הקוטרי של בטא‑ארסטין כאשר פפטיד מקורו בקולטן נוכח. בתאים חיים, הדמיות נוספות וחיישני העברת אנרגיה אישרו ש‑Gαs ובטא‑ארסטין 1 מתקרבים זה לזה בעקבות גירוי הורמונלי וש‑Gαs מסייע לדחוף את בטא‑ארסטין 1 לכיוון קונפורמציה פעילה יותר. 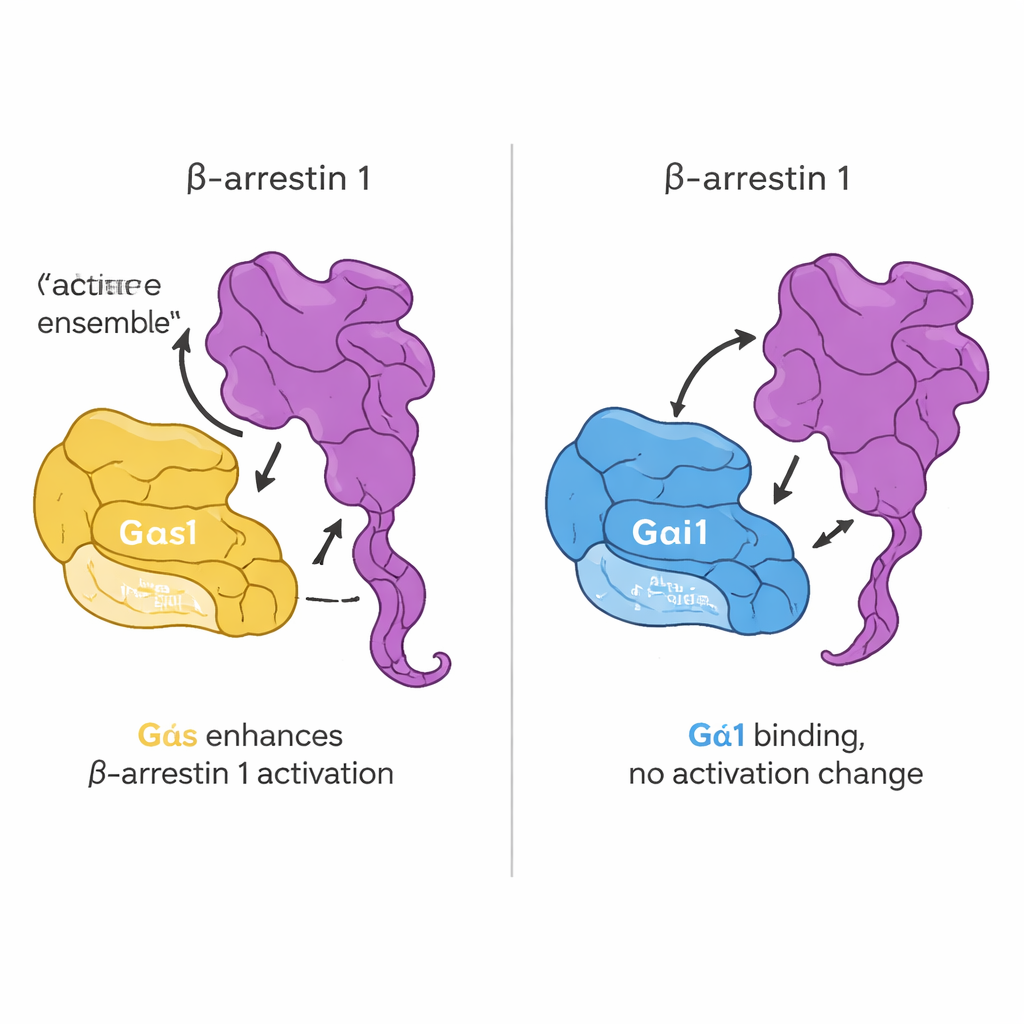
שכבה חדשה של בקרה באיתות תאיים
במבט כולל על תוצאות אלו, המחקר מציע ש‑Gαs ו‑Gαi1 קשורים ישירות לבטא‑ארסטין 1, אך בדרכים מעט שונות ובתוצאות מובחנות. אף אחד מחלבוני ה‑G אינו משנה את התנהגות ה"הפעלה/כיבוי" העיקרית שלו בעקבות קשר זה. במקום זאת, במיוחד עבור Gαs, האינטראקציה פועלת יותר כמו כפתור לכוונון עדין של בטא‑ארסטין 1, נדחפת או מייצבת אותה לצורה פעילה יותר שבה הזנב משתחרר. זה מוסיף שכבה שלא הוערכה דיו לאיתות של GPCR: לא רק שקולטנים יכולים לתאם בין חלבוני G ובטא‑ארסטינים, אלא שחלבוני G ובטא‑ארסטינים יכולים גם למודל זה את זה ישירות. בטווח הארוך, מיפוי האינטראקציות העדינות האלו עשוי לסייע למעצבי תרופות לכוון את האיתות לאורך מסלולים מועילים — בהגברה של מסלולים רצויים ובהמנעות מאלו שמגבירים תופעות לוואי.
ציטוט: Duan, L., Kim, H., Suh, Y. et al. Functional and structural insights into interactions between β-Arrestin 1 and Gαs or Gαi1. Nat Commun 17, 1879 (2026). https://doi.org/10.1038/s41467-026-68690-z
מילות מפתח: קולטני חלבון G־מוצמדים לממברנה, בטא-ארסטין, אותות חלבוני G, מנגנוני איתות תאיים, ביולוגיה מבנית