Clear Sky Science · he
שיבוש שונה של שומני הממברנה על־ידי אנטיביוטיקות ליפופפטידיות, קוליסטין וטורנריסיקלמיצינים
מדוע הדבר משמעותי עבור אנטיביוטיקות עתידיות
צפויים שמפגעים עמידי-תרופות יהרגו עשרות מיליוני אנשים מדי שנה עד אמצע המאה, ואחדים מהפתוגנים הקטלניים ביותר הם חיידקים שליליים-גרם שכבר מתעלמים מרבות מהאנטיביוטיקות. קוליסטין הוא אחד הכימיקלים הבודדים שעדיין מסוגלים לטפל בזיהומים אלה, אבל הוא פוגע בחולות והחיידקים לומדים לעקוף אותו. המחקר הזה מפרק כיצד קוליסטין פועל בהשוואה למשפחה חדשה של אנטיביוטיקות טבעיות הקרויות טורנריסיקלמיצינים, ומגלה ששינויים כימיים זעירים יכולים להוליד דרכי הרג שונות למדי — ואפשרות לפיתוח תרופות בטוחות יותר.
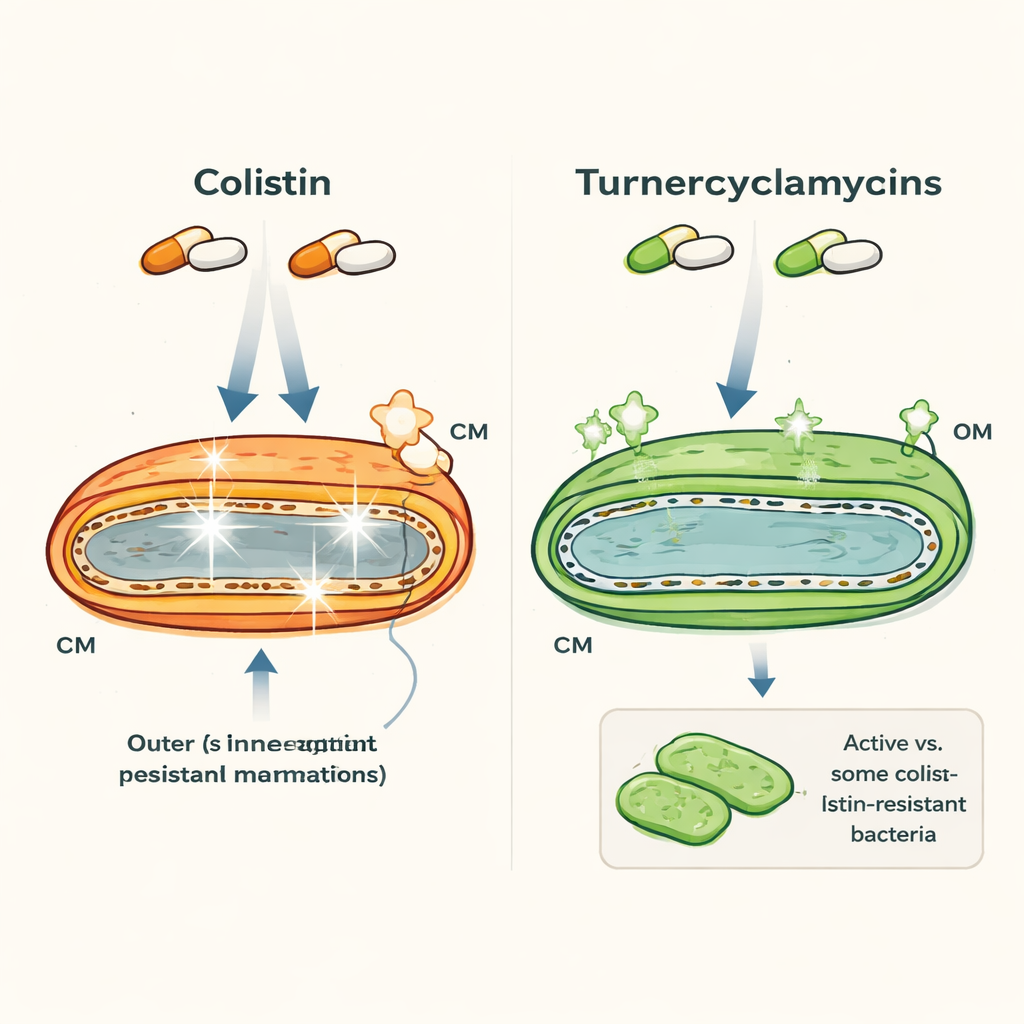
שני תרופות דומות במראה, אך עם התנהגות שונה לחלוטין
קוליסטין וטורנריסיקלמיצינים הן שתיהן ליפופפטידים — מולקולות שמשלבות זנב שומני עם טבעת פפטיד — ושתי המשפחות מיועדות לחיידקים שליליים-גרם כמו Escherichia coli ו־Acinetobacter. במבט ראשון הן נראות דומות, אך תכונותיהן שונות במהותן. קוליסטין הוא טיפל אחרון שמתחיל לעבוד במהירות אך עלול לפגוע בכליות ובעצבים של בני אדם, והחיידקים נושאים גנים לעמידות כמו mcr-1. טורנריסיקלמיצינים, שהתגלו בחיידקים המשויכים לתולעי אונייה, יכולים להרוג רבים מאותם פתוגנים, כולל כמה זנים עמידים לקוליסטין, אך מראים רעילות נמוכה בהרבה בניסויים במעבדה. באופן מפתיע, שתי גרסאות שמופרדות רק על־ידי הארכה קטנה של הזנב השומני כבר מציגות דפוסי עמידות שונים, מה שמרמז שתכונות מבניות עדינות מאוד חשובות.
איך קוליסטין פוצע וחורר וטורנריסיקלמיצינים נעשים לאט
המחברים השתמשו בכימיות זוהרות, ניסויי חיסול בזמן ומיקרוסקופ אלקטרונים כדי לצפות כיצד התרופות משפיעות על ממברנות החיידק לאורך הזמן. קוליסטין גורם במהירות לדליפת שתי הממברנות — החיצונית והפנימית הציטופלזמטית — מה שמוביל למות תאים מהיר בתוך כמה שעות. טורנריסיקלמיצינים, לעומת זאת, הורגים לאט יותר — לוקח 6 עד 10 שעות כדי לנקות תרביות לחלוטין — ומטרידים בעיקר את הממברנה החיצונית. צבעים זוהרים שמתניעים כאשר הממברנה הפנימית נפגעת הראו אותות חזקים עבור קוליסטין אך רק אותות מתונים ומאוחרים יותר עבור טורנריסיקלמיצינים, ותמונות ברזולוציה גבוהה אישרו נזק זעום נראה לעין לממברנה הפנימית גם כשהתאים מתים. זה מצביע על כך שטורנריסיקלמיצינים אינם הורגים בדרך הקלאסית של ‘‘יצירת נקבים’’ שמאפיינת רבות מהאנטיביוטיקות הפוגעות בממברנה.
אבני בניין שומניות כגלגלי בקרה נסתריים
שתי משפחות התרופות תלויות בסופו של דבר ברכיב חיידקי שנקרא ליפופוליסכריד (LPS), שנבנה בממברנה הפנימית ובדרך כלל מייצא לפניו אל פני השטח החיצוני. כאשר החוקרים השביתו שלבים מוקדמים בביוסינתזה של LPS, גם קוליסטין וגם טורנריסיקלמיצינים איבדו פעילות; אך כאשר חסמו את מכונת ההובלה שמזיזה את ה־LPS החוצה, התרופות עדיין עבדו. משמעות הדבר היא שהנוכחות של אבני הבניין של ה־LPS חיונית, אך היעד הסופי שלהן אינו. הבדל מרכזי הופיע כאשר מדדו קשירה ישירה: קוליסטין נדבק ל־LPS טהור בעוצמת מיקרומולארית, בעוד שטורנריסיקלמיצינים לא הראו קשירה מדידה. במקום זאת, טורנריסיקלמיצינים הושפעו מאוד משומנים אחרים בממברנה. פוספוליפידים מסוימים, במיוחד פוספטידילגליצרול, יכלו להחליש או לויסת את פעילותם, והתרופות נתפסו בקלות על ידי וניקולות ממברנה חיצוניות — בלונים שומניים זעירים שמשתחררים מהחיידקים.
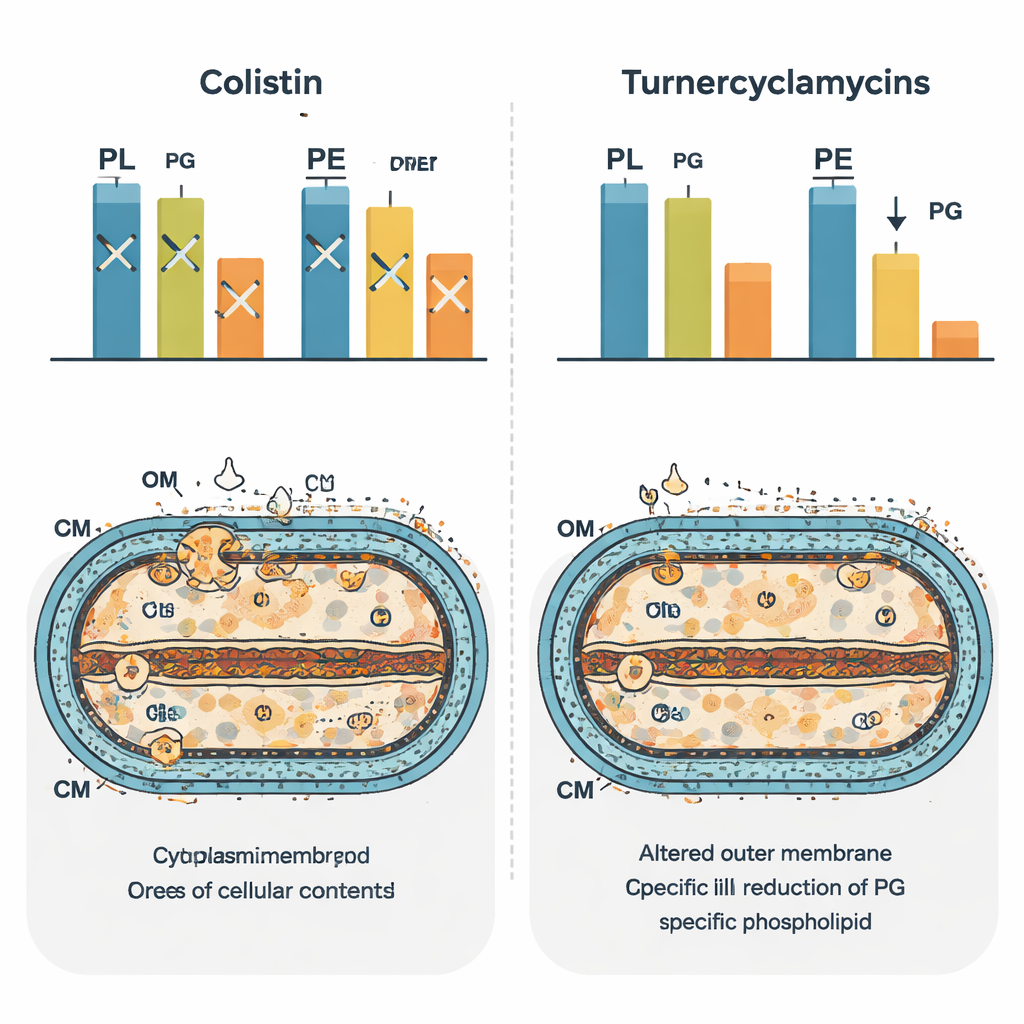
חוטים מחדש של נוף השומנים החיידקי
כדי לראות את ההשפעה הרחבה על התא, הקבוצה השתמשה ב"פוספוליפידומיקה" המבוססת על ספקטרומטריית מסה כדי לערוך קטלוג של מאות סוגי שומנים לאחר הטיפול. קוליסטין יצר דפוס מובהק של שינויים, המשקף את השיבוש הרחב של הומיאוסטזת הממברנה. טורנריסיקלמיצינים יצרו חתימה שונה שהזכירה במידה רבה חיידקים החסרים חלבון מעביר שומנים בשם MlaA. בתאים אלה, לגזרים דיאציליים מסוימים נצפתה ירידה ולצורות מונואציליות נצפתה עלייה, מה שמרמז שהמחזור הנורמלי ושכתוב הפוספוליפידים בין הממברנות הופר. באופן בולט, רמות הפוספטידילגליצרול ירדו בתאים שטופלו בטורנריסיקלמיצינים, מה שמחזק את הרעיון ששומן זה קשור ישירות לעוצמתם. החוקרים מציעים שטורנריסיקלמיצינים עלולים לפעול כמחקים מולקולריים החוסמים את המסלולים המקשרים בין סינתזת חומצות שומן, LPS ופוספטידילגליצרול או את הובלתם.
מה משמעות הדבר לעיצוב תרופות טובות יותר
פשטנית, המחקר מראה שקוליסטין הורג על־ידי קריעה מהירה של שתי שכבות ההגנה של חיידק שלילי-גרם, בתיווך קשירה חזקה ל־LPS, בעוד שטורנריסיקלמיצינים פועלים יותר כסאפטאג׳ים של שרשרת אספקת השומנים של התא. הם מחליקים אל הממברנה החיצונית, מפריעים בהדרגה לאופן שבו שומנים ספציפיים מיוצרים וממוחזרים, ובסופו של דבר גורמים לכשל במעטפת התא — מבלי להרביץ בחוזקה לממברנה הפנימית. מאחר שמנגנון זה עדין וממוקד יותר מקושר לרעילות נמוכה יותר ולפרופיל עמידות שונה, הבנתו מציעה מפת דרכים לפיתוח דור הבא של אנטיביוטיקות ליפופפטידיות. על־ידי כיוונון מדויק של תכונות כגון אורך ורוויה של הזנב השומני, כימאים עשויים לבנות תרופות שתחסכנה רקמות אנושיות, תשמרנה פעילות כנגד זנים עמידים לקוליסטין, ותשאירנה אותנו צעד אחד לפני המירוץ החימוש המתמשך מול חיידקים עמידי־אנטיביוטיקה.
ציטוט: Lim, A.L., Miller, B.W., Fisher, M.A. et al. Differential membrane lipid disruption by lipopeptide antibiotics, colistin and turnercyclamycins. Nat Commun 17, 1880 (2026). https://doi.org/10.1038/s41467-026-68681-0
מילות מפתח: עמידות אנטיביוטית, חיידקים שליליים-גרם, קוליסטין, אנטיביוטיקות ליפופפטידיות, שומני ממברנה