Clear Sky Science · he
בסיס מבני לקונפורמציות הדינמיות של AP-4 ולשיתוף פעולו עם ARF1
כיצד תאים ממיינים ומשנעים את המטען שלהם
כל תא הוא מחסן שוקק חיים, שממיין ומשנע ללא הרף אלפי "חבילות" חלבוניות ליעדים הנכונים. כשהמערכת הזו מתקלקלת בתאי עצב, התוצאה יכולה להיות הפרעות מוח ותנועה משמעותיות. המחקר הזה חושף כיצד מכונה מרכזית אחת למשלוח, הנקראת AP-4, משנה צורה ומשתפת פעולה עם חלבון מווסת בשם ARF1 כדי לעמוס מטען לתוך בועיות תחבורה זעירות ולמה הגמישות שלה חשובה כל כך לתפקוד תקין של נוירונים.
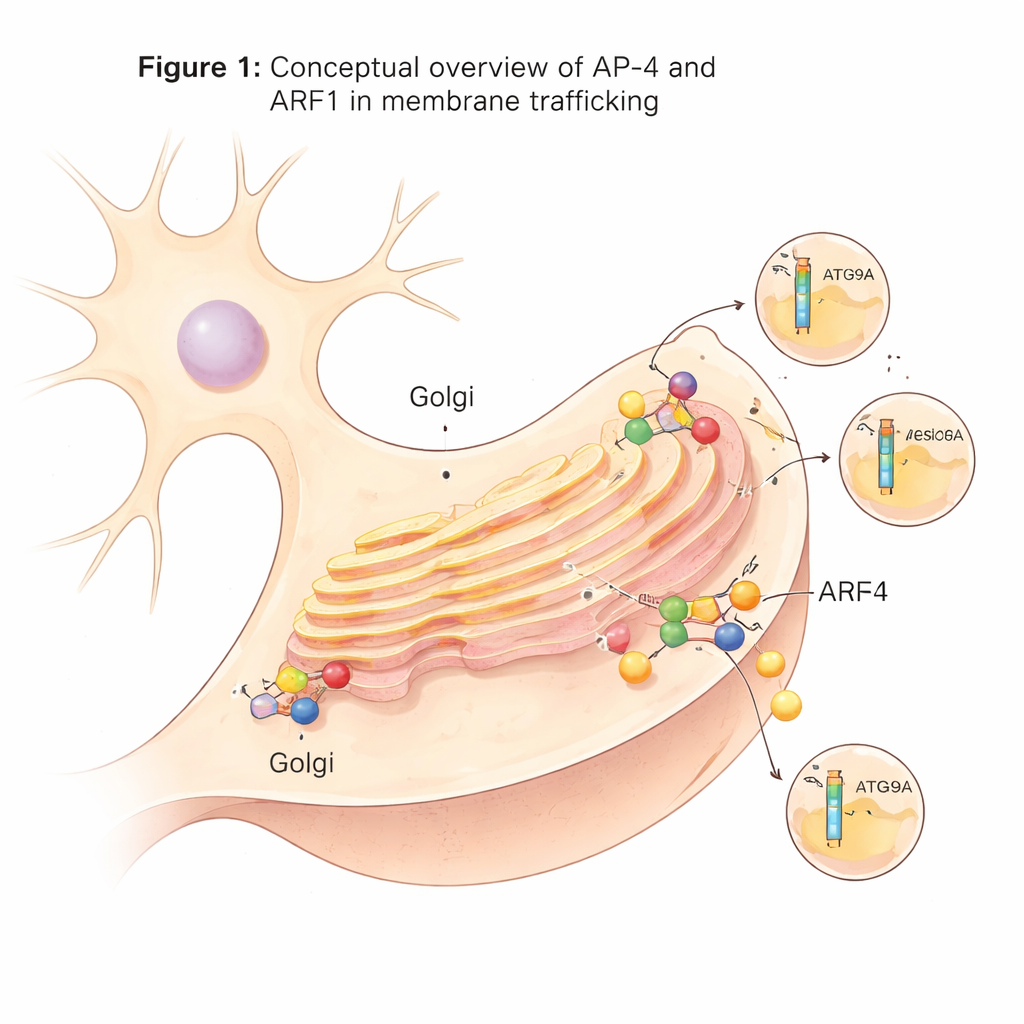
מכונת משלוח מיוחדת בתאי עצב
בתוך התאים, בועיות תחבורה רבות מתבלטות מתחנת המיון המרכזית הידועה כרשת הטרנס-גולג'י. הבועיות האלה תלויות בקומפלקסים של חלבוני מתווך, או קומפלקסי AP, שפועלים כמו רציפי העמסה: הם מזהים חלבוני מטען ועוזרים לעטוף אותם בבועיות מצופות. AP-4 הוא אחד המתווכים האלה וייחודו בכך שהוא, בניגוד לאחרים רבים, אינו משתמש בחלבון השלד הנפוץ קלתרין. אף על פי ש-AP-4 מיוצר ברקמות רבות, הוא ממלא תפקיד חשוב במיוחד בתאי עצב. כאשר AP-4 חסר או פגום בבני אדם, מטענים קריטיים כגון חלבון הקשור לאוטופאגיה ATG9A וכמה קולטי גלוטמט אינם נעים כראוי, מה שמוביל למצב חמור בהתפתחות העצבים הידוע כסינדרום חוסר AP-4.
קומפלקס שמשנה צורה במנוחה
המחברים השתמשו במיקרוסקופיה אלקטרונית קריוגנית, שיטה חזקה הדמיה שיכולה להראות התכנסות תלת-ממדית של הרכבים חלבוניים גדולים, כדי לקבוע את המבנה התלת-ממדי של קומפלקס "הליבה" של AP-4 בתמיסה. AP-4 בנוי מארבע תת-יחידות היוצרות יחד מבנה בצורת קערה. הם גילו ש-AP-4 אינו יושב בצורה קשיחה יחידה. במקום זאת, הוא מתרוצץ באופן טבעי בין צורה "סגורה", שבה תת-יחידה אחת (הדומיין הקצה-אחורי של תת-היחידה הבינונית) מקופלת במרכז הקערה, לבין צורה "פתוחה", שבה החלק הזה מתנדנד החוצה והופך לגמיש מאוד. ניסויי זוהר חד-מולקולרי נוספים הראו שתת-יחידה זו אכן בוחנת לפחות שלוש עמדות — סגורה, חלקית פתוחה ופתוחה לחלוטין — ובכך חושפת ש-AP-4 הוא דינמי מטבעו גם לפני קשירה לממברנות.
תפקידו של ARF1: מגייס, לא מתג ראשי
קומפלקסים מתווכים רבים קרובים עוברים ממצב לא פעיל למצב פעיל על ידי קשירה לחלבוני בקרה קטנים הנקראים ARF. כדי להבין כיצד זה פועל עבור AP-4, החוקרים פתרו מבנים של AP-4 קשור ל-ARF1, חלבון קטן הקושר GTP ועוגן לממברנות. הם מצאו ש-ARF1 מצמיד בעיקר לאחת מתת-היחידות הגדולות של AP-4 בקרבת ה-N-טרמינוס שלה, באופן דומה למה שנמצא בקומפלקסי AP אחרים. באופן מפתיע, קשירת ARF1 אינה מעוררת ארגון מבני דרמטי ב-AP-4. הצורות הסגורה והפתוחה עדיין שורדות יחד, והארכיטקטורה הכוללת של הקומפלקס נשארת ברובה ללא שינוי. בדיקות ביוכימיות אישרו שמגעים ספציפיים בין ARF1 ל-AP-4 חיוניים לגיוס לממברנה, אך ARF1 לבדו אינו נועל את AP-4 למצב פעיל יחיד.
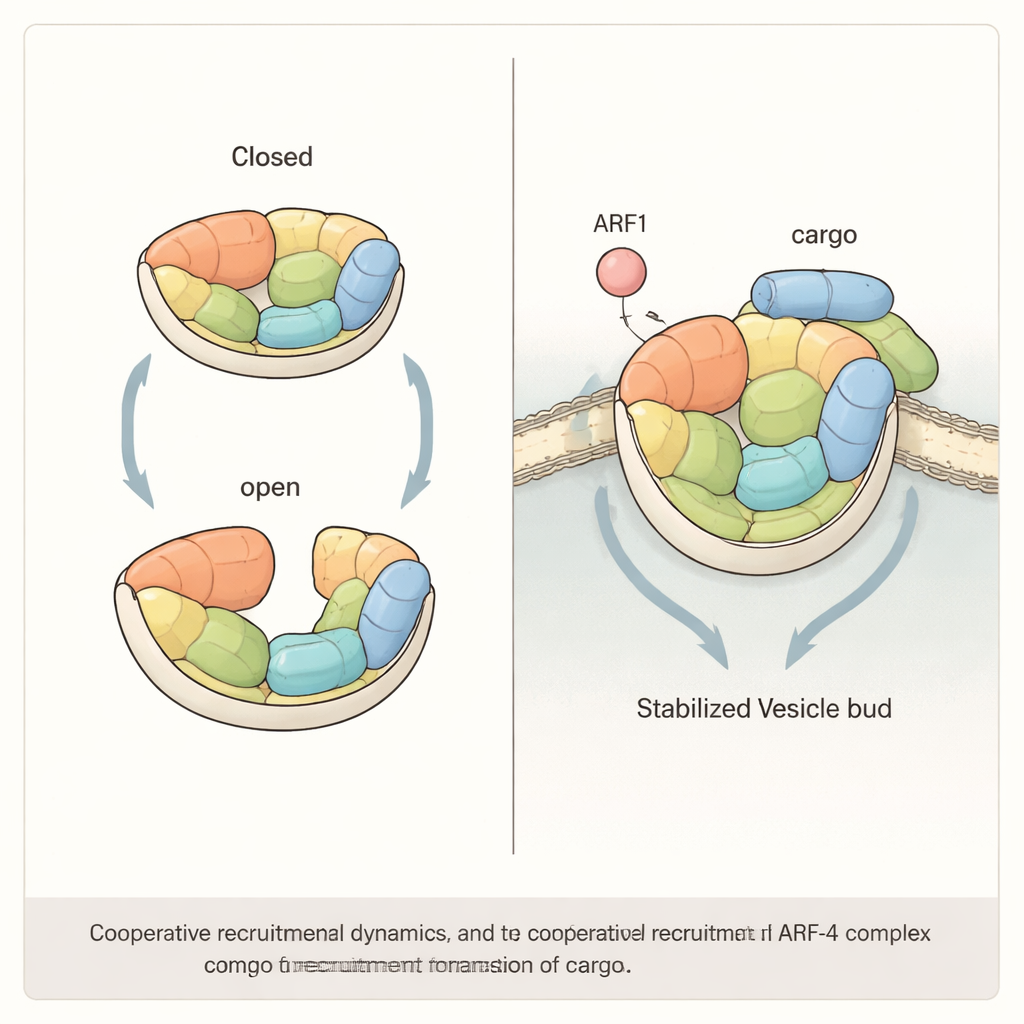
שיתוף פעולה בין מווסת למטען
המחקר מראה בנוסף כי גיוס יעיל של AP-4 לממברנות ככל הנראה דורש שיתוף פעולה בין ARF1 לחלבוני המטען עצמם. על ידי שיחזור המערכת על חרוזים וליפוזומים מלאכותיים, המחברים מצאו ש-ARF1 או זנב קצר של המטען ATG9A יכולים למשוך AP-4, אבל כאשר שניהם נמצאים יחד הם מושכים הרבה יותר AP-4 מהצפוי מסכום ההשפעות הבודדות שלהם. כאשר החוקרים הנדסו מוטציות שהקשיחו את מבנה AP-4 — מה שהפחית את יכולתו לנוע בין מצבי פתיחה וסגירה — האפקט הסינרגיסטי הזה אבדה. בתאים אנושיים שחסרו תת-יחידה מרכזית של AP-4, החזרת גרסאות מוטנטיות "קשיחות" בלבד של הקומפלקס כשלו בהושבת תנועת ATG9A מהגולג'י, מה שמדגיש שהגמישות של AP-4 אינה רק סקרנות אלא דרישה תפקודית.
מדוע הגמישות חשובה לבריאות המוח
בסך הכול, העבודה מציירת את AP-4 כמתווך שמשנה צורה ומדגמם קונפורמציות מרובות בתמיסה ועל ממברנות. במקום לפעול כמפסק דלוק/כבוי, ARF1 משמש כמגייס מבוסס ממברנה שעובד יחד עם חלבוני מטען לייצוב AP-4 בקונפיגורציות פרודוקטיביות להיווצרות בועיות. שיבוש האיזון הזה — בין אם על ידי החלשת קשירת ARF1 או המטען ובין אם על ידי הקפאת AP-4 לצורה אחת — פוגע ביצוא מטען מהגולג'י ועלול לתרום למחלות בהתפתחות העצבים. על ידי חשיפת הבסיס המבני להתנהגות הדינמית של AP-4, המחקר מספק מסגרת להבנת הפרעות הקשורות ל-AP-4 ומרמז על אסטרטגיות עתידיות לשיקום תנועתיות תקינה בנוירונים מושפעים.
ציטוט: Wang, Y., Li, W., Qiu, Y. et al. Structural basis for the dynamic conformations of AP-4 and its association with ARF1. Nat Commun 17, 1897 (2026). https://doi.org/10.1038/s41467-026-68679-8
מילות מפתח: מִסְלוּחַת ממברנה, קומפלקס המתווך AP-4, ARF1, היווצרות שלפוחיות, הפרעה בהתפתחות העצבים