Clear Sky Science · he
תאי NK חיוביים ל-ZNF683 שולטים ברגישות לכימותרפיה בקרב HPSCC מתקדם באמצעות עיצוב מחדש של המיקרו‑סביבה החיסונית
למה כימותרפיה עובדת טוב יותר בחלק מסוגי סרטן הגרון
אנשים עם קרצינומה קשקשית של ההיפופרינקס המתקדם — גידול הנמצא עמוק בגרון — לעתים קרובות עוברים כימותרפיה קשה עם תוצאות לא ודאיות. אצל חלק מהחולים הגידול נסוג בחדות, בעוד שאצל אחרים כמעט אין שינוי. המחקר שואל שאלה פשוטה אך מכרעת: מה שונה בתוך הגידולים שמגיבים היטב? באמצעות בחינה של תאי המערכת החיסונית פרט-פרט, החוקרים חושפים סוג מסוים של תא "שומר" שיכול להטות את הכף בין הצלחה לכישלון של הכימותרפיה הסטנדרטית.
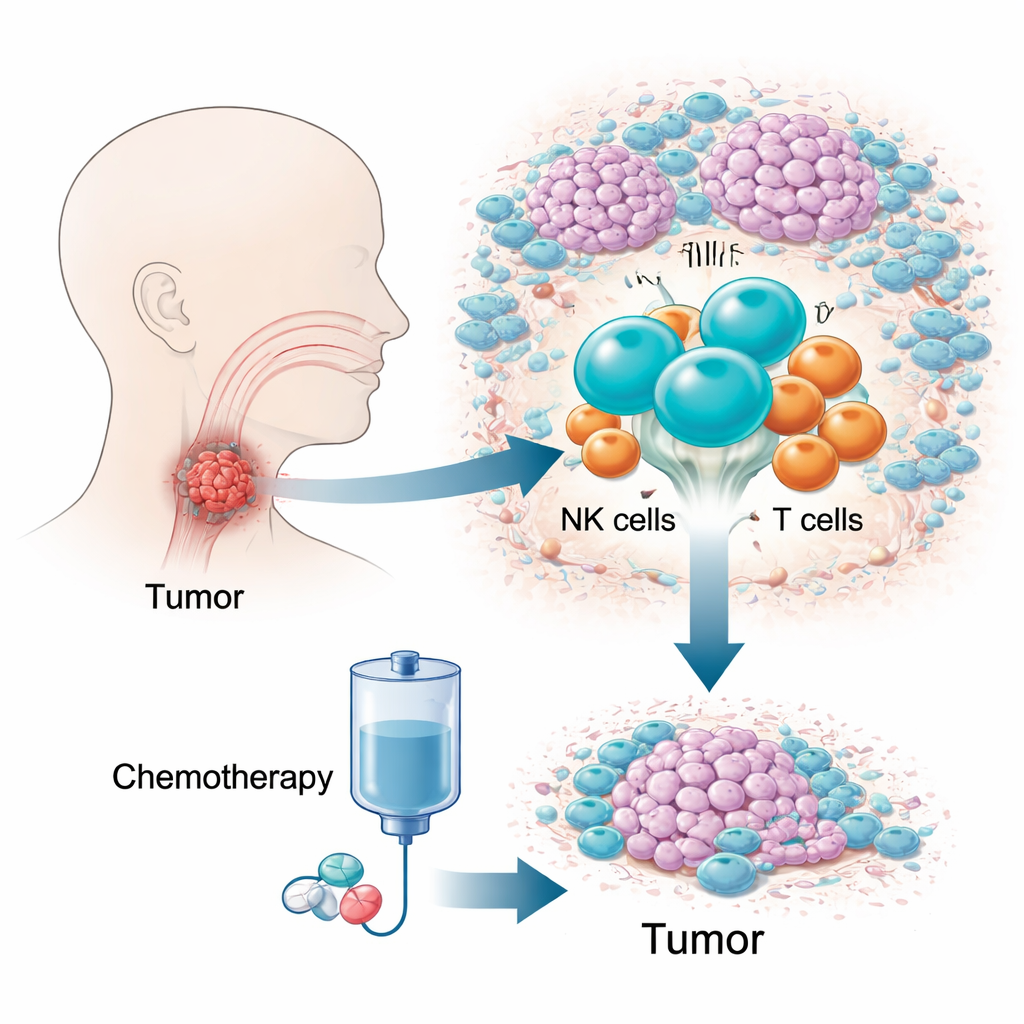
האתגר של גידול מוסתר וקשה לטיפול
קרצינומה קשקשית של ההיפופרינקס היא אחד מסוגי סרטן הראש והצוואר הקטלניים ביותר, בין השאר משום שהיא גדלה באזור צפוף וקשה לבחינה וגורמת למעט סימפטומים בשלבים המוקדמים. מטופלים רבים מאובחנים מאוחר, כאשר האפשרויות מוגבלות ושיעור ההישרדות לחמש שנים נמוך. שילוב תרופתי הידוע כ‑TPF נמצא בשימוש נרחב כי הוא יכול לשלוט במחלה תוך שמירה על תפקוד מיתרי הקול. עם זאת, אצל 10–20 אחוזים מהחולים נצפה מעט או אפס תגובה, מה שמוביל לאובדן זמן יקר. מבחני גנום מסורתיים, שממוצעים אותות על פני מיליוני תאים, התקשו להסביר את ההבדל הזה, ולכן המחברים פנו לחקור את האקוסיסטמה החיה של תאי החיסון בגידול.
קריאת הנוף החיסוני של הגידול תא אחר תא
החוקרים עקבו אחרי 12 חולים לאורך זמן, אספו דגימות גידול לפני ואחרי שני מחזורים של כימותרפיית TPF ופרופילו יותר מ‑150,000 תאי חיסון ברזולוציה של תא יחיד. הם גם בדקו 41 חולים נוספים לאימות ממצאים מרכזיים באמצעות דימות וציטומטריית זרימה. על ידי מיפוי פעילות הגנים וסוג כל תא הם בנו מפה מפורטת של המיקרו‑סביבה הגידולית: תאי T, תאי B, מאקרופאגים, תאי דנדריט, תאי פיטום, נויטרופילים ותאי NK (טבעיים הרגנים). מתוך כל השחקנים הללו, דפוס אחד בלט. לפני הטיפול, בגידולים שעברו כיווץ לאחר מכן היו הרבה יותר תאי NK מאשר בגידולים שהתנגדו לטיפול, וככל ששיעור תאי ה‑NK היה גבוה יותר, כך היה כיווץ הגידול הגדול יותר בסופו של דבר.
תת־קבוצה מיוחדת של תאי NK מכינה את תאי ה‑T להצלחה
בהעמקה, הצוות חילק את תאי ה‑NK לשלוש קבוצות על בסיס מאפיינים מולקולריים. רק אחת מהן, המסומנת על ידי גורם השעתוק ZNF683 ונמצאת בעיקר ברקמה שסביב מאורות הגידול, התקשרה בעוצמה עם תגובת כימותרפיה טובה. חולים שלגידולם היו יותר תאי NK חיוביים ל‑ZNF683 בבסיס היו בעלי סיכוי רב יותר להפיק תועלת מ‑TPF. בניסויים בעכברים, הסרת תאי NK מחקה כמעט לגמרי את היתרון של הכימותרפיה, מה שאישר כי פעילות ה‑NK אינה רק סמן אלא דרישה לטיפול יעיל. באופן מעניין, תאי NK אלה לא פעלו רק כרוצחים ישירים של סרטן; במקום זאת, תוכניות הגנים שלהם הוגברו ביחס להנחיה והפעלת תאי T.
איך תאי NK מאפשרים לתאי T להרוג גידולים בעוצמה
כדי להבין אילו תאי T הם המכריעים, המדענים עקבו אחרי קלונות של רצפטור התא‑T לפני ואחרי הטיפול. הם מצאו שבמגיבים הייתה התרחבות דרמטית של קבוצה מסוימת של תאי CD8 "זיכרון אפקטורי", העשירה במולקולה בשם GZMK, לאחר הכימותרפיה. תאים אלה ייצרו רמות גבוהות של ציטוקינים רעילים כמו TNF ואינטרפרון‑גאמא מבלי להראות תשישות עמוקה, מה שהופך אותם לרוצחים חזקים ועמידים. דימות מרחבי הראה כי לאחר הטיפול, תאי CD8 החיוביים ל‑GZMK התקבצו בעוצמה בתוך הגידולים של המגיבים אך לא באלה של הלא‑מגיבים. בניסויי תרבית משותפת במעבדה עם תאים אנושיים, מגע ישיר עם תאי NK חיוביים ל‑ZNF683 נהג בהרחבה של תת‑הקבוצה הזו של תאי CD8 GZMK+, השפעה שנמוגה כאשר התאים הופרדו במחסום.
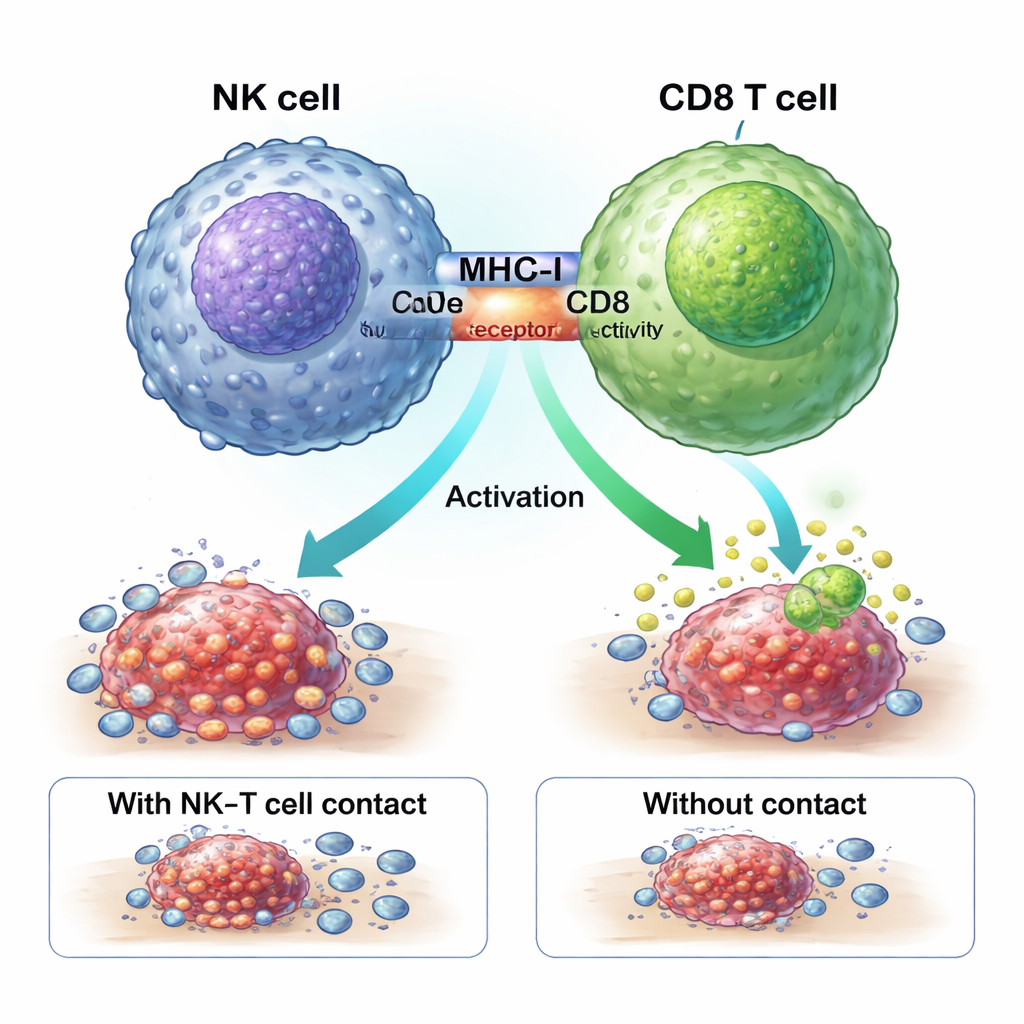
לחיצת יד פיזית שמפעילה לוחמים נגד הגידול
המחקר מראה שתאי NK חיוביים ל‑ZNF683 משפרים את תגובת הכימותרפיה באמצעות "לחיצת יד" פיזית עם תאי CD8. מולקולות מסוג MHC‑I על פני תא ה‑NK מעוררות את רצפטורי ה‑CD8 על תאי ה‑T באזור מגע צמוד, או הסינפסה החיסונית. חסימת MHC‑I עצרה את ייצור תאי ה‑CD8 החזקים החיוביים ל‑GZMK על ידי תאי ה‑NK. בעכברים מהונדסים במיוחד החסרים ZNF683 רק בתאי NK, תאי NK אלו הביעו פחות MHC‑I והיו פחות טובים בהפעלת תאי CD8, מה שמחזק את הרעיון ש‑ZNF683 מתכנת את תאי ה‑NK להיות מאמנים יעילים לתאי T ולא רק רוצחים פשוטים.
מה משמעות הממצאים לחולים
למסוג הקוראים שאינם מקצועיים, המסר המרכזי הוא שלא כל תאי החיסון בתוך גידול שווים. עבודה זו מזהה תת‑קבוצת תאי NK כסקאוטים מתקדמים שמכינים את שדה הקרב לפני תחילת הכימותרפיה. גידולים עשירים בתאים אלה ערוכים לשחרר גל של תאי CD8 חזקים כאשר התרופות מתחילות לפעול, מה שמוביל לכיווץ גידולי טוב בהרבה. מדידת שפע הציר הזה של NK–T לפני הטיפול יכולה לסייע לרופאים לחזות מי יהנה מ‑TPF ומי עשוי להזדקק לטיפולים חלופיים או משלימים. בעתיד, טיפולים שמגבירים או מחקים את תאי ה‑NK החיוביים ל‑ZNF683 עשויים להפוך גידולים עמידים של ההיפופרינקס לרגישים הרבה יותר לכימותרפיה הסטנדרטית.
ציטוט: Li, G., Xiao, W., Wu, H. et al. ZNF683+ NK cells govern chemotherapy sensitivity in advanced HPSCC via reshaping immune microenvironment. Nat Commun 17, 2069 (2026). https://doi.org/10.1038/s41467-026-68676-x
מילות מפתח: סרטן היפופרינקס, עמידות לכימותרפיה, תאי טבעיים הרגנים, מיקרו‑סביבה חיסונית של גידול, תאי CD8