Clear Sky Science · he
ויסות הרכבת המתאם AP1 על‑ידי החלבון המצ'פר בעל שתי ה'ידיים' MEA1
מדוע העוזר החבוי הזה בתא חשוב
בתוך כל תא אנושי, אלפי חבילות זעירות מעבירות חלבונים אל היעד הנכון או אל "מרכז המיחזור" התאי לפירוק. התנועה הזו שומרת על תקינות התאים ועל איזון ההגנה החיסונית. המאמר המסוכם כאן חושף חלבון שהיה קודם בלתי ברור, בשם MEA1, שמתברר כחשוב לבניית אחד ממכונות המיון שממלאות את החבילות הללו. הבנת פעילותו של MEA1 מסבירה כיצד תאים שולטות במטענים חשובים, כולל מולקולות שמדליקות ומכבות תגובות חיסוניות אנטי‑ויראליות.
פקוד תנועה במרכז המשלוחים של התא
רוב פעילות המשלוחים בתא עוברת דרך מבנה בשם גולג'י, ערמת שקיות שטוחות שפועלת כמו דואר מרכזי. מהגולג'י ניתן לשלוח מטען לשימוש במעטפת התא או להטות אותו למחלקות פנימיות לפירוק. קומפלקס חלבוני המכונה AP1 נמצא בלב מסלול זה. AP1 מזהה תגים על חלבוני מטען, מסייע לכופף את הממברנה ומגייס מעטה חיצוני של קלתרין ליצירת וזיקולות תחבורה קטנות. ללא הרכבה נכונה של AP1, מטענים קריטיים מצטברים במקומות הלא נכונים ונתיבים איתות רגילים, כולל אלה שקשורים לחסינות, עלולים להשתבש. 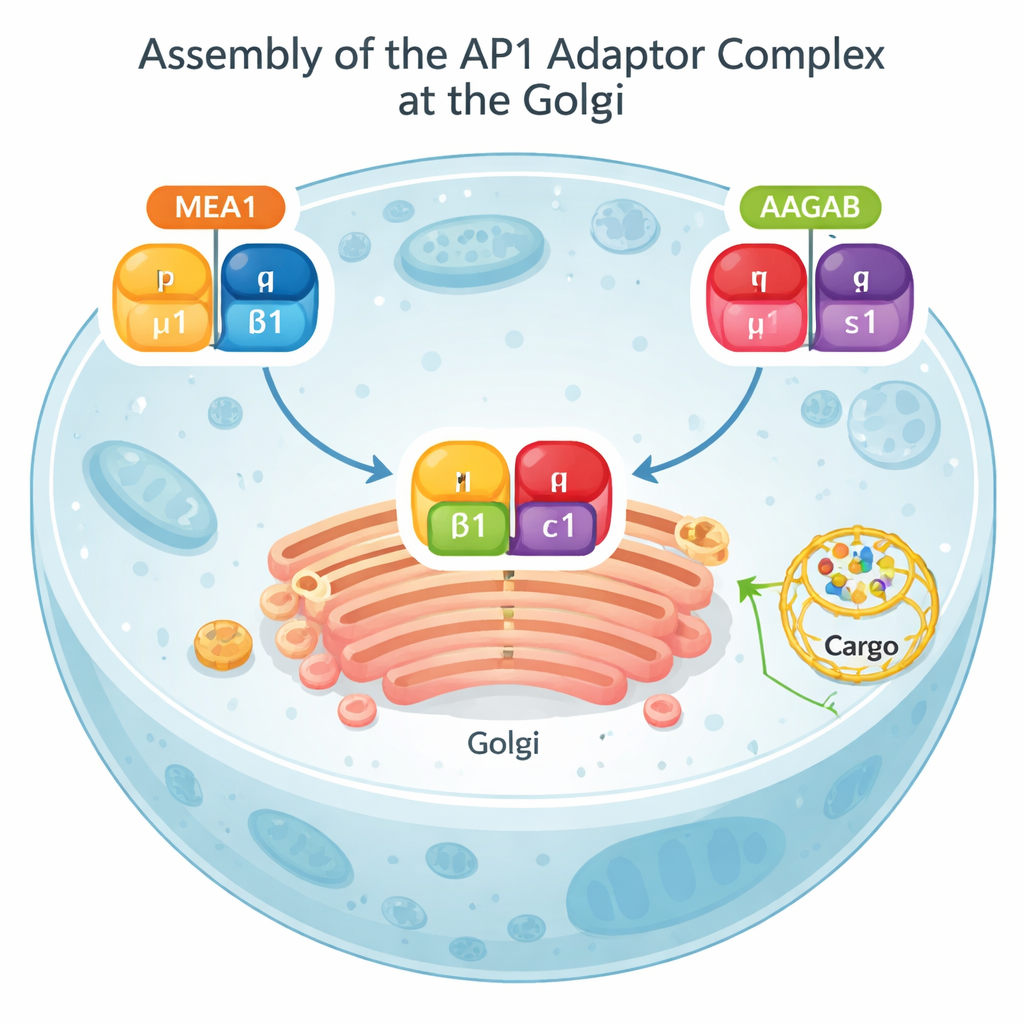
מציאת פועל הרכבה חסר
המחברים יצאו לזהות חלבונים שנקשרים פיזית ל‑AP1 ועשויים לסייע בהרכבתו. הם חפרו במסד נתונים גדול של אינטראקציות חלבון‑חלבון, סיננו מועמדים שסביר שלא יעבדו עם AP1, ואז השתמשו בכלי בינה מלאכותית, AlphaFold, כדי לחזות כיצד החלבונים הנותרים עשויים למגע עם חלקי ה‑AP1 השונים. החיפוש הבהיר את חשיבותו של MEA1, חלבון קטן שטרם תואר ונמצא ברקמות רבות. ניסויים המשך בתאים אנושיים אישרו כי MEA1 קושר שני תת‑יחידות ספציפיות של AP1, הנקראות μ1 ו‑β1, הן כשנבדקו בנפרד והן בצורתן הטבעית הבלתי‑מועברת.
MEA1 שומר על שלמות AP1 ועל זרימת המטענים בתא
כדי לחקור מה MEA1 עושה בפועל, החוקרים מחקו את גן MEA1 בקווי תאים אנושיים. בהעדר MEA1, כל ארבעת החלקים של AP1 הופחתו באופן דרסטי ונקודות האפיון של AP1 בסמוך לגולג'י כמעט ונעלמו. לאובדן זה היו השלכות פונקציונליות ברורות. מטען אחד של AP1, הרצפטור לחומצה פולית FOLR1, הצטבר על פני התא במקום להישלח פנימה — סימן מובהק לבעיית מיון על ידי AP1. מטען נוסף, חלבון האיתות החיסוני STING, כבר לא נארז ביעילות לוזיקולות בדרכן לליזוזומים, מרכזי המיחזור של התא. כתוצאה מכך, STING מוּפעַל ו־TBK1 הקינאז השותף שלו נשארו ברמות גבוהות, מה שמצביע על כך שהמתג המכבוי של מסלול אנטי‑ויראלי זה לא עבד כראוי. החזרת MEA1 לתאים השיבה את רמות ה‑AP1 ותיקנה את ליקויי התחבורה הללו.
מצ'פרון דו‑ידני ותהליך בנייה המבוסס התנגשות
בדיקות ביוכימיות ודגמי AlphaFold הראו ש‑MEA1 מתנהג כמו מצ'פרון הרכבה "דו‑ידני": החלק הקדמי שלו אוחז בתת‑היחידה μ1, בעוד שהחלק האחורי אוחז ב‑β1. כשמצויים בפני עצמם, μ1 ו‑β1 אינם יציבים ונוטים להתאבך או להישחק; קשירתם ל‑MEA1 הופכת אותם מסיסים ומוכנים להרכבה. מצ'פרון ידוע נוסף, AAGAB, מבצע תפקיד מקביל עבור שתי תת‑היחידות הנותרות של AP1, γ ו‑σ1. כאשר קומפלקסי MEA1–μ1–β1 ו‑AAGAB–γ–σ1 נפגשים, תת‑היחידות משתלבות לקומפלקס AP1 ארבע‑חלקי שלם. ברגע זה, שני המצ'פרונים משחררים את ידיהם וחוזרים לנוזל התא, בעוד AP1 החדש נע אל הממברנות לבצע את עבודת המיון שלו. מנגנון ה"התנגשות‑הדו‑מצ'פרונית" הזה מראה שהרכבת AP1 מנוהלת בקפידה ולא נשענת על מפגשים אקראיים.
לקחים רחבים על בקרת איכות תאית
מעבר ל‑AP1, המחקר מרמז על אסטרטגיה כללית יותר שתאים עשויים להשתמש בה לבניית מגוון מכונות חלבוניות גדולות. MEA1 יכול גם לסייע באופן חלש בקומפלקס מתאם אחר בשם AP2, וביחד עם AAGAB ומצ'פרון שלישי בשם CCDC32, הוא ממחיש מסלול רחב יותר שהמחברים מכנים "הידרכת הרכבת חלבוני מתאם". בתוכנית זו, מצ'פרונים מיוחדים מייצבים תת‑יחידות שבירות, מביאים זוגות מתאימים יחד וחוסמים זמנית את אתרי קשירת המטען עד שהקומפלקס נבנה במלואו ובטוח לפריסה. 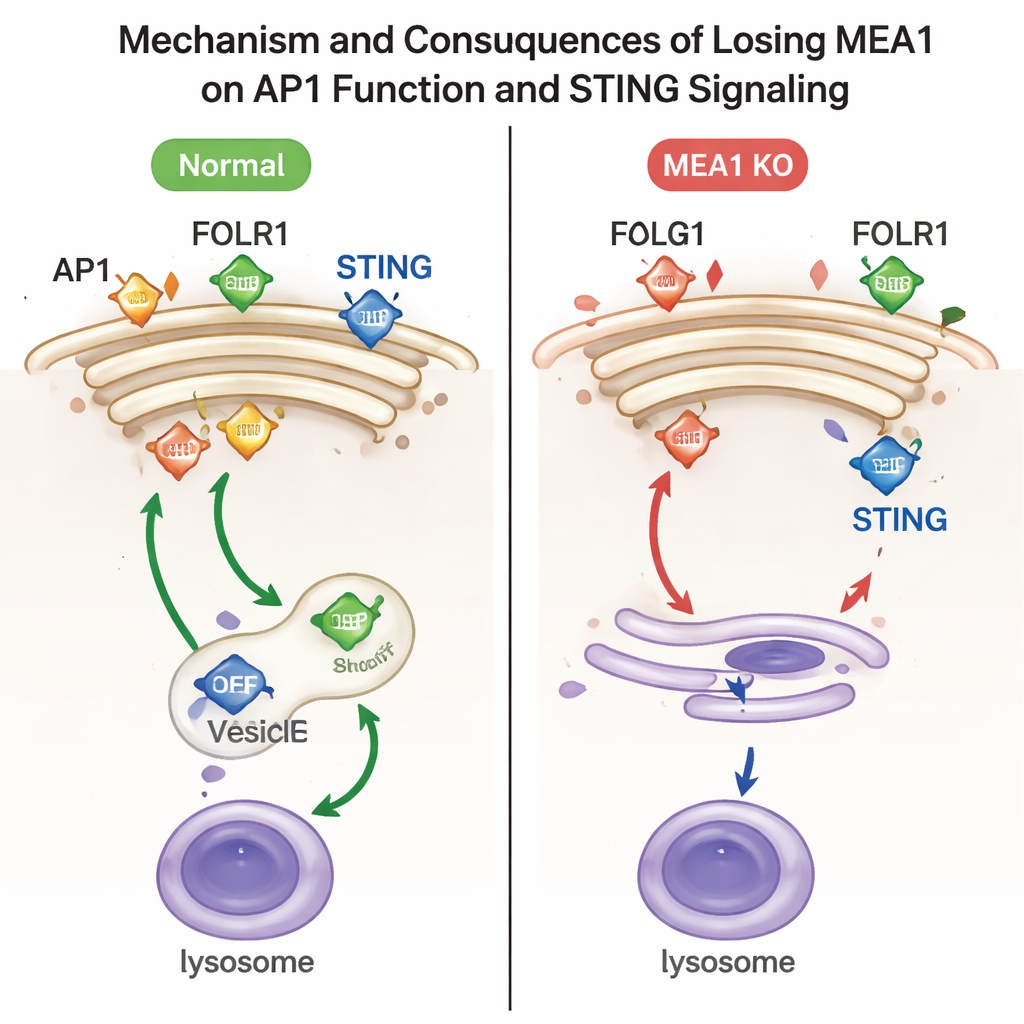
מה זה אומר לגבי בריאות ומחלה
עבור ציבור שאינו מומחה, המסקנה המרכזית היא ש‑MEA1 הוא פועל חשוב מאחורי הקלעים שסייע בהרכבת AP1, מכונת המיון הליבה בתאים שלנו. בהעדר MEA1, AP1 מתפרק, נוצרים צווארי בקבוק בתנועה התאית ומווסתים חשובים כמו STING אינם מכובים כיאות. ההבנה החדשה הזו עשויה בסופו של דבר לעזור להסביר מצבים חיסוניים מסוימים או מחלות נוספות שקשורות להובלת חלבונים לקויה, והיא חושפת עיקרון כללי לגבי האופן שבו תאים בונים בבטחה מכונות מולקולריות מורכבות מחלקים לא יציבים.
ציטוט: Wan, C., Wu, J., Ouyang, Y. et al. Regulation of AP1 adaptor assembly by the bi-handed chaperone MEA1. Nat Commun 17, 1876 (2026). https://doi.org/10.1038/s41467-026-68662-3
מילות מפתח: הובלת חלבונים, חלבון מתאם AP1, חלבוני מצ'פרונים מולקולריים, אותות STING, ביולוגיה תאית