Clear Sky Science · he
NeoPrecis: שיפור תחזית התגובה לאימונותרפיה באמצעות שילוב נאות של אימונוגניות ונוף הניואנטיגנים המודע לקלונליות
מדוע חלק מהסרטנים מגיבים לאימונותרפיה ואחרים לא
האימונותרפיה שינתה את הטיפול בסרטן, אך עדיין רבים מהמטופלים אינם נהנים ממנה וחלקם חווים תופעות לוואי משמעותיות. שאלה מרכזית היא מדוע חלק מהגידולים מזוהים ומוחרסים על ידי מערכת החיסון בעוד אחרים עוברים מתחת לרדאר. המחקר הזה מציג את NeoPrecis, שיטה חישובית הבוחנת ביתר דיוק את ה"דגלים" שהגידול מציג בפני מערכת החיסון — הניאואנטיגנים — ומשתמשת במידע הזה כדי לחזות טוב יותר אילו מטופלים צפויים להגיב לאימונותרפיות מודרניות.
דגלים חדשים על תאי הסרטן
תאי סרטן צוברים מוטציות ב‑DNA שיכולות לשנות את החלבונים שהם מייצרים. קטעים קטנים של חלבונים משונים אלה, המכונים ניאואנטיגנים, יכולים להופיע על פני התא ולהיראות כזרים על ידי תאי T — הרוצחים של מערכת החיסון. במשך שנים הרופאים והחוקרים הסתמכו על מדדים גסים כמו עומס המוטציות של הגידול — מספר המוטציות הכולל — כדי לאמוד את הסבירות לתגובה למעכבי נקודות בקרה חיסוניות. אבל זה כלי גס: לא כל מוטציה יוצרת מטרה נראית או מושכת עבור תאי T, וגידולים יכולים להיות פסיפס של תתי‑סוגי תאים שונים. NeoPrecis נועדה להתקדם מעבר לספירה פשוטה של מוטציות ולשפוט עד כמה מהן הן באמת מטרות מבטיחות על פני הגידול כולו.
בחינת שלושה מרכיבים עיקריים יחד
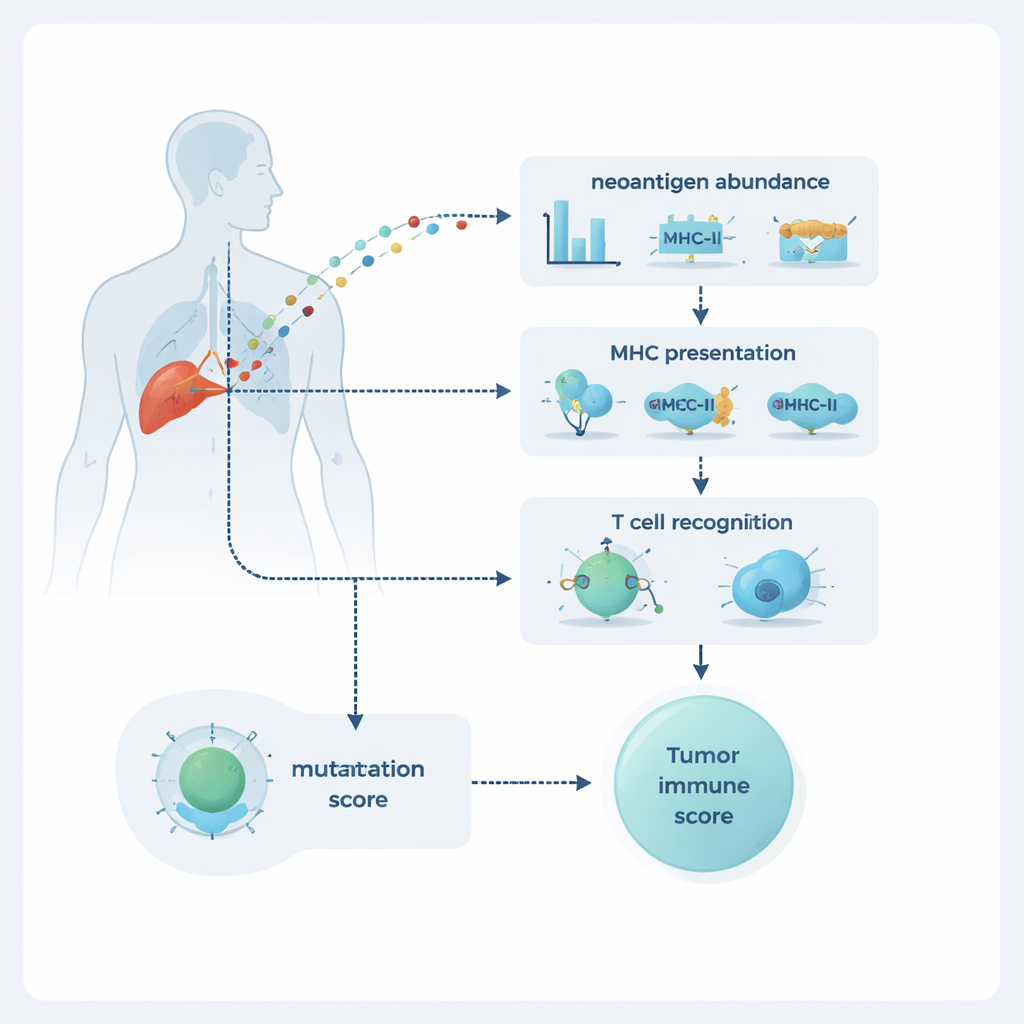
NeoPrecis מעריכה כל מוטציה לאורך שלושה ממדים: כמה היא שכיחה בגידול, האם סביר שתוצג על פני התא, וכמה סביר שתזוהה על ידי תאי T. השכיחות מוערכת באמצעות רציפת DNA ו‑RNA, שממחישות כמה המוטציה נפוצה וכמה היא מבוטאת. הצגה מודללית דרך קשירה למולקולות הנקראות MHC מחלקה I ו‑II, שפועלות כמו שלטי חוצות המציגים קטעי חלבון לתאי T. החלק החדשני ביותר הוא רכיב זיהוי תאי ה‑T, NeoPrecis‑Immuno. המודל הזה לומד ממסדי נתונים גדולים של אינטראקציות ידועות בין תאי T לפפטידים כדי להעריך עד כמה קטע משונה שונה מהמקביל התקין באופן שחשוב לזיהוי על ידי תאי T, ובמקביל מתחשב בווריאנטים הספציפיים של MHC שכל אדם נושא.
להשכיל את המחשב מה שתאי T "רואים"
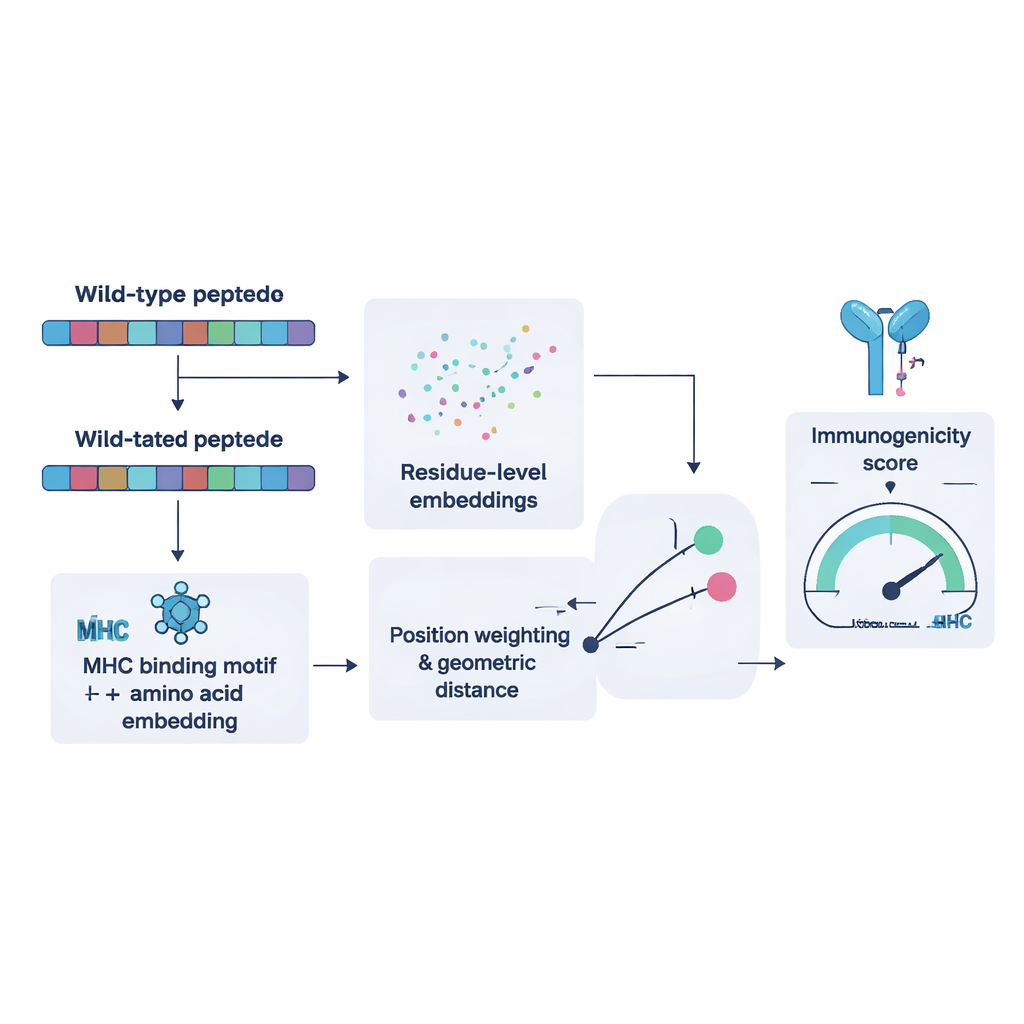
לצורך אימון NeoPrecis‑Immuno אספו החוקרים אלפי דוגמאות שבהן אותו תא T מכיר מספר פפטידים דומים ואחרות שאינן מזוהות. הם השתמשו בדוגמאות אלה כדי ללמד את המודל שקטעים מוטנטים הדומים מאוד לקטעים נורמליים פחות סבירים לעורר תגובה חיסונית, משום שמטרות דמויות‑עצמי לרוב מסוננות במהלך התפתחות תאי ה‑T. המודל מייצג כל פפטיד כנקודה במרחב מתמטי המכוון על ידי רצף חומצות האמינו שלו והעדפות הקשירה של מולקולות MHC של האדם. לאחר מכן הוא מודד כמה רחוק הפפטיד המוטנט נמצא מהמקור. מרחקים גדולים יותר — המותנים במוטיבים — תואמים לסבירות גבוהה יותר לאימונוגניות. בבדיקות מול כלים קיימים על מערכי נתונים עצמאיים של סרטן, NeoPrecis‑Immuno השווה או עלה עליהם, במיוחד בעבודה עם MHC מחלקה II, המעריכה הצגה לתאי T מסייעים התומכים ומחזקים תגובות נגד‑גידול.
ממוטציות בודדות אל הגידול השלם
מוטציות בודדות הן רק חלק מהתמונה; גם האופן שבו הן מפוזרות בתוך הגידול משפיע. חלק מהמוטציות הן "קלונליות", נמצאות כמעט בכל תא סרטן, בעוד אחרות "תת‑קלונליות", נוכחות רק בכיסים מסוימים. NeoPrecis בונה "נוף ניאואנטיגנים" על‑ידי סכימה של ציוני האימונוגניות שלו על פני המוטציות ושכבת מידע לגבי לאילו תתי‑קלונים הן שייכות וכמה נפוצים תתי‑הקלונים האלה. כך מתקבלים ציוני‑גידול המדגישים סרטנים עשירים בניאואנטיגנים חזקים ומשותפים לרבים — במיוחד כאלה הניתנים להצגה גם על MHC מחלקה I וגם על מחלקה II ויכולים לעורר תגובות מתואמות של תאי T מסייעים ורוצחים. בקבוצות מטופלים עם מלנומה וסרטן ריאה שלא‑קטיני שהתמודדו עם מעכבי נקודות בקרה, ציוני NeoPrecis הבחינו במגיבים ובלא‑מגיבים באופן מדויק יותר מאשר ספירת מוטציות סטנדרטית, והיו מועילים במיוחד בגידולים ריאתיים מורכבים והטרוגניים.
מה המשמעות עבור מטופלים
עבור מטופלים, ההבטחה של NeoPrecis היא התאמה מדויקת יותר של אימונותרפיות לאלו שצפויים להרוויח, והבנה ברורה יותר מדוע חלק מהגידולים עמידים לטיפול. באמצעות התמקדות באיכות ובפיזור של הניאואנטיגנים — לא רק בכמותם — המסגרת מסבירה מדוע גידולים בעלי עומסי מוטציות דומים יכולים להתנהג בצורה שונה לחלוטין. בעתיד, מפות מפורטות כאלה של הנוף הנראה‑חיסוני של הגידול עשויות לכוון לא רק את השימוש במעכבי נקודות בקרה, אלא גם את העיצוב של חיסונים מותאמים אישית נגד סרטן, שיותאמו למקד את המטרות החזקות והרחבות‑השיתוף ביותר בכל סרטן של מטופל.
ציטוט: Lee, KH., Sears, T.J., Zanetti, M. et al. NeoPrecis: enhancing immunotherapy response prediction through integration of qualified immunogenicity and clonality-aware neoantigen landscapes. Nat Commun 17, 1966 (2026). https://doi.org/10.1038/s41467-026-68651-6
מילות מפתח: אימונותרפיה בסרטן, ניואנטיגנים, הטרוגניות של הגידול, מעכבי צירים חיסוניים, אונקולוגיה חישובית