Clear Sky Science · he
הנדסת מערכת MmeFz2-ωRNA לעריכה גנומית יעילה באמצעות מסגרת משולבת חישובית-ניסויית
מספרי גנים קטנים לבעיות רפואיות גדולות
עריכת גנים כבר שינתה את האופן שבו מדענים חוקרים מחלות, אך להפוך אותה לתרופות בטוחות ומעשיות עדיין מהווה אתגר מרכזי. מכשול גדול הוא שה"מספרי" הדנ"א החזקים של היום, כמו CRISPR-Cas9, הם פיזית גדולים וקשה לארוז אותם לתוך כלי ההעברה הזעירים המשמשים בחולים. במחקר זה מוצג כלי עריכה גנומית קומפקטי חדש, מבוסס על משפחת אנזימים מוכרת פחות בשם Fanzor2, ומודגם כיצד בינה מלאכותית יכולה לשכתב אותו במהירות למועמד חזק לטיפולים גנטיים עתידיים.
מחלקה חדשה של עורכי גנים קומפקטיים
רוב עורכי הגנום הנוכחיים, כגון Cas9 ו-Cas12a, הם חלבונים כבדים המורכבים יותר מאלף שיירים אמינו. הגודל הזה מקשה על דחיסתם לנגיפי AAV (adeno-associated viruses), מערכת ההעברה המובילה בתרפיות גנטיות. לעומת זאת, חלבוני Fanzor2 קטנים בהרבה ומצויים באופן טבעי באאוקריוטים — הענף של החיים שכולל בעלי חיים ובני אדם. החוקרים התמקדו בחבר אחד במשפחה זו, MmeFz2, המשתמש במולקולת RNA קצרה בשם ωRNA כדי לזהות ולחתוך רצפי דנ"א ספציפיים. על הנייר MmeFz2 נראה אידיאלי לטיפול: קומפקטי ותכנותי. בפועל, עם זאת, הפעילות שלו בתאי אדם הייתה חלשה ביותר, כאשר נמנע עריכה בלפחות אחוז אחד מהאתרים המיועדים. הצוות הציב לעצמו מטרה להפוך את האנזים הזה לכלי מעשי.
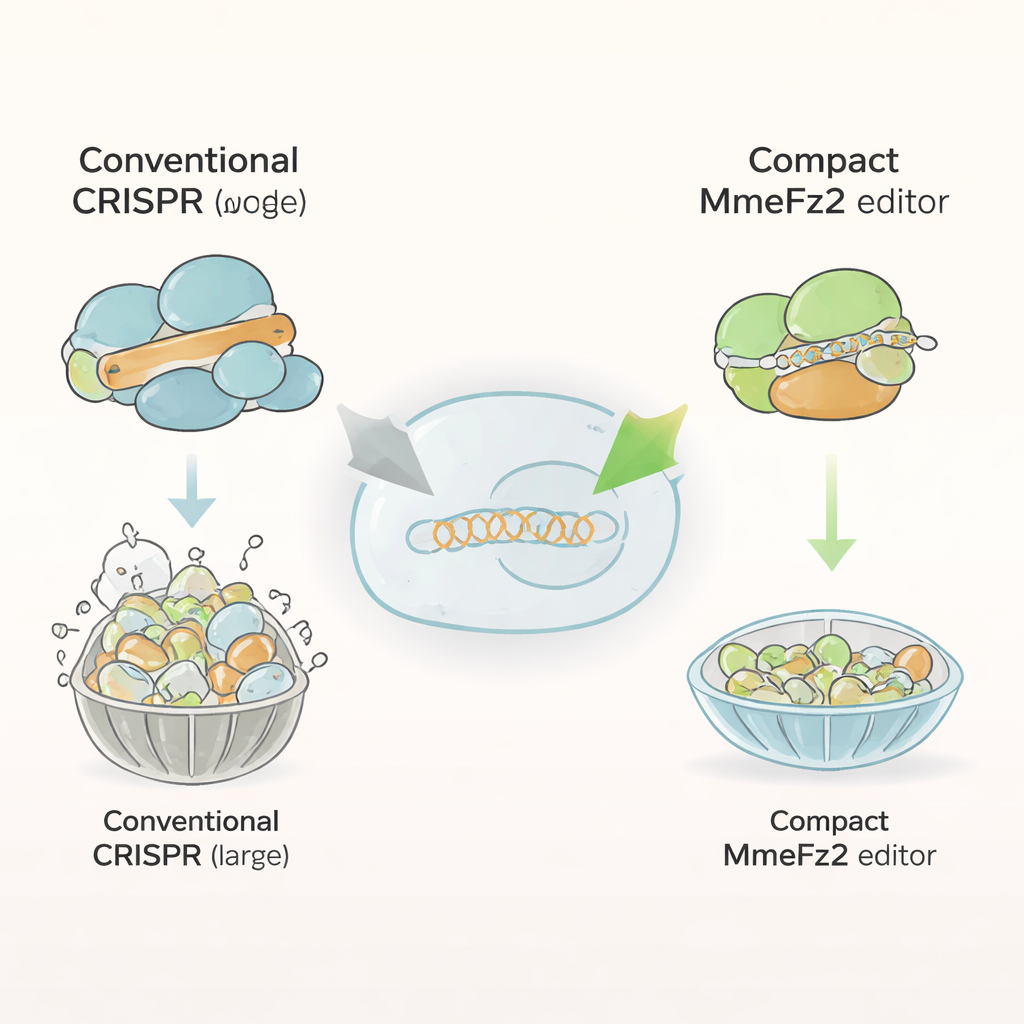
שימוש בבינה מלאכותית לעיצוב מולקולת המדריך
היעד הראשון היה ה-ωRNA — המדריך שאומר ל-MmeFz2 היכן לחתוך. בעזרת AlphaFold3, תוכנית מתקדמת החוזה מבנים תלת־ממדיים של קומפלקסים חלבון–RNA–DNA, החוקרים בנו מודל של MmeFz2 קשור ל-ωRNA ולמטרת דנ"א. המבנה הווירטואלי הגליל שכללים מסוימים של ה-ωRNA היו רפויים, בעלי זוגיות לקויה וכמעט לא נגעו בחלבון. בהנחיית מידע זה, הקבוצה החליפה באופן שיטתי קישורים לא יציבים ב-RNA והסירה רצפי יורידין שיכולים להפריע לתעתוק. לאחר מכן הם בחנו עשרות וריאנטים בתאי אדם. על ידי צבירת השינויים הטובים ביותר וגזירת אזור גבעול מיותר, הם יצרו ωRNA מקוצר קטן ב-30% ובכל זאת הניב קפיצה של כמעט פי 20 ביעילות העריכה במספר רב של אתרי דנ"א.
כיוונון החלבון באמצעות למידת מכונה
בהמשך שיפרו את החלבון עצמו. שוב נעזרו ב-AlphaFold3 כדי למפות היכן MmeFz2 נוגע ב-RNA וב-DNA ובעיצבו מעל מאה שינויים של חומצת אמינו בודדת שנועדו להעצים את המגעים או לשפר את הגמישות. לאחר סינון של וריאנטים אלה בתאים, הזינו את נתוני הביצועים למערכת EVOLVEpro — מערכת למידת מכונה שבנויה על מודלי שפה לחלבונים המאומנים ממיליוני רצפים טבעיים. הכלי למד אילו תכונות נוטות להגביר פעילות והציע קומבינציות חדשות של מוטציות שחזויות כיעילות עוד יותר. לאחר מספר סבבים של הלולאה החישובית–ניסויית הזו, החוקרים הגיעו לשני וריאנטים אנזימטיים מותאמים שבעזרתם, יחד עם ה-ωRNA המשופר, הוכפלו פעילות העריכה ביותר מפי 60 ביחס למערכת ההתחלתית.
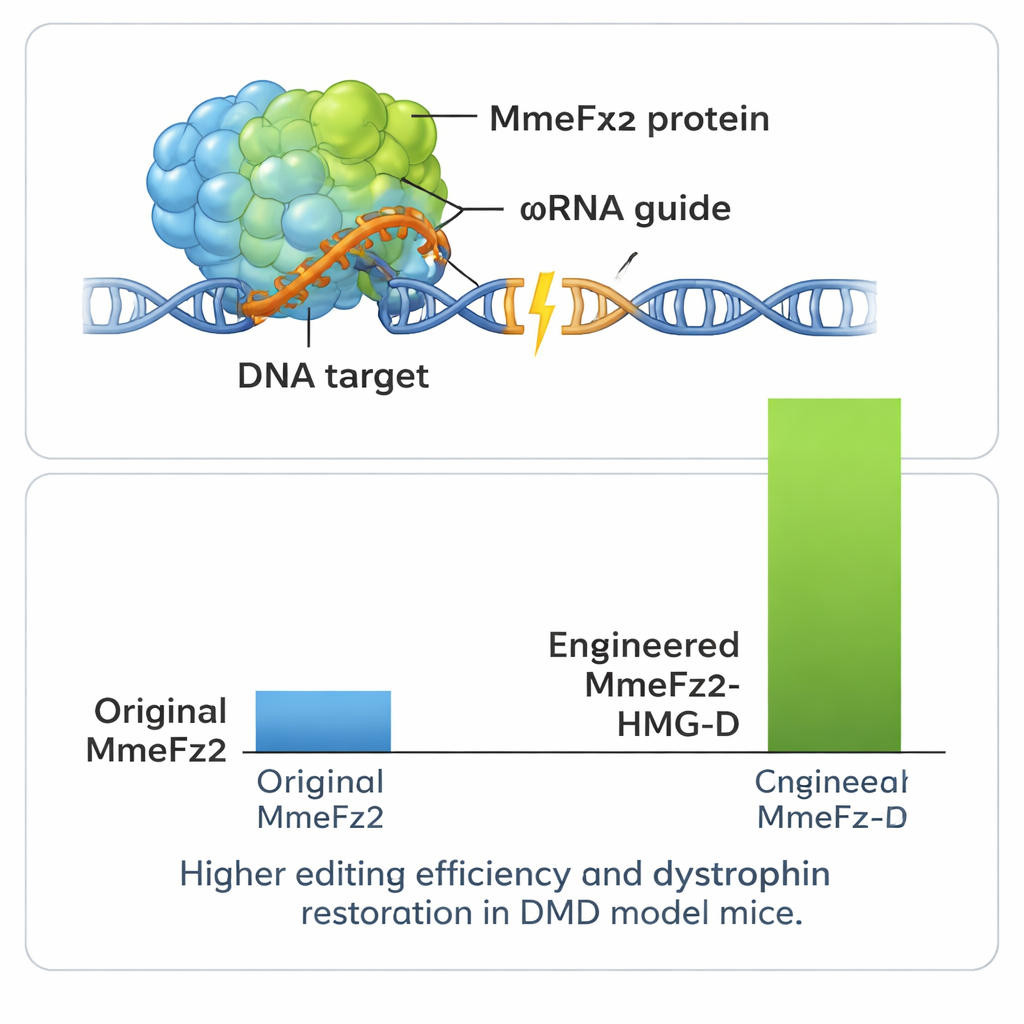
הגברת הכוח ובחינה במודל מחלה
כדי להפיק עוד ביצועים מהמערכת, המחברים חיברו את MmeFz2 לתחומי קשירת דנ"א קטנים שעוזרים לחלבון להיצמד לחומר הגנטי. אחד מהם, בשם HMG-D, הוכיח עצמו כמאד יעיל כאשר הוא צמוד לסוף האנזים המעוצב, והניב רמות עריכה מעל 80% בחלק מהאתרים. חשוב לציין, בדיקות באתרים משוערים של מיקומים מחוץ למטרה בגנום הראו שההגברה הזו לא לוותה באובדן משמעותי של דיוק. מכיוון שעורך הגנים כולו — כולל החלבון ו-RNA המדריך — כל כך קומפקטי, הוא נכנס בנוחות לווקטור AAV יחיד, דבר שאינו אפשרי עבור רוב מערכות ה-CRISPR. הצוות ניצל יתרון זה במודל עכבר למחלת דושן, הפרעה קטלנית של התנוונות שרירים הנגרמת על ידי שגיאות בגֵן דיסטורפין. הזרקה חד-פעמית של העורך המסופק ב-AAV לשריר הרגל הובילה לתיקונים ניתנים לזיהוי ב-RNA של הגֵן ולשחזור חלבון הדיסטורפין בשיעור משמעותי של סיבי השריר.
מה משמעות הדבר לתרפיות גנטיות עתידיות
עבור קהל שאינו מומחה, המסר המרכזי הוא שהמחברים הפכו אנזים חיתוך גנים חלש ומעט מוכר לעורך קומפקטי ובעל ביצועים גבוהים שניתן לספק בחבילה ויראלית יחידה ויכול לתקן מחלה גנטית קשה במודל חיה ריאלי. לא פחות חשוב הוא האופן שבו הגיעו לשם: באמצעות שילוב הדוק של חיזוי מבנה מבוסס AI ולמידת מכונה עם מבחנים מעבדתיים ממוקדים, הם שיפרו הן את החלבון והן את ה-RNA המדריך ביעילות רבה יותר מאשר שיטות ניסוי וטעייה מסורתיות. אסטרטגיה משולבת זו עשויה להאיץ את יצירתם של עורכי גנום רבים מדור-הבא, ולהביא תרפיות גנטיות מדויקות ובטוחות יותר קרובות לחולים בסוגי דיסטורפיה שרירית ומחלות תורשתיות נוספות.
ציטוט: Li, S., Xu, K., Li, G. et al. Engineering the MmeFz2-ωRNA system for efficient genome editing through an integrated computational-experimental framework. Nat Commun 17, 1867 (2026). https://doi.org/10.1038/s41467-026-68644-5
מילות מפתח: עריכת גנים, אלטרנטיבות ל-CRISPR, דושן מדיוליס דיסטורפי, תרפיה גנטית תוך-ויראלית, בינה מלאכותית בביולוגיה