Clear Sky Science · he
הערכת יציבות קיפול חלבון בהתחשבות מפורשת במצבי שאינם מקופלים
מדוע יציבות חלבון חשובה
כל חלבון בגופך הוא מנוע מולקולרי זעיר שצריך להתקפל לצורה תלת‑ממדית מדויקת כדי לתפקד כראוי. אם הקיפול הזה עדין מדי, החלבון עלול לתפקד באופן שגוי, להצטבר בקבוצות, או שלא להיוצר כלל — בעיות המקושרות למחלות ולכישלונות בייצור תרופות וחומצות אמינו מבוססות חלבון. מדידה של יציבות חלבון במעבדה היא איטית ומורכבת, ולכן מדענים מחפשים שיטות מחשב שיכולות לומר באופן אמין, מתוך הרצף בלבד, עד כמה בקלות חלבון יתפרק.
מבט חדש על חלבונים מקופלים ושאינם מקופלים
רוב האלגוריתמים המודרניים מתמקדים בעיקר בצורתו המקופלת של החלבון. הם לרוב מתחילים ממבנה חזוי בידי בינה מלאכותית, כמו AlphaFold, ומתייחסים למבנה יחיד זה כגורם העיקרי שקובע יציבות. אך היציבות היא למעשה פער האנרגיה בין שתי אנסמבלות רחבות: המצב המקופל הצפוף והצורות הרבות והרופפות שמרכיבות את המצב הבלתי מקופל. המחברים טוענים שההתעלמות מהצד הבלתי מקופל של האיזון הזה היא סיבה מרכזית לכך שכלים קיימים מתקשים להתאים למדידות הניסיוניות של אנרגיית הקיפול החופשית, הידועה כ‑ΔG.
מודל חדש שלומד את שני המצבים
החוקרים מציגים את IFUM, מערכת למידה עמוקה שנועדה להעריך את ΔG תוך כדי שלמידה על מאזן המצבים המקופל והבלתי מקופל עבור כל חלבון. במקום להתייחס למצב הבלתי מקופל כרקע מעורפל, IFUM משתמשת ברעיונות מפיזיקת פולימרים כדי לייצג אותו כ"כבל אקראי" ומקודדת הן את המצב המקופל והן את המצב הבלתי מקופל כמפות מרחקים בין זוגות חומצות אמינו. המודל מקבל מידע מרשתות רצף ומבנה מאומנות מראש חזקות, ואז חוזה במשותף את היציבות הכוללת ומפת הסתברות המתארת מהי חלקיות האוכלוסייה המקופלת לעומת הבלתי מקופלת עבור כל זוג רצפים. אימון על מאגר גדול מאוד של חלבונים קטנים המאופיינים ניסיונית וחלבונים ידועים כמיותרים מסייע ל‑IFUM לזהות גם רצפים מבניים היטב וגם רצפים רפויים.
תוצאות טובות יותר וכיסוי רחב יותר של מוטציות
כאשר נבדק על מאגר מבוקר בקפידה של חלבונים קטנים, IFUM חוזה ערכי ΔG ניסיוניים עם שגיאה נמוכה יותר וקורלציה גבוהה יותר מאשר שיטות מבוססות בינה מלאכותית קודמות שהתבססו אך ורק על המבנה המקופל או על מודלי שפה שאומנו על רצפים. באופן מהותי, המודל מטפל גם במגוון רחב של שינויים ברצף. הוא מתאר במדויק את השפעות מוטציות נקודה בודדות וכפולות, וכן החדרות ומחיקות שמשנות את אורך החלבון — מצבים שבהם כלים רבים קיימים נכשלו או לא נבנו לפעול. השוואה פנימית מראה שסילוק המטרה של מצב הבלתי מקופל מחמיר במידה ניכרת את הביצועים, מה שמדגיש כי מיפוי מפורש של האנסמבל הבלתי מקופל אינו רק נחמה רעיונית אלא מרכזי לדיוק החיזויים.
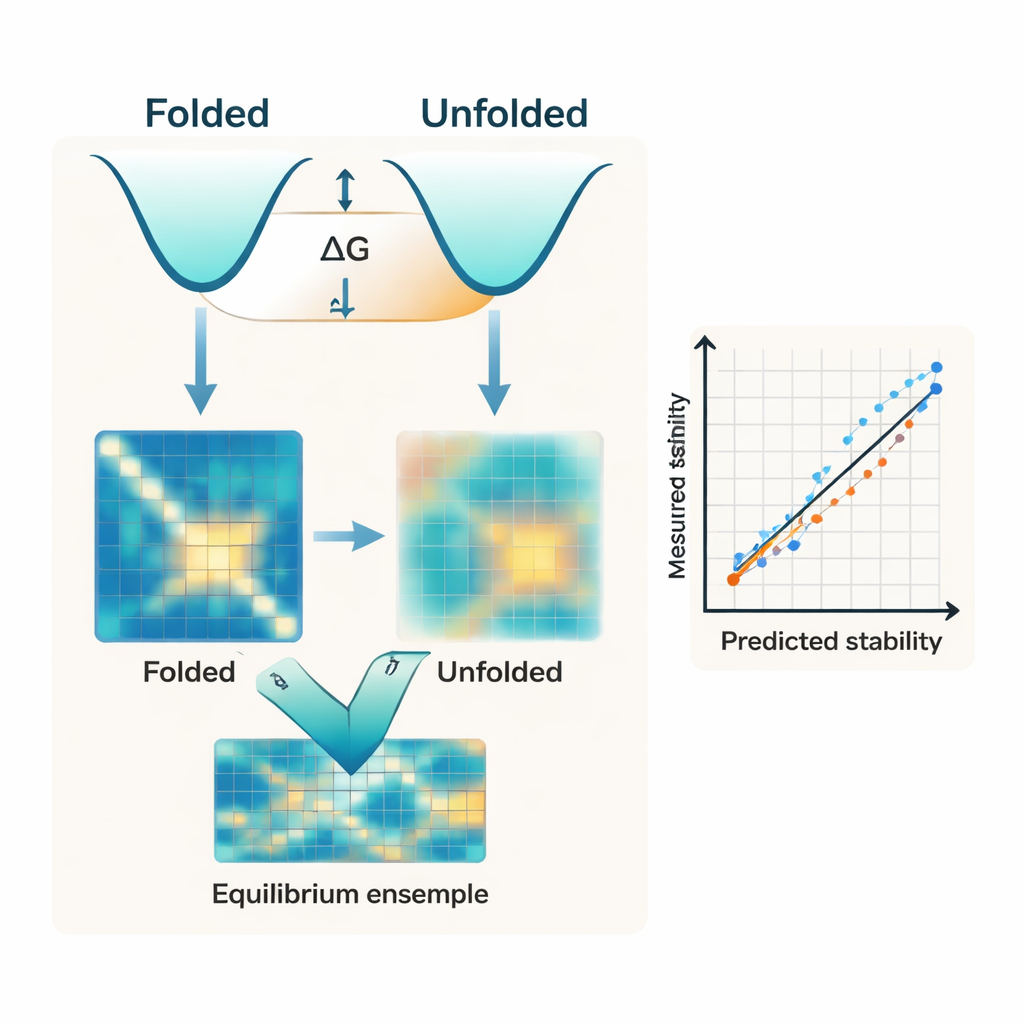
ממלכת העיצוב למבחנים בעולם האמיתי
כדי לבחון האם IFUM יכול להנחות הנדסת חלבונים אמיתית, המחברים מיישמים אותו בשלוש בעיות עיצוב מאתגרות: ייצוב חלבוני אינטרפרון‑למבדא, שינוי צורתו של חלבון איתות חיסוני IL‑10, ושיפור אנזים משנה‑סוכר בשם UGT76G1. בכל שלושת המקרים, היצבויות החזויות על ידי IFUM התאימו היטב לטמפרטורות ההיתוך הנמדדות, המציינות כמה חום חלבון יכול לעמוד בו לפני התפרקותו. המודל גם מסייע בסינון של מאות חלבונים מעוצבים חדשים מחשבונית כדי לבחור את אלה הסבירים להתקפל ולהישאר מסיסים בתוך תאים, תוך שהוא עולה על ניקוד הביטחון הנפוץ מרשתות חיזוי מבנה. תוצאות אלה מרמזות כי ניתן להשתמש ב‑IFUM כ"מסנן יציבות" פרקטי לצד בדיקות מבוססות מבנה בזרימות עבודה מודרניות של עיצוב חלבונים.
מגבלות וכיווני עתיד
כמו כל מודל, ל‑IFUM יש גבולות. הוא מאומן בעיקר על חלבונים קצרים, חד‑שרשיים ומסיסים, והמספרים האבסולוטיים של היציבות שלו נעשים פחות מהימנים עבור חלבונים גדולים בהרבה או כאלו עם לולאות גמישות נרחבות או אזורי חצייה של ממברנה. תיאורו של המצב הבלתי מקופל עדיין מהווה מודל סטטיסטי מפושט במקום תמונה מלאה וריאליסטית של כל הצורות האפשריות. עם זאת, הגישה ממחישה שלימוד בינה מלאכותית להתחשב הן באנסמבל המקופל והן באנסמבל הבלתי מקופל מניב הערכות יציבות מהימנות יותר. עבור לא‑מומחים, המסקנה המרכזית היא ש‑IFUM מקרב אותנו ליכולת לשאול מחשב, בביטחון כמותי, "האם עיצוב חלבון זה אכן יעמוד יחד?", ובכך להאיץ פיתוח של תרופות ביולוגיות בטוחות יותר ואנזימים תעשייתיים חזקים יותר.
ציטוט: Lee, H., Cho, Y., Yun, J. et al. Protein folding stability estimation with explicit consideration of unfolded states. Nat Commun 17, 1883 (2026). https://doi.org/10.1038/s41467-026-68637-4
מילות מפתח: יציבות חלבון, קיפול חלבון, למידה עמוקה, עיצוב חלבונים, מוטציות