Clear Sky Science · he
ננורובוטים מוסווים ממקדים ומווסתים דפוסי תקשורת תת‑תאית במקרופאגים לקידום שיכוך עצבים
מדוע עוזרים זעירים "מוסווים" חשובים לפגיעות בחוט השדרה
פגיעה בחוט השדרה פעמים רבות גוררת שיתוק לכל החיים, כיוון שרקמת העצבים שנפגעה קשה מאוד לשיקום. סיבה מרכזית לכך היא שמקום הפגיעה הופך לאזור עוין מלא בדלקת ולחץ תאיים החוסמים ריפוי. המחקר מתאר סוג חדש של ננורובוט מוסווה שנע באמצעות זרם הדם, חומק ממערכות ההגנה של הגוף, ומתכנת מחדש תאי חיסון באתר הפגיעה — מהמצב התוקפני למצב התיקון — ומסייע לגדילת עצבים בחיות עם נזק לחוט השדרה.
הבעיה: דלקת שלא גובה את עצמה
לאחר פגיעה בחוט השדרה, הגל הראשון של הנזק הוא מהטראומה הפיזית עצמה. אך גל שני ואיטי יותר מונע על‑ידי דלקת, מולקולות רעילות שנקראות רדיקלים חופשיים (ROS), ותמותה תאית נרחבת. תאי חיסון הנקראים מקרופאגים ממהרים לנקות שברי רקמה. בשלבים המוקדמים הם מאמצים מצב תוקפני "M1" שהורג פתוגנים ותאים פגועים אך גם משחרר אותות דלקתיים קיצוניים. כדי שהריפוי האמיתי יתחיל, אותם תאים צריכים בהמשך לעבור למצב מרגיע "M2" התומך בתיקון רקמה, יצירת כלי דם, ושחזור עצבי. לצערנו, הלחץ הקיצוני ברקמה הפגועה יכול לכבל מקרופאגים במצב M1 המזיק, וליצור מעגל של דלקת כרונית המונעת התאוששות פונקציונלית.
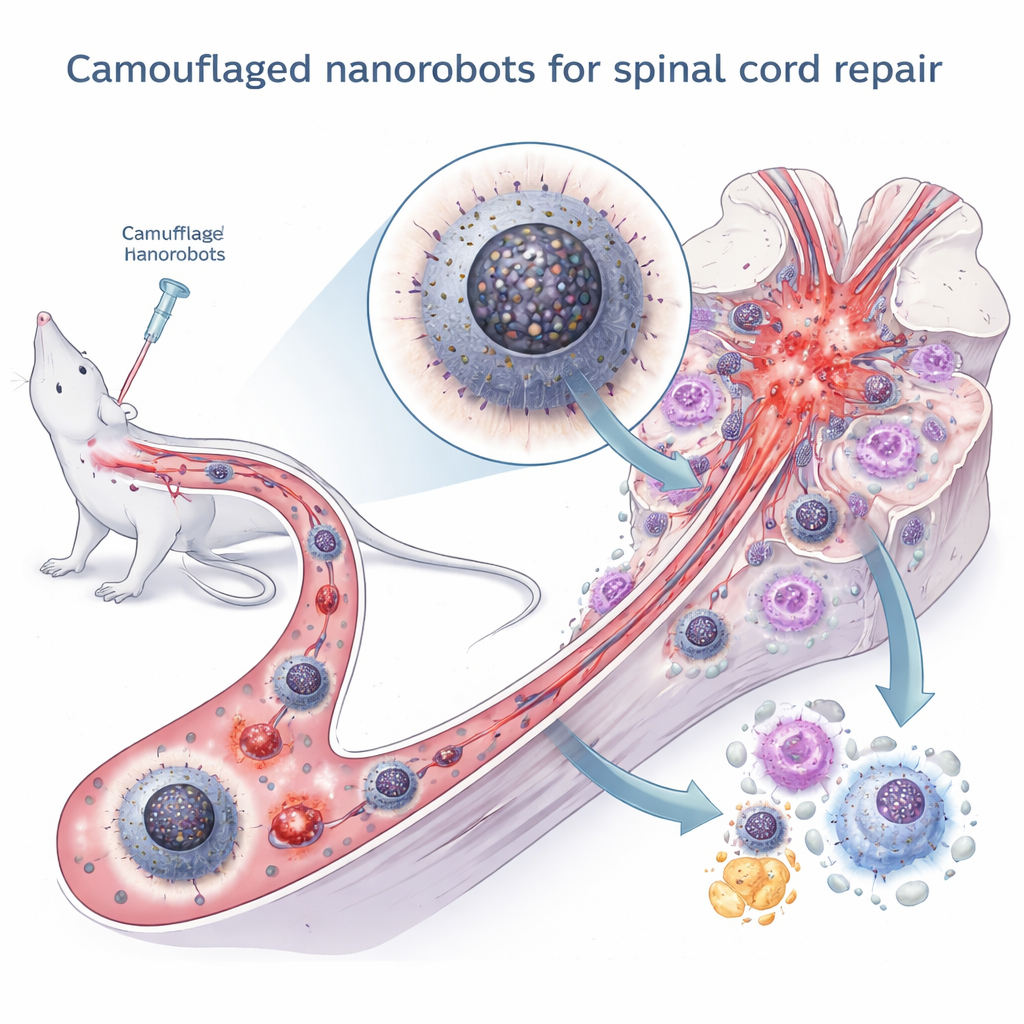
שיחה נסתרת בין רכיבים תוך‑תאיים
המחברים התמקדו ב"שיחה" פנימית עדינה אך קריטית בתוך המקרופאגים: התקשורת בין שני מחסנים מרכזיים — הרשתית האנדופלסמית (המסייעת בקיפול חלבונים ואחסון סידן) והמיטוכונדריה (תחנות האנרגיה של התא). בתנאים נורמליים המבנים הללו מחליפים כמויות קטנות של יוני סידן דרך אזורי מגע מותאמים, ומייחסים כך ייצור אנרגיה לצרכי התא. לאחר הפגיעה, עם זאת, רמות גבוהות של רדיקלים חופשיים גורמות לקיפול חלבונים שגוי ולמתח ברשתית האנדופלסמית. מתח זה דוחף העברה מופרזת של סידן אל המיטוכונדריה, מה שמוביל לקריסת אנרגיה, ליצירת עוד מולקולות רעילות, ולדליפה של DNA מיטוכונדריאלי לנוזל התוך‑תאי. DNA שברח זה מפעיל מסלול אזעקה חזק הנקרא cGAS–STING–NFκB, שמייצב עוד יותר את המקרופאגים במצב הדלקתי M1.
עיצוב ננורובוט מוסווה
כדי לשבור את מעגל ההרס הזה, הצוות בנה ננורובוט רב‑שכבתי בשם BP@D/N. בליבה שלו יש נקודות קוונטיות מפוספיד שחור — חלקיקים זעירים בעלי פעילות אנטי‑חמצונית ואנטי‑דלקתית חזקה אך יציבות נמוכה בגוף. נקודות אלו נארזו במעטפת חלולה מפולידופאמין, חומר ביocompatible שמגן עליהם מפירוק מוקדם ותורם גם הוא תכונות אנטי‑חמצוניות. לבסוף, כל החלקיק עטוף בממברנה שמקורה בנויטרופילים מונעים, סוג של תאי דם לבנים הנמשכים באופן טבעי לאיזורי דלקת. "המסווה" הזה מאפשר לננורובוט להתחמק מהסילוק החיסוני, לעקוב אחרי אותות דלקת אל חוט השדרה הפגוע, ולהיצמד למקרופאגים ללקיחה יעילה.
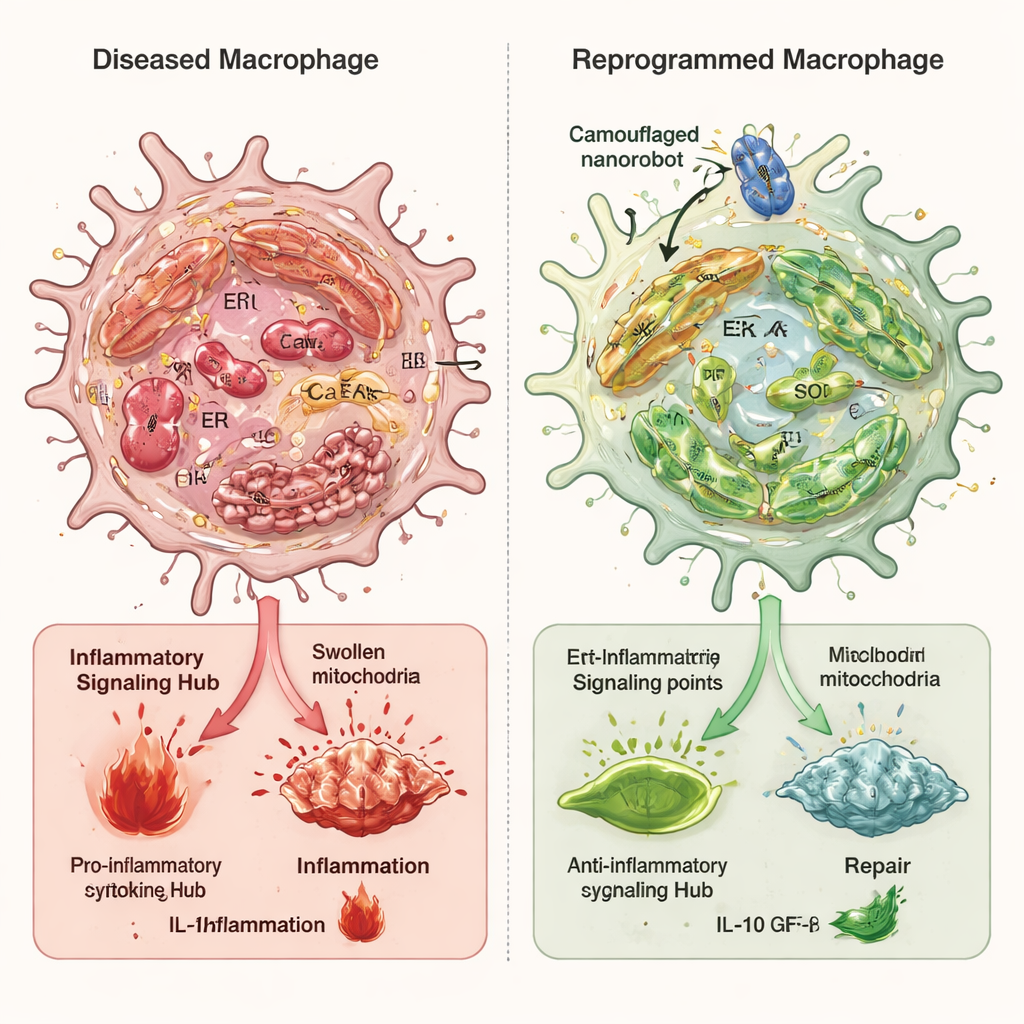
חיבור מחדש של תאי חיסון לחוצים
בעבודות תאיות, מקרופאגים שנחשפו לטריגרים דלקתיים הראו רמות גבוהות של מתח ברשתית האנדופלסמית, מיטוכונדריה נפוח ונהרסת, עודף סידן, והפעלה חזקה של מסלול האזעקה cGAS–STING–NFκB. כאשר טופלו בננורובוטים המוסווים, הלחץ החמצוני הכולל ירד בחדות, הממברנות הפנימיות בין הרשתית האנדופלסמית והמיטוכונדריה נעשו פחות מקושרות יתר, וסידן מיטוכונדריאלי חזר לכיוון הנורמה. זה מנע דליפה של DNA מיטוכונדריאלי לנוזל התוך‑תאי והחליש את מפל הרמזים הדלקתיים. שחקן מרכזי בתהליך זה היה אנזים בשם Ero1α, שעוזר לבקר את הסביבה החמצונית ושחרור הסידן מהרשתית האנדופלסמית. הננורובוטים הקטינו את פעילות Ero1α, וכאשר החוקרים הגבירו באופן מלאכותי את Ero1α, זה ביטל ברובו את היתרונות של הננורובוט, ואישש את תפקידו המרכזי.
מהרגע שמרגיעים דלקת עד לצמיחת עצבים
השינויים הפנימיים האלה הפכו את המקרופאגים ממצב M1 ההרסני למצב M2 המרפא. בתרביות, התאים המוטים ל‑M2 הפרישו פחות מולקולות דלקתיות כמו TNF‑α ו‑IL‑6 ויותר גורמי גדילה המעודדים תאי עצב ותאי תמיכה לצמוח ולהאריך אקסונים. במודלים של חולדות עם פגיעה בחוט השדרה, הזרקות חוזרות של הננורובוטים הובילו לפחות אותות חיסוניים מזיקים בגידול, פחות צלקתיות, היווצרות חללים קטנה יותר, ויותר סיבים עצביים מתחדשים. בעלי החיים שקיבלו את הננורובוטים המוסווים השיגו שיפור בתנועת הגפיים האחוריות, תגובות שריר חזקות יותר, ושיפור במבנה השלפוחית בהשוואה לטיפולים שלא טופלו או לננו‑חלקיקים פחות ממוקדים.
מה זה עשוי משמעותית עבור מטופלים בעתיד
העבודה מציגה כי כיוונון מדויק של המתח הפנימי והתקשורת בין מחסני התא יכול להפוך תאי חיסון מנוגדים למועילים לרקמה העצבתית הפגועה. בעטיפת חלקיקים אנטי‑חמצוניים עוצמתיים אך שבירים בתוך ננורובוט מוסווה וממוקד, החוקרים השיבו איזון בריא יותר בין דלקת לתיקון בחוט השדרה הפגוע של חולדות. למרות שנותר עוד הרבה עבודה לפני שניתן יהיה לבדוק גישה זו בבני אדם, היא מציעה מתווה מבטיח: במקום לדכא דלקת באופן כללי, טיפולים עתידיים עשויים לכוון מכניקה תאית ספציפית בתוך מקרופאגים כדי ליצור סביבה מזמינה יותר לשחזור עצבי לאחר פגיעה בחוט השדרה.
ציטוט: Guo, Q., Wang, W., Jiang, X. et al. Camouflaged nanorobots target and regulate macrophage subcellular organelle crosstalk patterns to promote neural regeneration. Nat Commun 17, 1952 (2026). https://doi.org/10.1038/s41467-026-68636-5
מילות מפתח: פגיעה בחוט השדרה, ננורובוטים, מקרופאגים, שחזור עצבי, ננודראמה