Clear Sky Science · he
אופיינות מטבולית של אינטראקציות בין גידול למערכת החיסון באמצעות אימונופלואורסצנציה מרובת סמנים חושפת מנגנוני מרחב של תגובה לאימונותרפיה בסרטן ריאה שאינו תאי קטלני (NSCLC)
מדוע מחקר זה חשוב
האימונותרפיה שינתה את הטיפול עבור חלק מהחולים עם סרטן ריאה מתקדם, אך מרבית החולים עדיין רואים את הגידול שלהם מתפתח למרות תרופות אלו החזקות. המחקר שואל שאלה פשוטה אך מכרעת: האם אפשר לבחון מקרוב את רקמת הגידול עצמה—לאן התאים פזורים וכמה אנרגיה הם צורכים—כדי לחזות מי יפיק תועלת אמיתית מאימונותרפיה? על ידי הפיכת דגימות ביופסיה זעירות למפות תאיות מפורטות, המחקר שואף לקרב את טיפול בסרטן הריאה לגישה אישית באמת.
מבט פנימי על גידולי ריאה כמו מפה עירונית
הצוות בחן רקמות מ-55 אנשים עם סרטן ריאה שאינו תאי קטלני (NSCLC) במצב מתקדם שטופלו בחסמי נקודות ביקורת חיסוניות, קבוצה מרכזית של תרופות אימונותרפיה. לפני הטיפול, דגימות הגידול צופו בלוח בעל 44 סמנים באמצעות אימונופלואורסצנציה מרובת סמנים, מה שאיפשר לראות חלבונים רבים בו־זמנית. מערכת למידה עמוקה זיהתה אז את סוגי התאים המרכזיים—כמו תאי גידול, תאי T, תאי B, מאקרופאגים ופיברובלסטים—וסיווגה את מצבם התפקודי (למשל, מופעלים, מתחלקים או מותשים) וכן את הפרופיל המטבולי שלהם, כלומר כיצד הם מייצרים ומשתמשים באנרגיה. במקום רק לספור תאים, החוקרים גם מיפו את מיקומי התאים ביחס זה לזה, ויצרו אזורים דמויי שכונות בתוך כל ביופסיה.
גידולים תובעניים באנרגיה וסביבת החיסון שלהם
מוקד מרכזי היה המטבוליזם—האופנים שבהם תאים מייצרים דלק כדי לגדול או להילחם במחלה. החוקרים הגדרו "שכונות מטבוליות" ברמות וסוגים שונים של שימוש באנרגיה, מפעילות נמוכה ועד אזורים מאוד פעילים העשירים בפוספורילציה חמצונית וגליקוליזה. הם גילו כי גם תאי הגידול וגם תאים חיסוניים מסוימים, כגון מאקרופאגים, הראו לעתים קרובות מסלולי ייצור אנרגיה חזקים. חלק מהתבניות הללו נקשרו לתוצאים של מטופלים. למשל, גידולים עם פעילות גבוהה במסלולים שעוזרים להם להשתמש בחומצות אמינו ולהפעיל את מעגל ה-TCA נטו להשתייך למטופלים שחזרו חולה מוקדם לאחר אימונותרפיה. לעומת זאת, חלק מתאי הפלזמה (תאי B המייצרים נוגדנים) עם מסלולים מטבוליים פעילים בתוך הגידול היו שכיחים יותר במטופלים שהיו טובים יותר, מה שמרמז שלא כל התאים בעלי פעילות אנרגטית הם מזיקים—חלקם עשויים לתמוך בחיסון אנטי-גידולי יעיל.
שחקני חיסון טובים ורעים בנוף הגידול
מעבר לשפע הפשוט, סוג ותפקוד תאי החיסון היו גם הם חשובים. מאקרופאגים שנשאו את המולקולה הציטוטוקסית גרנזים B נקשרו חזק להישרדות חופשית מהתקדמות גרועה יותר, במיוחד כאשר נמצאו בשכונות מטבוליות נמוכות או לא פעילות. אזורים אלו עשויים לייצג אזורים דלים בחזון או כבויים שבהם המתקפה החיסונית מוחלשת. לעומת זאת, סידורים מסוימים של תאי T רגולטוריים (Tregs) ופיברובלסטים בגבול שבין הגידול לרקמה הסובבת נראו קשורים לתוצאים טובים יותר, אולי משקפים דפוס שבו תאים מדכאים מוחזקים בקצוות ולא חודרים עמוק לתוך הגידול. יחסים בין סוגי תאים חיסוניים שונים, כגון גרנולוציטים לעומת תאי CD8, גם הם עקבו אחרי התגובה, והדגישו שמאזן המערכת החיסונית והמיקום שלה חשובים, לא רק מספרי התאים הכוללים.
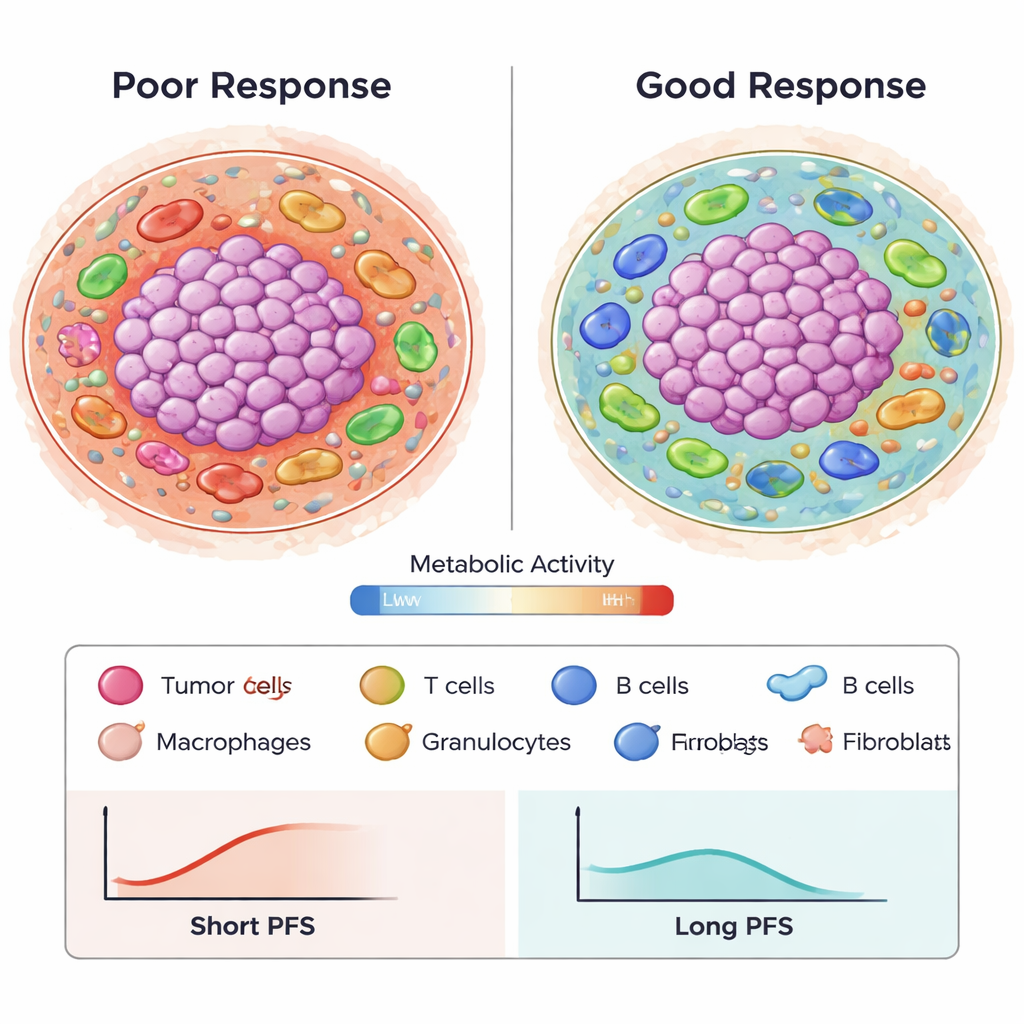
ממתמונות מורכבות לתבניות מנבאות
כדי לפענח יותר ממיליון תכונות מרחביות מהונדסות שמתארות סוגי תאים, מרחקים ומצבים מטבוליים, המחברים השתמשו בשיטת בחירת תכונות מתקדמת (Stabl) וכלי מודלינג להישרדות. הם זיהו 87 תכונות מפתח, רבות מהן משקפות כיצד תאים מטבולית פעילים של הגידול מתקשרים עם מאקרופאגים ותאי T, או כיצד סוגים ספציפיים של תאים חיסוניים מתקשחים ליד כלי דם ופיברובלסטים. באמצעות תכונות אלה במודלים של רגרסיית קוקס, הם בנו מנבא שאמד הישרדות חופשית מהתקדמות עם דיוק (AUC) סביב 0.8 לתקופה של 24 חודשים, תוך שיפור על פני סמנים בודדים מסורתיים כגון צביעת PD-L1 או עומס המוטציות בגידול בעבודות שפורסמו קודמות. חשוב לציין כי מספר תכונות היו לשחזור בשתי קבוצות מטופלים בלתי תלויות, מה שמרמז שהתבניות אינן סתם רעש אקראי.
מה זה אומר עבור המטופלים
לאדם מן השורה, המסר הוא שמקום הישיבתם של התאים בגידול ריאה וכיצד הם מזינים את עצמם עשויים לעזור להסביר מדוע חלק מהמטופלים מגיבים היטב לאימונותרפיה בעוד שאחרים לא. המחקר מראה כי מידע מרחבי ומטבולי עשיר מדגימת ביופסיה שגרתית, בשילוב בינה מלאכותית ומידול סטטיסטי, יכול לחשוף חתימות של סיכוי לתועלת או לעמידות. למרות שהעבודה זקוקה לאימות בקבוצות גדולות יותר ובחתכים של רקמות שלמות, היא מתווה דרך לעבר בדיקות עתידיות שעשויות להגיד לרופאים, לפני תחילת הטיפול, אילו מטופלים צפויים לקבל שליטה יציבה מאימונותרפיה ואילו עלולים להזדקק לאסטרטגיות חלופיות או משולבות.
ציטוט: Monkman, J., Kilgallon, A., Lawler, C. et al. Metabolic characterization of tumor-immune interactions by multiplexed immunofluorescence reveals spatial mechanisms of immunotherapy response in non-small cell lung carcinoma (NSCLC). Nat Commun 17, 837 (2026). https://doi.org/10.1038/s41467-026-68633-8
מילות מפתח: עמידות לאימונותרפיה, סרטן ריאה שאינו תאי קטלני, מיקרו-סביבת הגידול, ביולוגיה מרחבית, מטבוליזם של סרטן