Clear Sky Science · he
H3K9me2 בתיווך G9a מנחה שיקום אפיתל מעי דרך השתקה אפיגנטית של גנים הקשורים למחזור התא
מדוע היכולת של המעי לתקן את עצמו חשובה
כל יום, ציפוי המעי נחשף לתנאים קשים: חומצת הקיבה, חלקיקי מזון ולטריליונים של מיקרובים. ועדיין רקמה זו לא רק שורדת — היא מתחדשת כל הזמן. כאשר מערכת התיקון הזו נכשלת — אחרי הקרנות, במחלת מעי דלקתית או בזיהומים קשים — אנשים עלולים לסבול מכאבים, דימומים וסיבוכים מסכני חיים. המחקר הזה חושף "מפסיק" חבוי בתוך תאי המעי שעוזר להם להחליט מתי מפסיקים במנוחה ומתי מתחילים לבנות מחדש, ומציע רמזים לטיפולים חדשים שיכולים לחזק את צוות התיקון הטבעי של המעי.
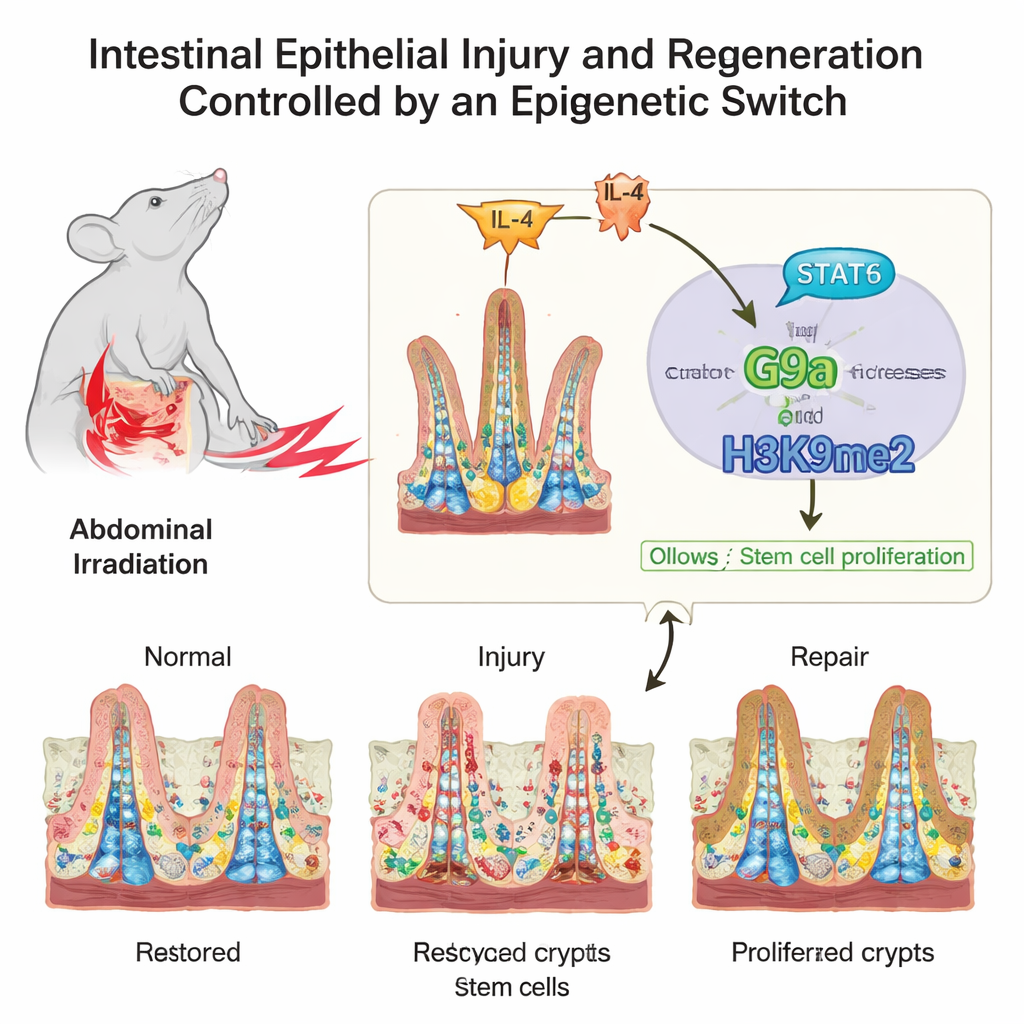
ארכיטקטורה עדינה תחת עומס מתמיד
המשטח הפנימי של המעי נראה מתחת למיקרוסקופ כמו שטיח פרווה, עם בליטות דמויות אצבעות (ויולים) הסופגות חומרים ומעגלים המכונים קריפטים שבהם חיים תאי גזע. תאי גזע אלה וצאצאיהם המתרבים במהירות חייבים למצוא איזון בין חידוש שוטף לתיקון חירום. המחברים התמקדו באופן שבו תגים כימיים על חלבוני עיטוף ה‑DNA, הנקראים היסטונים, משפיעים על איזון זה. תגיות אלה אינן משנות את הגנים עצמם, אלא פועלות יותר כמו כפתורי עמעום, שמגבירים או מדליקים אשכולות של גנים כאשר המעי עובר ממצב רגיל לפציעה וחזרה לבריאות.
סמן אפיגנטי שעוקב אחרי נזק והחלמה
באמצעות עכברים שנחשפו לקרינה — גורם נפוץ לפגיעה במעי בזמן טיפולי סרטן — החוקרים סרקו סימני היסטון רבים בקריפטים העשירים בתאי גזע. סימן אחד, הידוע כ‑H3K9me2, עלה בחדות כאשר המעי עבר מפציעה לתהליכי תיקון. אנזים הכותב שלו, חלבון בשם G9a, הראה דפוס דומה. הצוות בחן גם דגימות אנושיות ממטופלים שקיבלו הקרנות אזור האגן, וכן אנשים עם מחלת קרוהן. בשני המקרים, רמות גבוהות יותר של H3K9me2 ו‑G9a בתאי המעי הלכו יד ביד עם סימנים משופרים של שיקום רקמה, מה שמרמז שהמערכת זו שמורה בין עכברים לבני אדם.
כשהמפסיק של התיקון נשבר
כדי לבדוק האם סימן זה הוא רק צופה או שהוא באמת מניע ריפוי, המדענים הסירו את G9a באופן ספציפי מרירית המעי של עכברים, או חסמו את פעילותו בעזרת תרופה. בשני המקרים ירדו רמות ה‑H3K9me2. לאחר קרינה או פגיעה כימית, עכברים אלה איבדו יותר משקל, המעי שלהם היה קצר ויותר פגוע, והם הראו פחות קריפטים מתחדשים ותאי גזע מאשר בעלי חיים תקינים. גם ללא פגיעה מכוונת, רירית המעי של עכברי חסרי G9a נראתה מוגבלת: הקריפטים היו רדודים יותר, הוילי קצרים יותר, ומספרי תאי הגזע וצאצאיהם המומחים ירדו. "מיני־מעיים" זעירים שגודלו מתאים אלה במעבדה גם הם פיתחו גרוע, מה שממחיש שמערכת מולקולרית זו מרכזית לחידוש היומיומי של המעי.
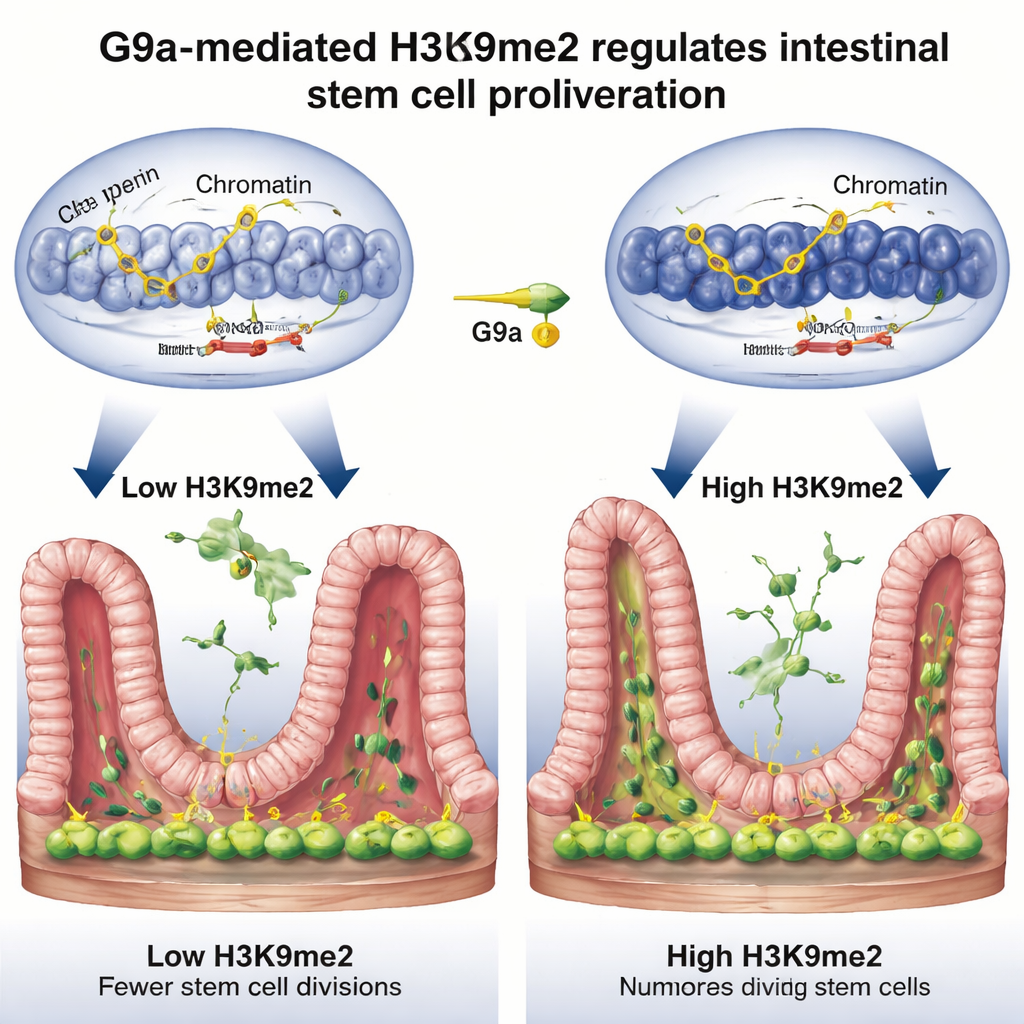
שחרור הבלמים על חלוקת התאים
בהעמקה, הצוות חקר אילו גנים נשלטים על ידי מפסיק התיקון הזה. על ידי שילוב של שלוש שיטות רחבות‑היקף של הגנום, הם מצאו ש‑H3K9me2, שמונח על ידי G9a, נוטה לשבת על מקטעי DNA שלרוב פועלים כבלמים על מחזור התא — גנים כמו Rb1cc1, Rb1, Cdkn1a ו‑Pten, שמאטו או עוצרים חלוקת תאים. כאשר G9a נעדר, הסמן הכימי נעלם מאזורים אלה, ה‑DNA הסובב התפתח, וגני הבלימה הופעלו בחוזקה רבה יותר, מה שהוביל להאטה בהתרבות תאי הגזע. במהלך תיקון נורמלי אחרי פגיעה, רמות H3K9me2 באותם גנים עלו, פעילותם ירדה, ותאי הגזע היו חופשיים יותר להתחלק ולשקם את הציפוי. במהות, G9a ו‑H3K9me2 השתקו זמנית את אותות ה"עצור" כדי לאפשר לרקמה לשגשג מחדש.
שרשרת איתות ממחוות חיסוניות אל התיקון
המעי אינו פועל לבד; הוא מאזין כל הזמן לאותות מהמערכת החיסונית. החוקרים עקבו אחרי אחד האותות הללו שממוקם מעל G9a בשרשרת הבקרה. לאחר פגיעה, רמות השליח החיסוני IL‑4 עלו, והפעילו חלבון שנקרא STAT6 בתוך תאי המעי. STAT6 הפעיל נקשר ישירות לאזור הבקרה של גן G9a והגביר את ייצורו. כך נוצרה שרשרת פיקוד: IL‑4 מפעיל את STAT6, STAT6 מעלה את G9a, ו‑G9a מוסיף H3K9me2 כדי לשתק גנים-בלמים של מחזור התא, מה שמאפשר לתאי הגזע להתרבות ולשחזר את הרירית הפגועה.
מה המשמעות של זה לטיפולים עתידיים
עבור לא‑מומחה, הממצאים הללו מראים ששיקום המעי מונחה לא רק על ידי גנים, אלא על ידי סימנים כימיים הפיכים שמדייקים מתי משתמשים בגנים אלה. מסלול IL‑4–STAT6–G9a–H3K9me2 מתנהג כמו לוח בקרה פנימי שמרפה את הבלמים על חלוקת תאי הגזע זמן קצר מספיק כדי לרפא, ואז ניתן לאפס אותו. בעתיד, טיפולים שמחמירים בעדינות מסלול זה — כגון תרופות או כלים גנטיים שמעלים את רמות G9a בזמן ובמיקום הנכונים — עשויים לעזור למטופלים להחלים מהר יותר מפגיעות קרינה, התלקחויות של מחלת מעי דלקתית או מצבים אחרים שפוגעים ברירית המעי, ובאותו זמן למזער את הסיכונים של גדילה בלתי נשלטת של תאים.
ציטוט: Chen, J., Shi, X., Zhou, X. et al. G9a-mediated H3K9me2 orchestrates intestinal epithelial regeneration through epigenetic silencing of cell cycle-related genes. Nat Commun 17, 1874 (2026). https://doi.org/10.1038/s41467-026-68626-7
מילות מפתח: שיקום מעי, אפיגנטיקה, תאי גזע, מתילציה של היסטונים, מחלת מעי דלקתית