Clear Sky Science · he
חותם דינמי של פשרה בין פעילות ליציבות באבולוציית לקטמזות
מדוע זה חשוב עבור עמידות לאנטיביוטיקה
עמידות לאנטיביוטיקה נראית לעתים כמו קופסה שחורה: החיידקים "במובן מה" משתנים והתרופות מפסיקות לעבוד. המחקר הזה פותח את הקופסה עבור אחד האנזימים המפורסמים ביותר לעמידות, TEM‑1 β‑lactamase, שעוזר לחיידקים לפרק אנטיביוטיקות דמויות פניצילין. בעזרת מעקב אחרי האופן בו צורתו ותנועותיו של האנזים משתנות כאשר הוא מתפתח כדי להתאים לתרופות חדשות, המחברים חושפים מדוע מוטציות שמגבירות פעילות לעתים קרובות מחלישות את היציבות, ואיך האבולוציה מוצאת דרכים חכמות לאזן בין השניים.
מַלחֵם פניצילין לשובר תרופות רחב
TEM‑1 במקור מצטיין בפרוק אנטיביוטיקות פניצילין ישנות אך חלש בהתמודדות עם תרופות חדשות ומהודקות יותר כמו cefotaxime. במגוון שורות קליניות, מוטציה מרכזית יחידה בשם G238S מופיעה קרוב לאתר הפעיל של האנזים, הכיס שבו נחתכות האנטיביוטיקות. מוטציה זו משפרת משמעותית את יכולת האנזים להחריב את ה‑cefotaxime, בעוד שהיא פוגעת רק באופן מתון בתפקודו המקורי לפרוק פניצילין. המחברים מראים ש‑G238S אינה פשוטה מרחיבה את הכיס; היא מארגנת מחדש את האופן שבו מספר לופים והליקסים סביב הכיס נעים, ויוצרת קונפורמציה פונקציונלית חדשה שמתאימה טוב יותר לתרופות גדולות.
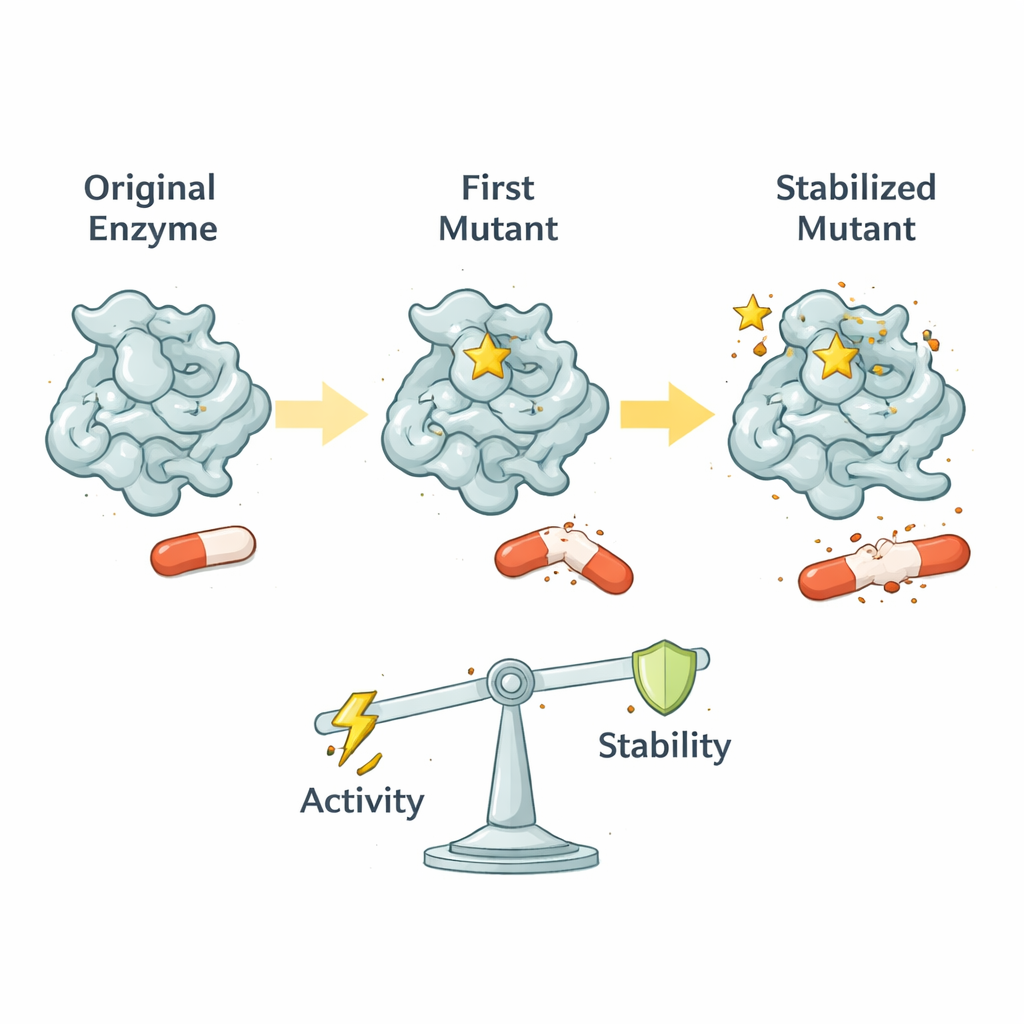
תנועת חלבון ככפתור כיוונון אבולוציוני
בהסתמך על טכניקות מתקדמות של תהודה מגנטית גרעינית (NMR), החוקרים מדדו איך חלקים שונים של TEM‑1 נעים על פני סקאלות זמן הנעות מטריליוניות עד אלפיות השנייה. ה‑wild‑type של TEM‑1 די קשיח, מה שעוזר לו לעבד ביעילות את המצע המקורי שלו. G238S משמר את רוב הקשיחות המהירה הזו אך מציבה תנועות איטיות יותר ומכוונות בקפידה בקירות רבות של אתר הפעיל. תנועות אלו מהירות דיו כדי להתאים לכימיה של האנזים אך לא כל כך פרועות כדי לשבש שיירים קטליטיים קריטיים. התוצאה היא "חלון" מובנה של גמישות אופטימלית: תנועה מספקת כדי לפתוח את הכיס ל‑cefotaxime, תוך שמירה על יישור נכון של המכונה הכימית המרכזית.
לא לבחור צורה אחת אלא לאזן בין שתי צורות
האבולוציה אינה מקפיאה את TEM‑1 לצורה חדשה יחידה. במקום זאת, האנזים מדגמן לפחות שתי קונפורמציות עיקריות: מצב "פניצילינאז" הדומה למבנה המקורי ומצב פתוח יותר "צפוטקסימאז" המתאים יותר לתרופות חדשות. מוטציות נוספות שמופיעות מאוחר יותר, כמו E104K ו‑A42G, עושות מעשה דק: במקום פשוט לייצב את הצורה החדשה הידידותית ל‑cefotaximase, הן מאזנות מחדש את התערובת של שני המצבים. נתוני NMR מראים שחלקים שונים של אתר הפעיל ושל השלד התומך יכולים לשנות את האוכלוסיות שלהם באופן עצמאי לאורך רצף שתי־המצבים הזה. זה מוביל למערך קומבינטורי של וריאנטים של האנזים, כל אחד עם תמהיל שונה של קונפורציות דמויות פניצילין ודמויות דמויות cefotaxime, ולכן לפרופילים קטליטיים שונים.
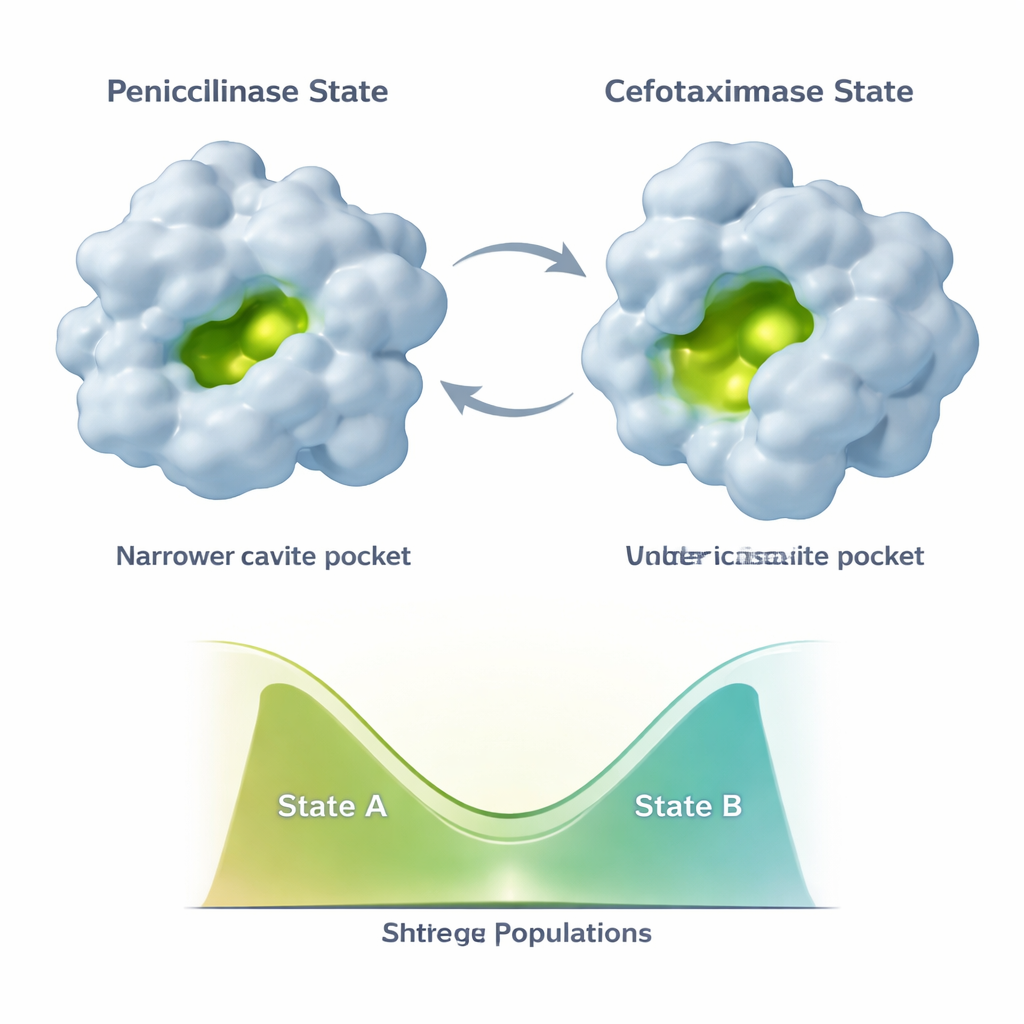
נקודות תורפה נסתרות ותיקונים מרחוק
מוטציות המשפרות פעילות נושאות לעתים עלות נסתרת: הן מחלישות את החלבון. במקום לבחון רק התפרקות מלאה, הצוות מיפוי יציבות מקומית ברמת מקטעים קצרים באמצעות החלפת מימן–דויטריום ושימוש בספקטרומטריית מסה. נמצא ש‑G238S מייצרת חוסר יציבות לא רק בלופים הקרובים אלא גם בהליקסים ומקטעי בטא מרוחקים שמרכיבים את השלד המבני. חלק מאיזורים אלו חופפים לכיס אלוסטרי "קריפטי" — פתיחה לא מנוצלת לעתים במרכז החלבון שיכולה לקשור מולקולות קטנות ולהחליש פעילות. G238S מקלה על פתיחת כיס זה, ובמהלך כך בונה תכונה של מעין עכבה עצמית חלשה לתוך האנזים. מוטציות מאוחרות יותר, במיוחד A42G, מחזקות את רשת השלד המוחלשת הזו, משפרות יציבות מקומית סביב שלושה הליקסים המשולבים מבלי להסיר את הדינמיקה המועילה של אתר הפעיל. במילים אחרות, האבולוציה טלאת נקודות תורפה מבניות מרוחקות במקום לבטל את החידוש המקורי.
מה המחקר חושף על אסטרטגיית האבולוציה
לקורא שאינו מומחה, המסר המרכזי הוא שחלבונים כמו TEM‑1 אינם מפתחים עמידות על‑ידי הדלקה או כיבוי פשוטים. כל מוטציה מעצבת במידת מה את האופן שבו האנזים נושם, מתכופף ומחלק את זמנו בין תנוחות עבודה שונות. G238S פותחת דלת לתפקיד חדש — לפרק אנטיביוטיקות חדשות — אך גם יוצרת פגיעויות מקומיות ומצב חלקית של עכבה עצמית. מוטציות משניות פועלות כהעמקות זהירות, מייצבות את השלד ומכוונות את האיזון בין הקונפורציות הישנות והחדשות כדי שהאנזים יוכל להישאר גם פעיל וגם עמיד. נקודת מבט דינמית זו של האבולוציה, שבה תנועות וחולשות מקומיות שוות חשיבות למבנה הסטטי, יכולה לסייע בעיצוב אנטיביוטיקות עתידיות ותרופות המכוונות לאנזימים שיהיה קשה יותר לחיידקים לעקוף.
ציטוט: Arcia, E., Keramisanou, D., Jacobs, L.M.C. et al. Dynamic signature of activity-stability tradeoff in lactamase evolution. Nat Commun 17, 1884 (2026). https://doi.org/10.1038/s41467-026-68620-z
מילות מפתח: עמידות לאנטיביוטיקה, בטא-לקטמז, אבולוציה של חלבונים, דינמיקת אנזימים, יציבות חלבון