Clear Sky Science · he
הרחבת טווח המטען בקונפוּגָטים של נוגדן–תרופה באמצעות העברת תרופות המכילות קבוצת הידרוקסיל דרך פוספוראמידטים המתמוטטים בעצמם
טילים חכמים יותר נגד סרטן
תרופות נגד סרטן יכולות להיות חזקות מאוד, אך לעתים פועלות כמו פצצה מקיר לקיר: הן פוגעות ברקמות בריאות כמעט באותה עצמה שבה הן פוגעות בגידולים. קונפוּגָטים של נוגדן–תרופה (ADCs) נוצרו כדי לפתור בעיה זו על ידי חיבור של תרופה עוצמתית לנוגדן שמזהה תאי סרטן, והופך את הטיפול לטיל מונחה. מאמר זה מסביר חיבור כימי חדש בין הנוגדן לתרופה שעושה את הטילים הללו גם מדויקים יותר וגם גמישים יותר, ופותח את הדלת לסוגי תרופות לסרטן רבים יותר מאלה ש-ADCs כיום יכולים לשאת.
מדוע התרופות הממוקדות של היום עדיין מוגבלות
ADCs מורכבים משלושה חלקים: נוגדן שמזהה סימן על תאי סרטן, תרופה רעילה ("מטען"), וקשר כימי שמחבר ביניהם. מרבית ה-ADCs המאושרים מסתמכים רק על מספר מצומצם של מטענים שפוגעים ב-DNA או חוסמים חלוקת תאים בדרכים דומות. סיבה מרכזית לכך היא הקישור: עליו להחזיק את התרופה בחוזקה בזמן שה-ADC נמצא במחזור הדם, ואז לשחררה נקייה כשהוא בתוך תא הגידול. קישורים קיימים פועלים היטב רק עם קבוצות כימיות מסוימות על התרופות, במיוחד אמינים, ולעתים מתקשים עם התרופות רבות המכילות קבוצות אלכוהול (–OH). זה משאיר כמות גדולה של סוכנים מבטיחים על המדף, כיוון שלא ניתן להעבירם בבטחה או ביעילות באמצעות עיצובי ADC קיימים.
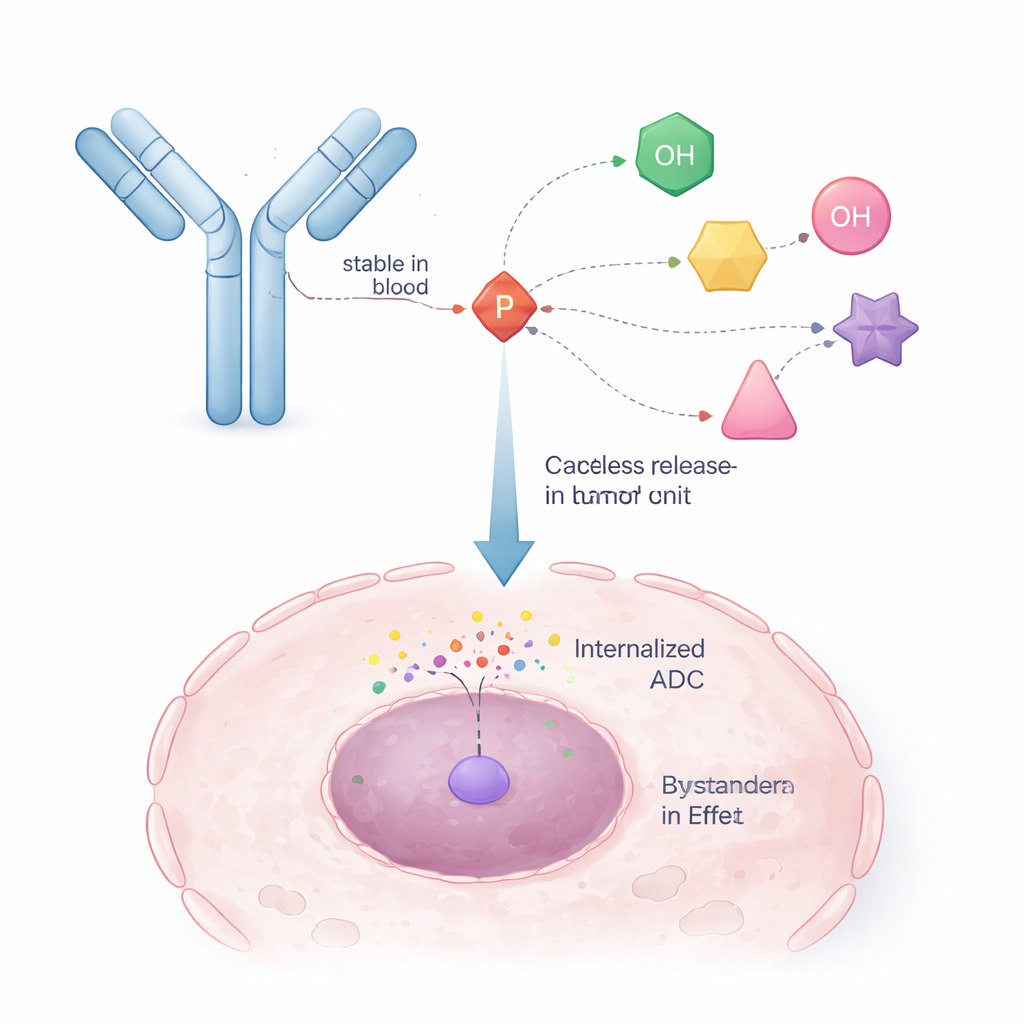
הלוואת רעיון מטבליות אנטי־ויראליות
החוקרים פנו לאסטרטגיה שכבר הוכחה בתרופות אנטי־ויראליות, הנקראת ProTides. בתרופות אלה, יחידה כימית מבוססת זרחן מסתירה זמנית את קבוצת הזרחן המטעינה של התרופה כך שתוכל לחדור לתאים, ואז מתפרקת בתוך התא ומשחררת את הצורה הפעילה. המחברים תכננו מחדש את הרעיון כך שזרוע אחת של ליבת הזרחן משמשת לחיבור לנוגדן, בעוד הזרועות האחרות מחזיקות את תרופת הסרטן. כך נוצר "קישור המתמוטט עצמי": ברגע שמפעיל פנימי (כמו אנזים בתא גידול) חותך חלק קטן מהמבנה, יחידת הזרחן קורסת בצורה מבוקרת ומשחררת את מולקולת התרופה המקורית כשהקבוצת האלכוהול שלה משוחזרת וללא שינוי.
בניית חיבור כימי רב־תכליתי
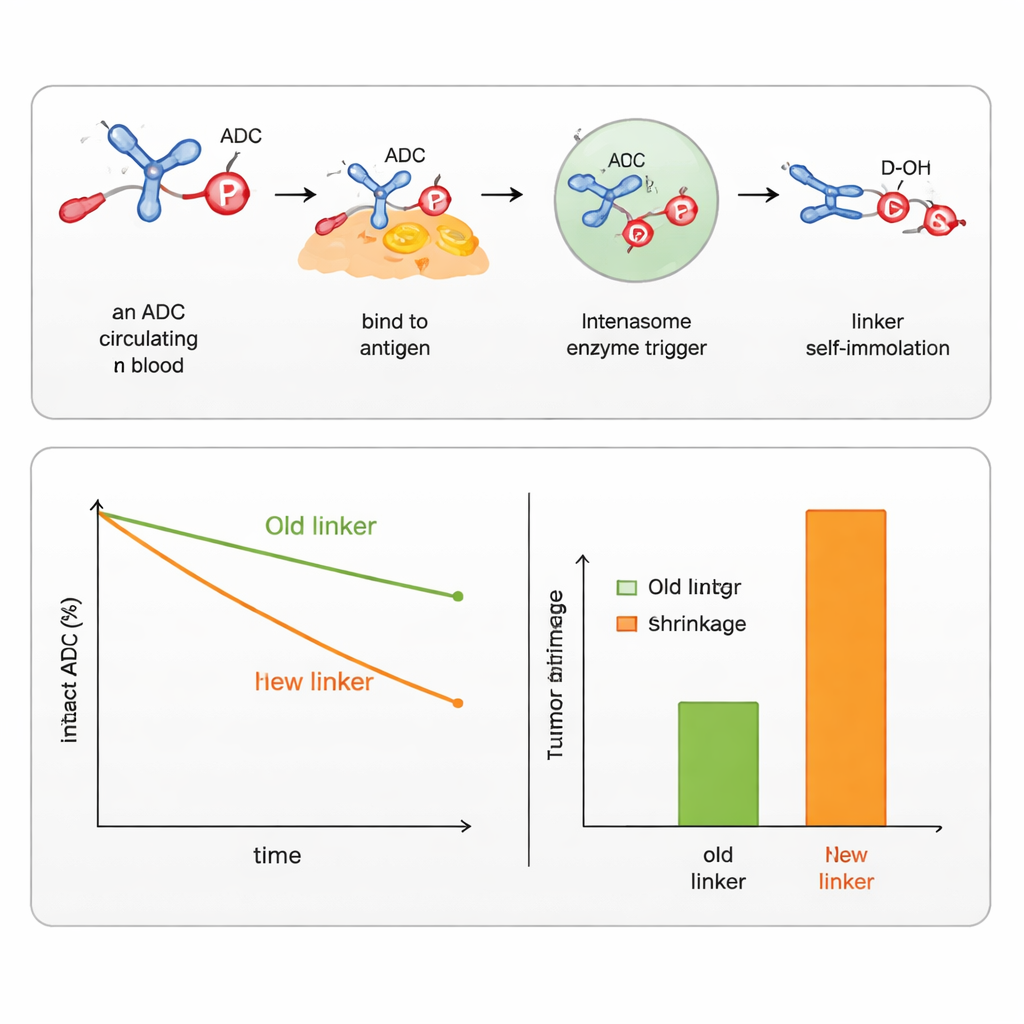
הצוות הוכיח שבעזרת כיוונון הקבוצות סביב אטום הזרחן הם יכולים לכוונן עד כמה הקישור יציב בדם וכמה מהר הוא יתפרק בתוך התאים. הם תכננו גרסאות שתגענה למספר סוגי טריגרים נפוצים בתאי סרטן, כולל אסטרזות ופרוטאזות (אנזימים החותכים קשרים ספציפיים), וגם אנזימים שמכירים קבוצות סוכר או תנאים מחמצנים/מוליכים באברוני התא. באמצעות עיצובים אלה הם הצליחו לחבר ולשחרר גם אלכוהולים ארומטיים (כמו הכימותרפיה SN38) וגם אלכוהולים אליפטיים (כמו DXd, המטען ב-ADC מאושר לסרטן השד). בהשוואה ישירה עם קישורים מסחריים קיימים ל-SN38 ול-DXd, קישורי הפוספוראמידט החדשים שמרו על התרופות קשורות זמן רב יותר בסרום, מסרו יותר תרופה לגידולים, וייצרו כיווץ חזק יותר של הגידול במודלים עכבריים, בעוד שהשפעתן על תאים בריאים הייתה חלשה יותר.
פתיחת דלת לריבוי מטעני תרופות לסרטן
כדי לבדוק עד כמה הקישור שימושי באופן רחב, החוקרים הרכיבו ADCs שנושאים עשר תרופות שונות שכולן כוללות לפחות קבוצת –OH אחת אך פועלות בדרכים שונות בתוך תאי סרטן. אלו כללו מעכבים של סינתזת DNA, קיפול חלבונים (HSP90), מטבוליזם אנרגטי (NAMPT ו-DHODH), והתרגום של חלבונים, וכן סוכנים ידועים כמו פאצטקסל וגמציטאבין. למרות טווח המבנים הרחב, הצליחו ליצור ADCs הומוגניים עם רמת טעינת תרופה גבוהה עבור כולם. במחקרים בסריגי תאים במגוון סוגי סרטן, רוב ה-ADCs הללו הראו עוצמה בננומולרי או תת־ננומולרי ובחירה ברורה לתאים שהביעו את מטרה הנוגדן, מה שאישר שהקישור יכול לשחרר באופן עקבי תרופה פעילה בתוך התאים הנכונים.
גמציטאבין כדוגמה מרכזית
גמציטאבין היא כימותרפיה נפוצה, אך בצורתה המקובלת היא מופרשת מהגוף במהירות כך שעל החולים לקבל מינונים גדולים וחוזרים, מה שמגביל את הכמות שניתן להעניק בבטחה. באמצעות קישור הפוספוראמידט המחברים ציוונו את הגמציטאבין לנוגדן הפונה ל-HER2 באחד משני עמדות אלכוהול, והראו ששתי הגרסאות שבמרגע שהן בתוך תאי סרטן משחזירות פעילות מלאה. במודלים עכבריים של גידולי HER2-חיוביים, מנה יחידה של ADC הגמציטאבין — שכללה כמות כוללת של גמציטאבין בערך אלף פעמים פחות מהפרוטוקולים המקובלים של תרופה חופשית — גרמה לשליטה חזקה וסלקטיבית בגידול. התנהגות ה-ADC במחזור הדם התאמה במידה רבה לזו של הנוגדן החשוף, ומנות גבוהות היו נסבלות היטב בחולדות, מה שמעיד על מרווח בטיחות רחב.
מה משמעות הדבר לטיפולי סרטן בעתיד
עבור הקהל הרחב, המסר המרכזי הוא שעבודה זו מספקת מחבר כימי חדש וגמיש מאוד שמאפשר לנוגדנים לשאת מגוון רחב יותר של תרופות לסרטן מאשר קודם — ובאופן בטוח יותר. על ידי הבטחת כך שהתרופות יישארו מחוברות בזמן ההסתובבות בדם וישתחררו רק לאחר שה-ADC נלכד בתוך תא סרטן, קישורי הפוספוראמידט משפרים את כמות התרופה שמגיעה לגידול ומצמצמים נזק לרקמות בריאות. לא פחות חשוב, הם מאפשרים שימוש חוזר בתרופות מולקולריות קטנות ועוצמתיות שכבר קיימות — בעלות צורות ומנגנונים שונים — כטיפולים ממוקדים. הדבר יכול להרחיב משמעותית את התפריט של ADCs הזמינים לחולים ולעזור להתמודד עם גידולים שהתפתחו לעמידות מול ערכת המטענים המוגבלת של היום.
ציטוט: Ochtrop, P., Jagtap, A.P., Felber, J.G. et al. Expanding the payload scope in antibody-drug conjugates by delivery of hydroxy-containing drugs through self-immolative phosphoramidates. Nat Commun 17, 759 (2026). https://doi.org/10.1038/s41467-026-68605-y
מילות מפתח: קונפוּגָטים של נוגדן–תרופה, העברת תרופות לסרטן, קישורים המתמוטטים עצמם, כימיית פוספוראמידט, כימותרפיה ממוקדת