Clear Sky Science · he
קיאנציה ריגיודיברסנטית ובחירתית אננטיומטרית של קשרי C–H באמינים שניוניים נשלטת על‑ידי ליגנד
למה שינוי של קשרים זעירים חשוב לתרופות גדולות
תרופות נפוצות רבות מכילות מבנים זעירים המבוססים על חנקן הנקראים אמינים. שינויים עדינים באופן הקישור של האטומים סביב אמינים אלו יכולים להפוך תרופה חלשה לטיפול חזק ומדויק — או להפוך אותה ללא פעילה או אפילו מזיקה. המאמר הזה מתאר שיטה חדשה לשינוי מבני אמינים אלה לפי הרצון, המאפשרת לכימאים לבחור בדיוק באיזה מקום במולקולה לבצע את התגובה ואיזו צורה מראה (אננטיומר) לייצר — שתי נקודות קריטיות בעיצוב תרופות בטוחות ויעילות יותר.
בחירת מיקום אחד במולקולה צפופה
אמינים בתרופות לעתים קרובות נושאים מספר קשרי פחמן–מימן (C–H) דומים מאוד שהתנהגותם בדרך כלל כמעט זהה. הכימאים היו שמחים להחליף רק אחד מאותם מימנים בקבוצה תפקודית שימושית, כגון קבוצת “ציאנו” (–CN), מבלי להפריע לשאר המולקולה. זה קשה מכיוון שתגובות סטנדרטיות נוטות לפעול באתר הפעיל ביותר שמכתיבה מבנה המולקולה, לא לפי בחירת הכימאי. כאן, המחברים עובדים עם אמינים שניוניים פשוטים וגמישים הנושאים שני שרשרות פחמן שונות על החנקן. הם מראים שבעת התחלה מאותו אמין ניתן לכוון את התגובה לאחד משני מיקומים שכנים — או בסמוך ליחידת N‑מנטיל הקטנה (האתר שמכונה α′) או פחמן אחד נוסף בהמשך בשרשרת השנייה (אתר ה‑β) — פשוט על‑ידי החלפת הליגנד המקיף את קטליזטור הנחושת.
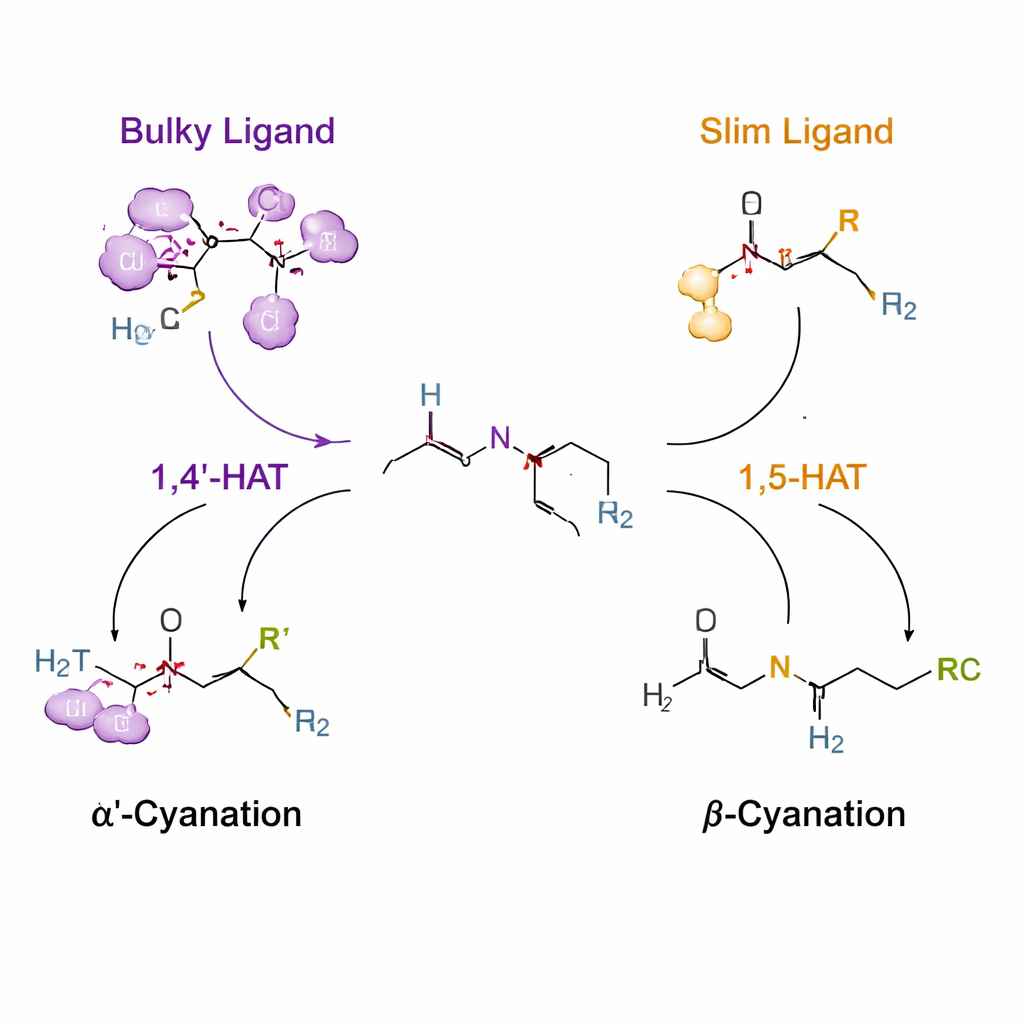
שימוש "בקפיצות" מימן מבוקרות להנחיית הפעילות
הטריק המרכזי נשען על תהליך הקרוי העברת אטום מימן (hydrogen atom transfer), שם רדיקל קצר‑מועד הממוקד בחנקן מותח מימן מפחמן סמוך. בעקרון, רדיקלים כאלה מעדיפים מרחק מסוים, לטובת טווח של שישה אטומים הידוע כ‑1,5‑HAT. המחברים מחברים לאמין ידית זמנית של אוריאה וכלור כך שבתנאים קטליטיים של נחושת הרדיקל הממוקד בחנקן נוצר ויכול לקטוף מימן מהאתר α′ או מהאתר β. על‑ידי עיצוב ליגנדים — מולקולות אורגניות העוטפות את הנחושת — הם משנים את הסביבה של הרדיקל. ליגנד מאוד מסיבי (מכונה L14) דוחף את המערכת לכיוון שלב 1,4′‑HAT חריג המכוון ליחידת N‑מנטיל, ומניב קיאנציה סלקטיבית ב‑α′. ליגנדים דקים יותר (כגון L8) מאפשרים את המסלול הקונבנציונלי 1,5‑HAT, וכך מכוונים את התגובה לאתר ה‑β.
מבחינת שליטה במיקום לשליטה בידיות
מעבר לבחירת המיקום, הצוות גם חיפש שליטה על בידיות (כירליות), שהיא מהותית כי רבות מהתרופות קיימות כצורות יד שמאל ויד ימין שמתנהגות שונה בגוף. כדי להשיג זאת הם מציגים ליגנדים כירליים — מולקולות בעלות צורה ידית — לתוך קומפלקס הנחושת. שני ליגנדים כאלה, L24 ו‑L41, נותנים העדפה גבוהה לאחד מהאננטיומרים כאשר מתקינה קבוצת ציאנו במיקומי β, כולל אתרים בנזיליים (בסמוך לטבעות ארומטיות) ואליליים (בסמוך לקשר כפול פחמן‑פחמן). על מגוון רחב של אמינים כמוצא, השיטה מספקת תוצרים מסונתזים ב‑β עם סלקטיביות מצוינת הן במיקום והן בבידיות, והיא עובדת בקנה מידה גרמי, מה שמעיד שההליך פרקטי ויציב לסינתזה.
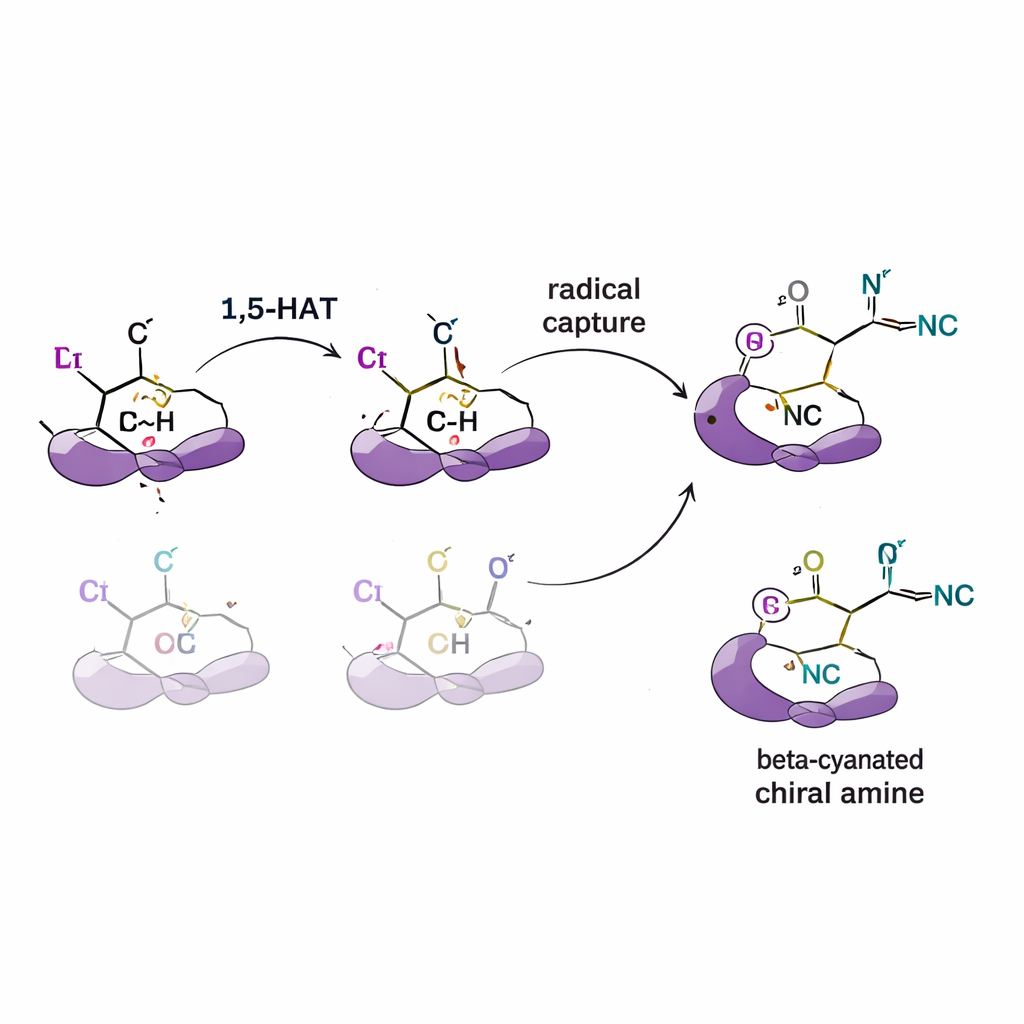
בדיקת המנגנון שמאחורי הסלקטיביות
כדי להבין כיצד נוצרת שליטה זו, המחברים ערכו סדרת ניסויים מכניסטיים. בהוספת מלכודות לרדיקלים הם מאשרים שבעצם משתתפים ביניים רדיקליים ריאקטיביים. בשימוש בסובסטרטים שבהם מימנים מסוימים הוחלפו בדוטריום (צורת מימן כבדה יותר) הם מגלים השפעות איזוטופיות של קינטיקה המעידות כי שלב העברת המימן הוא הצעד האיטי שקובע את הסלקטיביות. ניסויים עם תיוג מראים גם שהמימן נע בצעד יחיד חד‑כיווני ולא משוטט הלוך ושוב בין עמדות. סימולציות ממוחשבות משלימות (תורת הפונקציונל צפיפות) תומכות בממצאים האלה, ומראות שצורתו ומסתו של הליגנד משנות את אנרגיית המסלולים המתחרים של העברת המימן ואת הדרך שבה הרדיקל משלב אז עם הנחושת והציאניד כדי לתת את האננטיומר המועדף.
מה המשמעות לכך בעיצוב תרופות עתידי
בסך הכול, העבודה הזו מציגה אסטרטגיה גמישה לשיחזור קבוצות אמין נפוצות בשני אתרים קרובים על‑פי דרישה, עם שליטה מדויקת על בידיות המולקולה. על‑ידי החלפת הליגנד בקטליזטור נחושת, כימאים יכולים לבחור האם למקם קבוצת ציאנו על יחידת N‑מנטיל קטנה או על הפחמן השכן בשרשרת הצד אחרת, ואף לבצע זאת על פני מגוון מולקולות דמויות‑תרופה מורכבות. מאחר שקבוצות ציאנו הן אבני דרך יקרות ערך להמרה לקבוצות פונקציונליות רבות אחרות, הגישה הזו של "בחירת אתר על פי חיוג" ו"בחירת יד על פי חיוג" אמורה להקל על חקירה ואופטימיזציה של תרופות חדשות הבנויות מאותו שלד אמיני בסיסי.
ציטוט: Mao, YJ., Chen, X., Li, HL. et al. Ligand-controlled regiodivergent and enantioselective C–H cyanation of secondary amines. Nat Commun 17, 1869 (2026). https://doi.org/10.1038/s41467-026-68598-8
מילות מפתח: פונקציונליזציה של אמינים, העברת אטום מימן, קטליזת נחושת, קיאנציה אננטיוסלקטיבית, כימיה רפואית