Clear Sky Science · he
אנזים ברזל חד‑גרעיני לא‑הימי דינמי ביותר לייצור ביוסינתטי של איזוניטריל בשני שלבים
איך חיידקים בונים כלים כימיים בלתי שגרתיים
איזוניטרילים הם קבוצות כימיות קטנות אך עוצמתיות שמתנהגות כמו סרוויסר של שוויץ: הן יכולות לקשור מתכות, להגיב במגוון דרכים, ולעיתים קרובות משמשות כ"ראש" הפעיל של אנטיביוטיקות ורעלים טבעיים חזקים. חיידקים גורמי מחלות, כולל פתוגן הטוברקולוזיס Mycobacterium tuberculosis, מצדיעים איזוניטרילים למולקולות שומניות כדי לסייע להם לגנוב מתכות מהמארח. מאמר זה בוחן כיצד אחד האנזימים שלהם, בשם Rv0097, מבצע את הכימיה התובענית הזאת בשני צעדים מתואמים בקפידה.
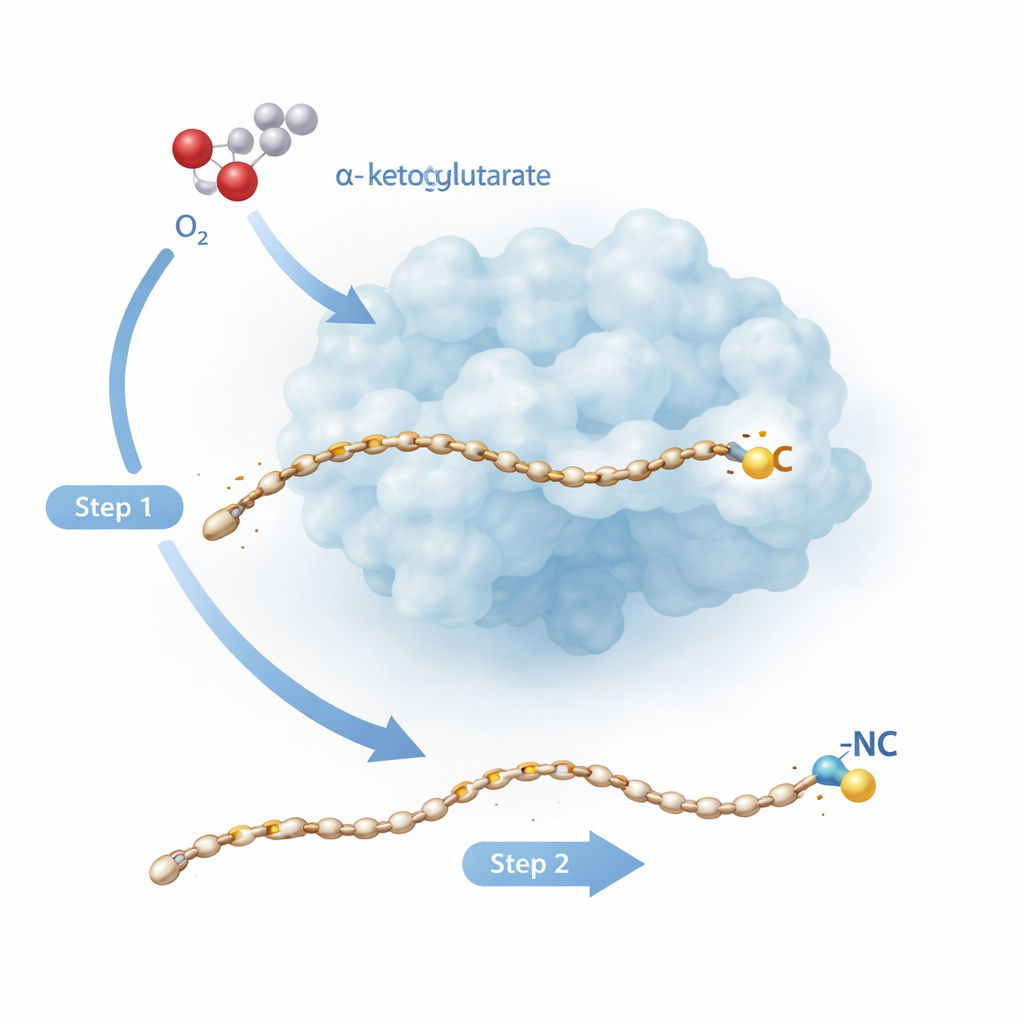
מַעֲשֵׂה מולקולרי דו‑שלבי
Rv0097 משתייך למשפחה גדולה של אנזימים התלויים בברזל שבדרך כלל מבצעים משימות פשוטות יותר כמו הוספת חמצן לאתר יחיד במולקולה. כאן, המשימה מורכבת יותר: מתוך בלוק בניין מסוג "גליציל–חומצת שומן", על האנזים ליצור קבוצת איזוניטריל חדשה לגמרי, כששני האטומים המרכזיים שלה — הפחמן והחנקן — מגיעים מאותו שבר גליצין קטן. מחקרים קודמים על אנזים קרוב, ScoE, הציעו שזה לא ניתן להשלמה במכה אחת. במקום זאת נדרשות שתי "חצי‑מחזורים" נפרדים, כל אחד מונע על‑ידי סוג של זן ברזל–חמצן שנוצר כשהאנזים מפצל מולקולה מסייעת בשם α‑קטוגלוטראט ומשלב אותה עם חמצן מהאוויר. המחקר החדש מתמקד באנזים של הטוברקולוזיס Rv0097 כדי לצפות, ברזולוציה אטומית, כיצד אנזים יכול לקשר בין שני צעדי‑שורש חירות על אותו תת‑ממשל תוך כדי שמירה על שליטה.
הקפאת האנזים בפעולה
באמצעות קריסטלוגרפיית קרניים‑X, החוקרים לכדו שש‑עשרה תמונות ברזולוציה גבוהה של Rv0097 במצבים שונים: ריק, קשור לתת‑המבנה השומני שלו (מולקולה בת עשר פחמנים הנקראת CADA), קשור למולקולת העזר α‑קטוגלוטראט, ובשילובים המדמים מתווכים חולפים של התגובה. המבנים הללו מראים של‑Rv0097 יש אישיות מפוצלת. במנוחה, אתר הפעילות שלו סגור ברובו, כאשר חומצת אמינו מפתח (פנילאלנין 102) מתהפכת בין שתי תצורות ששומרות על כיס זנב השומן יבש ומוכן לקשירה הידרופובית. כשה‑CADA נקשר, שארית זו ננעלת בתצורה אחת וה"ראש" הקוטבי של התת‑מולקולה מעוגן על‑ידי שרשראות טעונות בעוד זנבה השומני מקובע בתעלה הדוקה. שינויים בחלקיקי שער (F102 וג'רמין סמוך, G204) חוסמים את הכיס או נותנים כניסה למים מופרזת, מה שמפחית באופן חמור את הפעילות ומשנה את העדפת אורך השרשרת של האנזים.
מכסים נעים ולולאות דינמיות
מעבר לכיס התת‑מולקולה, Rv0097 מתנהג כמו מכונה זעירה עם דלתות נעות. הצוות הבחין בקונפורמציות "פתוחות" ו"סגורות" שבהן שתי אנטנות דמויות‑מכסה מתרחקות או מתקרבות מעל אתר הפעילות. פתיחה חושפת את מרכז הברזל ויוצרת מסלול לכניסת α‑קטוגלוטראט והתת‑מולקולה; סגירה מבודדת את הכימיה מהמים הסובבים כאשר התגובה מתנהלת. שתי לולאות פני שטח גמישות, שנקראות לולאת ה‑His ולולאת ה‑Arg על שם ההיסטידין והארגינין שהן נושאות, פועלות כשער נוסף. במבנים מסוימים הלולאות אלה מתכווננות פנימה כך שהארגינין יוכל לאחוז ב‑α‑קטוגלוטראט; באחרים הן נעות החוצה, ויוצרות כביכול תעלת צד דרכה יכולים לצאת שברי עזר משומשים (סוקצינאט ופחמן‑דיאוקסיד) ולחלוף α‑קטוגלוטראט חדש לשלב השני — וכל זאת בעוד המתווך שמקורו בתת‑המולקולה נשאר מהודק במקומו.
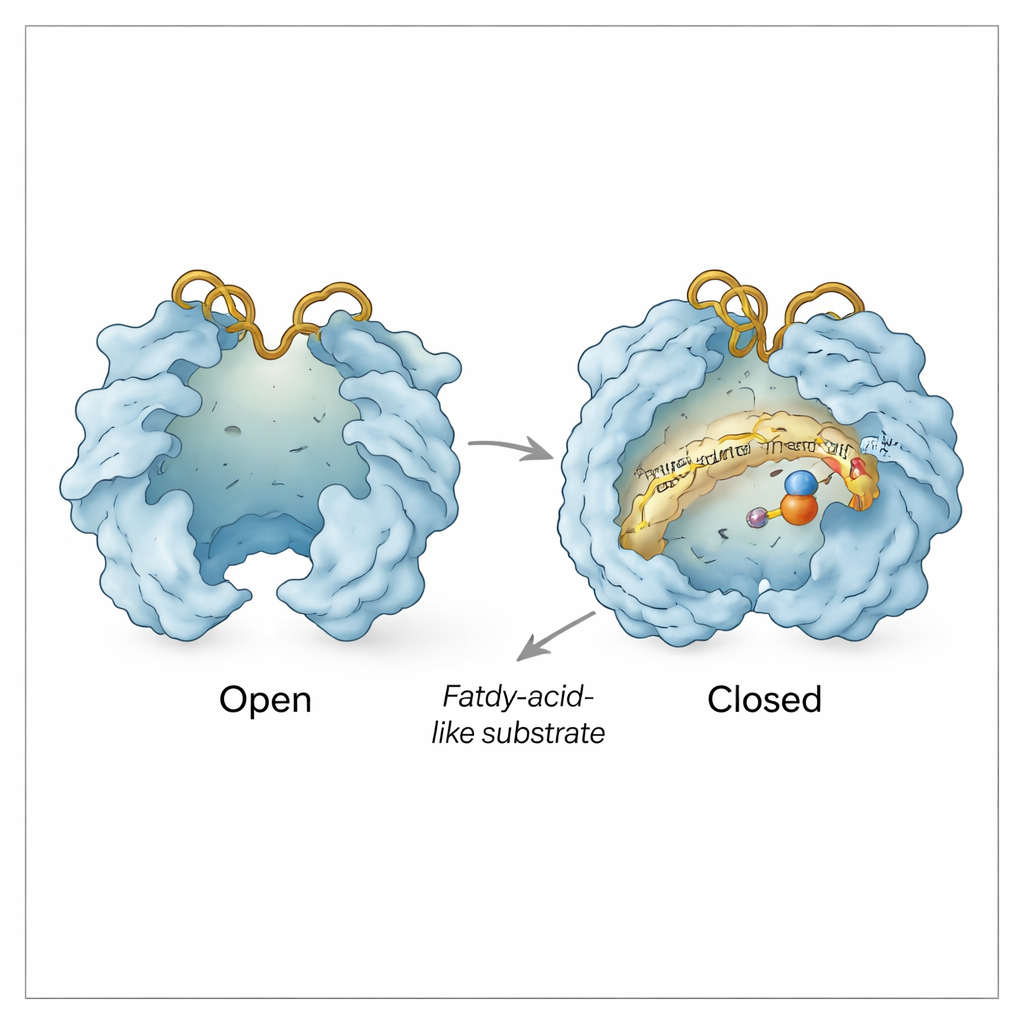
הגנה על מתווך שביר
בדיקות ביוכימיות תומכות בתמונה המבנית הזאת. החצי הראשון של התגובה ממיר את ה‑CADA למתווך אימין רב‑תגובה שהיה מתפרק במהירות אם היה נמלט לתמיסה. על‑ידי לכידת תוצר ההתפרקות הכימית שלו, המחברים מראים שרוב המתווך הזה מזוהה רק כשהאנזים עדיין נוכח, מה שמעיד שהוא נשאר קשור ומוגן בתוך Rv0097 בין שני חצי‑התגובות. המבנים מסבירים כיצד: מיקומים עדינים של לולאות ה‑His וה‑Arg, יחד עם הזזות קטנות של שאריות קרובות, נראים כאילו הם אוטמים את המתווך לתוך חלל מוגן בעודם עדיין מאפשרים למולקולות קטנות כמו α‑קטוגלוטראט, סוקצינאט ופחמן‑דיאוקסיד להחליף דרך תעלות מבוקרות.
מדוע זה חשוב לטוברקולוזיס ומעבר לו
ביחד, התוצאות חושפות את Rv0097 כאספקת‑קו דינמית וחלבונית יחידה שמשתמשת בכימיה מבוססת‑ברזל פעמיים ברצף על אותו תת‑מולקולה מבלי לשחרר מוצר חצי‑מהלך מסוכן. עבור חיידקי הטוברקולוזיס, הדיוק הזה תומך בייצור מולקולות המעוטרות באיזוניטריל שמסייעות להם לקבל מתכות חיוניות בתוך הגוף, ולמחקרים גנטיים יש עדויות לכך שהמסלול חשוב להישרדותם במהלך זיהום. עבור כימאים ומעצבי תרופות, העבודה מציעה תבנית למהנדס אנזימים קרובים לבניית תרכובות חדשות המכילות איזוניטריל, ומרמזת כי הפרעה למכסים ולשערים הנדים של Rv0097 יכולה להיות דרך לפיתוח אנטיביוטיקה חדשה.
ציטוט: Ye, N., Del Rio Flores, A., Zhang, W. et al. A highly dynamic mononuclear non-heme iron enzyme for the two-step isonitrile biosynthesis. Nat Commun 17, 2034 (2026). https://doi.org/10.1038/s41467-026-68588-w
מילות מפתח: ביוסינתזה של איזוניטריל, אנזים ברזל לא‑הימי, Mycobacterium tuberculosis, דינמיקת אנזימים, מוצרי טבע המתכתבים בקשרי כילייט