Clear Sky Science · he
הפרעת הומאוסטזיס של ברזל מרגישה את סרטן הלבלב לאלקטרופרציה בלתי הפיכה
להפנות חשמל וברזל נגד סרטן קטלני
סרטן הלבלב הוא אחד הסרטנים הקשים ביותר לטיפול, ואף טיפולים מקומיים אגרסיביים לעיתים קרובות אינם מצליחים למנוע חזרה. המחקר הזה בוחן דרך חדשה לשפר הליך קיים — אלקטרופרציה בלתי הפיכה (IRE), שמרסקת גידולים באמצעות פולסים חשמליים קצרים ועזים — כדי לגרום לו לפעול טוב ובטוח יותר. על ידי שיבוש חכם של האופן שבו תאים סרטניים מנהלים את ברזלם, החוקרים מראים שהם יכולים לדחוף תאים ששרדו למוות הרסני מסוג מסוים, ובכך להקטין את הסבירות שהגידול ישוב.
מדוע פולסים חשמליים לבדם אינם מספיקים
אלקטרופרציה בלתי הפיכה מטפלת בגידולים על ידי הכנסת אלקטרודות דקות לתוך הגידול או סביבו ושיגור פולסים מהירים ובעלי מתח גבוה. פולסים אלה יוצרים חורים קבועים בממברנות התאים, הורגים תאים סרטניים רבים ומעוררים תגובה חיסונית. אך השדה החשמלי אינו אחיד לחלוטין. אזורים שמקבלים פולסים חלשים מעט עלולים להשאיר תאים חיים, והשורדים הללו עלולים לזרע גידול חדש. כאשר הצוות בחן מקרוב תאי סרטן של הלבלב וגידולים בעכברים שנחשפו לשדה תת-קטלני, הם מצאו שבמקום למות בתהליך מונע-ברזל שנקרא פראופטוזיס, התאים הפעילו תוכנית הגנה נוגדת־חמצון רחבה. גנים מגן מרכזיים, כולל אלה המסייעים לנטרול נזקים הקשורים לברזל, הועלו ברמת הביטוי, מה שאיפשר לתאים לשרוד את ההתקפה ולהחלים.
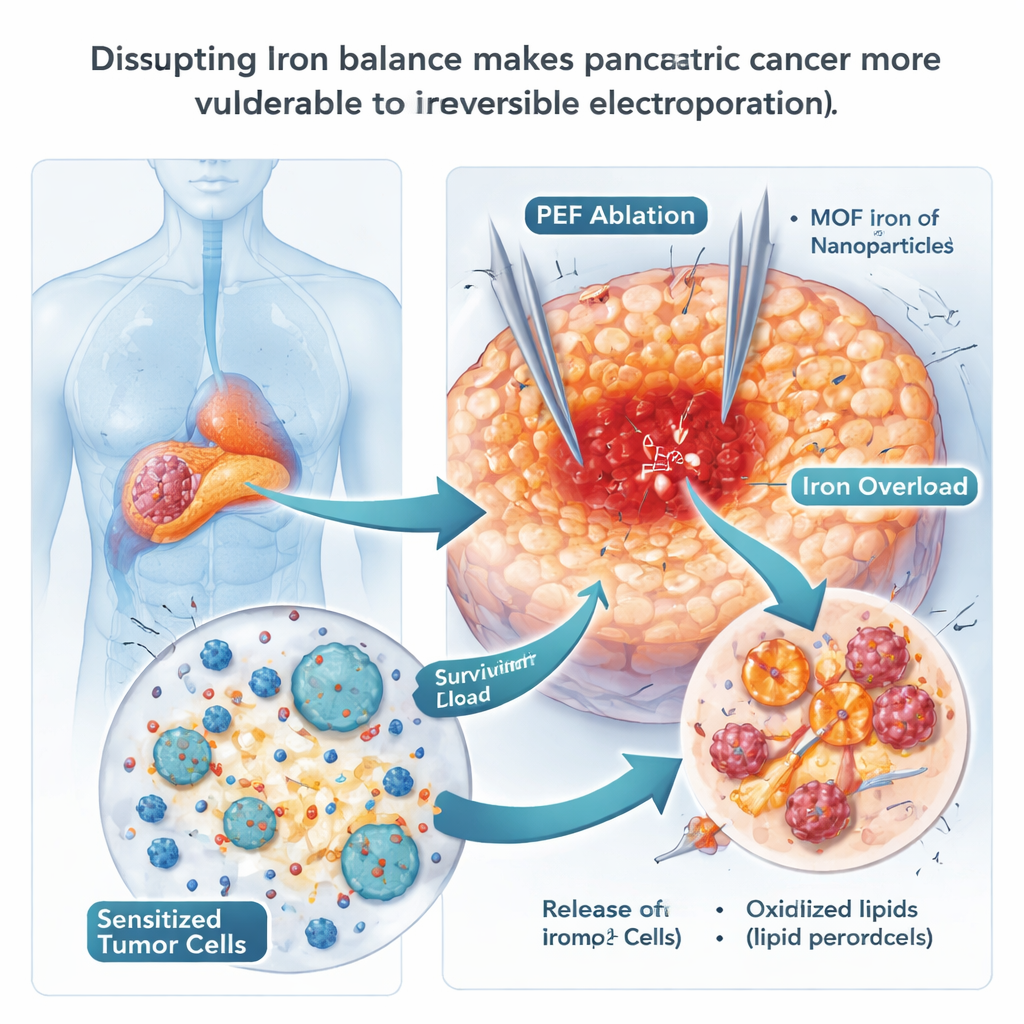
שימוש בננו-חלקיקי ברזל לדחיקת התאים להרס
מכיוון שפרופטוזיס תלוי בברזל, המדענים בדקו האם ננו-חלקיקים עשירים בברזל יכולים לדחוף את התאים הסרטניים מעבר לקצה. הם השתמשו בחלקיקים מבוססי מסגרת מתכת-אורגנית המכילים ברזל (MOF-Fe), שמשחררים ברזל במהירות בתוך תאיות חומציות בתאים. במנות בצלחת, תאי סרטן הלבלב שנטלו חלקיקים אלה צברו ברזל חופשי ושומנים מחומצנים בממברנותיהם — סימנים קלאסיים לפרופטוזיס — והקימו קולוניות במידה מועטה בהרבה. בעכברים, שילוב של MOF-Fe עם IRE עיכב את התחדשות הגידול לפרק זמן ארוך יותר מאשר כל טיפול בנפרד, והגידולים הראו סימנים רבים יותר לנזק חמצוני. עם זאת, היתרון הזה היה זמני: לאחר כשלוש שבועות החלו הגידולים להתאושש, מה שמרמז שהסרטן מצא דרך להסתגל לעודף הברזל.
מכוונים אל ה"כספת" של התא עבור הברזל
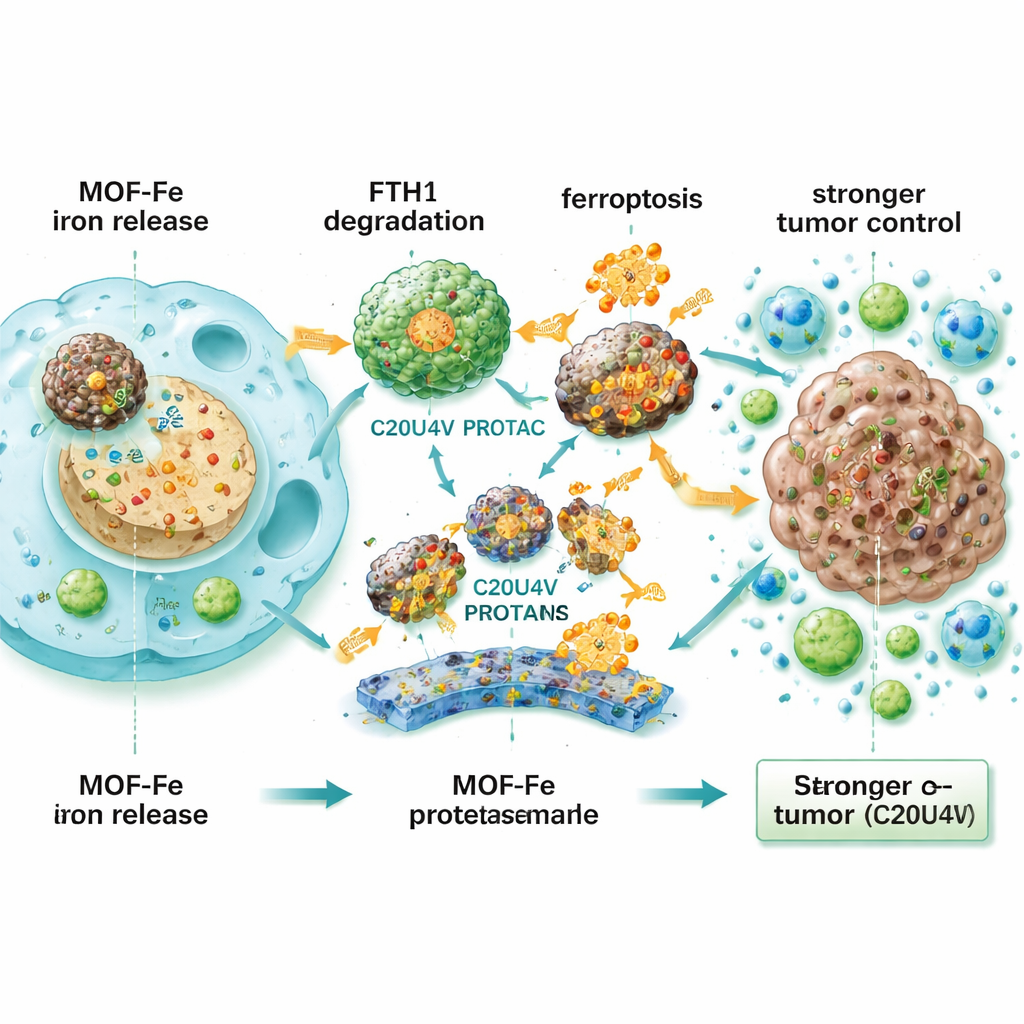
כדי להבין את ההתנגדות הזו, הצוות ניתח אילו חלבונים השתנו לאחר טיפול ב‑MOF-Fe. חלבון בולט היה שרשרת כבדה של פריטין 1 (FTH1), חלק מקומפלקס האחסון של הברזל בתא — המקבילה המולקולרית ל"כספת עמידה לאש" לברזל העודף. כאשר רמות FTH1 הוגברו בניסוי, התאים הסרטניים נעשו עמידים יותר לפרופטוזיס; כאשר FTH1 הופחתו, הם נעשו פגיעים יותר. זה הצביע על FTH1 כמגן מרכזי נגד מוות מונע-ברזל. החוקרים ייצרו אז מולקולה מעוצבת, C20U4V, שבנויה מחומצת ארכידוניק קשורה למסגרת PROTAC שמכוונת חלבונים ספציפיים למכונת ההשמדה של התא. בנוכחות MOF-Fe, C20U4V התקשרה לפריטין וגררה אותו לתג־השמדה, מה שהפחית באופן חמור את רמות FTH1 ומנע מהתא לאחסן את הברזל בבטחה.
מצלחות תאים לאורגנואידים ולעכברים
כשהושלבו MOF-Fe ו‑C20U4V, תאי סרטן הלבלב הראו לחץ חמצוני מוגבר, שומנים ממברנליים פגועים יותר, מיטוכונדריה חולה יותר, ויכולת התחדשות מצטמצמת במידה רבה. סינרגיה זו הופיעה גם באורגנואידים תלת־ממדיים שמקורם בחולים — מבנים זעירים דמויי גידול שגודלו מתאי חולים אמיתיים — שבהם הזוג התרופתי הקטין מאוד את גודל האורגנואידים ומספרם. מאחר ש‑C20U4V שומני ואינו מסיס במים, האריזה שלו נעשתה בתוך מיצלות רגישות לחמצן ריאקטיבי (M-C20U4V) שיכולות לנסוע בדם ולשחרר את התרופה ברקמת גידול שנמצאת בלחץ ובנזק. במודלים של עכברים עם גידולי לבלב שתוחמו מתחת לעור ובתוך הלבלב עצמו, שילוב משולש של IRE, MOF-Fe ו‑M-C20U4V הקטין את הגידולים בצורה משמעותית והאריך את ההישרדות בהשוואה לכל טיפול יחיד או משולב חלקי. בגידולים המטופלים נצפו פחות תאים מתחלקים, סימנים רבים יותר לפרופטוזיס וחדירה כבדה יותר של תאי T ותאים חיסוניים אחרים, מה שמעיד שהאסטרטגיה לא רק הורגת תאים ישירות אלא גם מסייעת למערכת החיסון לזהות ולהתקיף את הגידול.
מה זה יכול להצביע לחולים
ללא מומחיות מיוחדת, הרעיון המרכזי פשוט: גידולי לבלב לעיתים נמלטים לאחר הרס בפולסים חשמליים כי חלק מהתאים שורדים ומסתגלים במהירות. עבודה זו מראה שמילוי התאים האלה בברזל ובמקביל נטרול "כספת" הברזל שלהם יכול לכפות עליהם מצב הרס עצמי שהם מתקשים לעמוד בו. גישה זו עדיין בשלבי ניסוי ותדרוש בדיקות נרחבות של בטיחות ומעשיות בבני אדם, אך היא מציעה כי כיוונון מדויק של האופן שבו גידולים מנהלים יסוד בסיסי כמו ברזל יכול להפוך טיפול מקומי בלתי מושלם לנזק מכריע יותר כנגד אחד הסרטנים הקטלניים ביותר.
ציטוט: Li, L., Su, S., Wang, Z. et al. Disruption of iron homeostasis sensitizes pancreatic cancer to irreversible electroporation. Nat Commun 17, 1866 (2026). https://doi.org/10.1038/s41467-026-68585-z
מילות מפתח: סרטן הלבלב, אלקטרופרציה בלתי הפיכה, פרוטופטוזיס (פרוטוזה), ננו-חלקיקי ברזל, תרפיית PROTAC