Clear Sky Science · he
HIF מחזיק מעגל בקרה שעתקתי של ביטוי EPAS1 בסרטן כלייתי מסוג תא צלול
מדוע סרטן הכליה דורש בחינה מדוקדקת יותר
קרצינומת הכליה מסוג תא צלול היא הצורה השכיחה ביותר של סרטן הכליה, ורבים מהחולים כיום מקבלים תרופות החוסמות חלבון בשם HIF‑2α. תרופות אלה יכולות לצמצם גידולים, אך אינן פועלות באותה מידה על כולם. מחקר זה שואל שאלה פשוטה אך חשובה: מה גורם לחלק מהגידולים הכלייתיים לייצר כל כך הרבה HIF‑2α, והאם הבנת "מפתח ההפעלה" הזה תעזור לנו לחזות מי יפיק את התועלת הכי רבה מהטיפול ולתכנן טיפולים חדשים?
חיישן החמצן שהופך למנותק
תאי כליה בריאים משתמשים בחלבון בטיחות בשם VHL כדי לשמור על גורמי חישה לחמצן, הנקראים HIF, תחת שליטה הדוקה. כשהחמצן נש abundance, VHL מסמן חלבוני HIF להרס ומונע מהם להפעיל גנים המקדמים יצירת כלי דם וחלוקה תאית. בסרטן הכליה מסוג תא צלול, VHL לרוב אובד או נפגע. כתוצאה מכך, אחד מחברי משפחת HIF, HIF‑2α (מקודד על ידי גן EPAS1), נע מההרס ומצטבר. עבודות קודמות הראו כי פעילות גבוהה של HIF‑2α קשורה לצמיחה מהירה יותר של הגידול ותוצאות קליניות גרועות יותר, ושחסימת HIF‑2α יכולה להאט או לעצור גידולים אצל חלק מהחולים. עם זאת, הצעדים המולקולריים שמגבירים את פעילות גן EPAS1 בגידולי כליה לא היו מובנים היטב.
מתג DNA נסתר של גן סרטני
באמצעות דגימות גידול מחולים, נתוני תא יחיד ודגמי תאי סרטן, המחברים מראים שה-mRNA של HIF‑2α גבוה באופן ניכר בגידולים של כליה מסוג תא צלול בהשוואה לרקמת כליה נורמלית או לסוגי גידול כליה אחרים. לאחר מכן סרקו את אזור EPAS1 בגנום אחר סימני כימיה ומבנה שמצביעים על DNA רגולטורי פעיל. זה חשף מגבר עוצמתי — מעין מתג גנטי מרחוק — הממוקם כ-70,000 אותיות DNA upstream מ-EPAS1 הפעיל ספציפית בגידולי תא צלול. בתאי הגידול הכרומטין באזור המגבר פתוח, מעוטר בסימני הפעלה ומתעקל במגע פיזי עם המפעיל (promoter) של EPAS1, בעוד שבתאי האוליגת הכלייתיים הנורמליים אזור זה ברובו שקט. פעילות המגבר זו מתואמת עם רמות גבוהות יותר של EPAS1 במאגרים גדולים של נתוני סרטן. 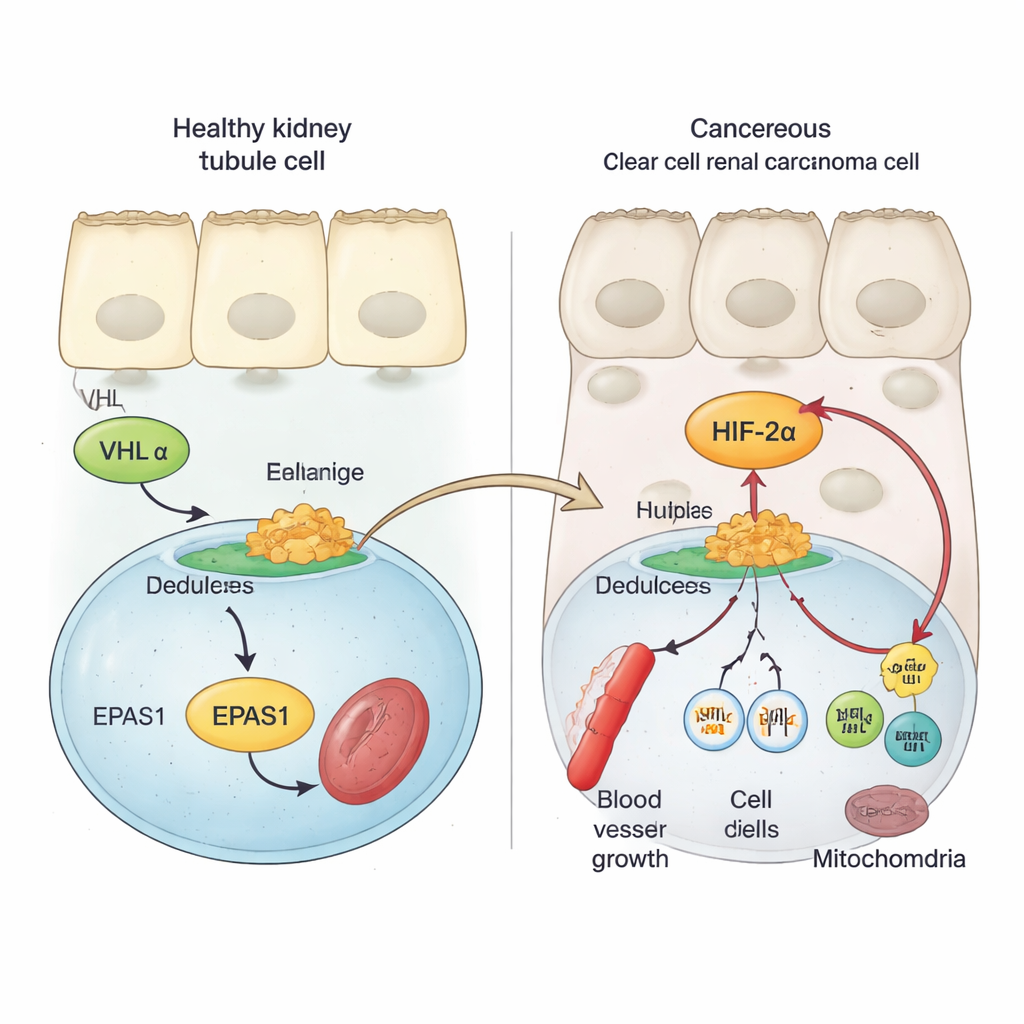
מעגל מחזק את עצמו שמונע על ידי גורמי זהות כלייתיים
המחקר מגלה שחלבוני HIF עושים יותר מלהגיב לחוסר חמצן — הם למעשה מסייעים לנהוג את הייצור שלהם עצמם. כאשר החוקרים משיבים את VHL או מסירים חלבון שותף מרכזי של HIF (HIF‑1β), רמות EPAS1 פוחתות והמגבר נעשה פחות נגיש. מיפוי ישיר של מגעי חלבון–DNA מראה ש-HIF נקשר לשני אזורי מגבר upstream של EPAS1, כולל המגבר הספציפי לתא צלול. בתאי גידול כליה, המגבר הזה גם מאויש על ידי PAX8 ו-HNF‑1β, גורמי שעתוק המסייעים להגדיר זהות תא כלייתי וידועים כתומכים בצמיחה סרטנית. הפרעה ב-PAX8 או HNF‑1β, או מוטציה באתרי הקשירה שלהם בתוך המגבר, מפחיתה את RNA והחלבון של HIF‑2α ומחלישה את פעילות המגבר. יחד, ממצאים אלה חושפים מעגל אוטו-רגולטורי: HIF‑2α, הפועל עם גורמי שושלת כליה, מרים את פעילות מגבר EPAS1, אשר בתורו מates עוד ייצור של HIF‑2α.
סיכון גנטי והתנהגות גידולית מתכנסות על אותו מעגל
אזור EPAS1 מזוהה זמן רב במחקרי גנום-רחב כנקודת חמות לסיכון לסרטן כליה, כאשר וריאנטים תורשתיים מסוימים קשורים לשכיחות סרטן גבוהה יותר ולמוטציות VHL בגידולים. על ידי שילוב נתוני גנטיקה עם מדידות ביטוי גנים, המחברים מראים שאנשים הנושאים את הגרסה בסיכון גבוה של וריאנט מרכזי ב-EPAS1 נוטים להציג רמות גבוהות יותר של HIF‑2α בגידולים שלהם — ואפילו בתאי הצינורות הכלייתיים הנורמליים כאשר HIF מייצב באופן ניסיוני. הדבר מציע שכליונות DNA תורשתיים יכולים לכוונן עד כמה המגבר מגיב, ולתת יתרון לחלק מכליות להעצים HIF‑2α יותר לאחר אובדן VHL. ניסויים בתאי גליוובלסטומה מראים שגם במקרים מסוימים של גידולי מוח ניתן להפעיל את אותו המגבר, מרמזים שהמודול הרגולטורי הזה עשוי להיות ממוחזר בסרטנים אחרים שבהם HIF‑2α חשוב. 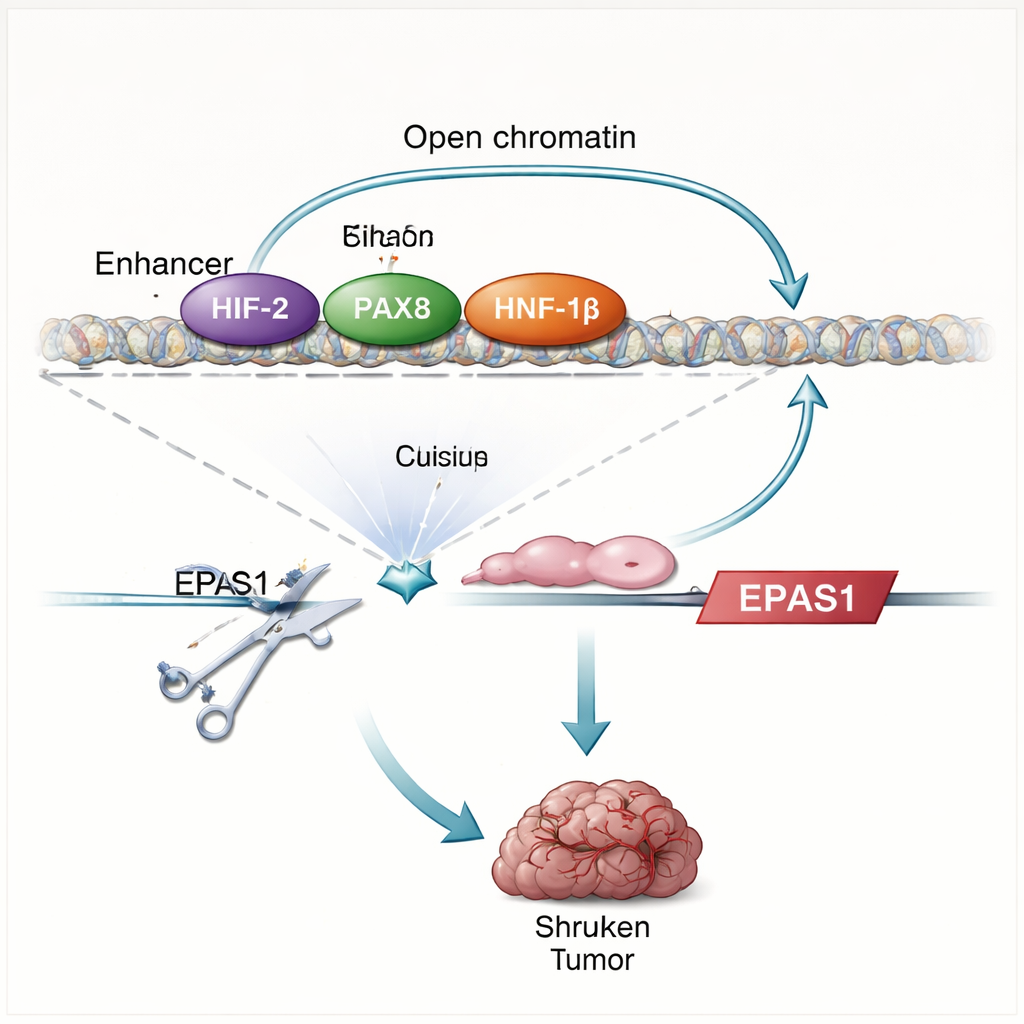
לשבור את המעגל כדי לעצור את צמיחת הגידול
כדי לבדוק עד כמה המגבר חיוני, הצוות משתמש בעריכת גנום CRISPR כדי לפגוע במוטיבים של קשירת HIF בתוכו בקווי תאי סרטן כליה ובתאי גידול טריים מהחולים. החיתוך הזה מוריד את RNA של HIF‑2α בכ-שליש עד חצי, מוריד את הרמות של גנים מוכרים המופעלים על ידי HIF‑2α כגון CCND1 ו-VEGFA, ומחליש את תוכנית הגנים של היפוקסיה רחבה יותר. כאשר תאים נערכו הושתלו בעכברים, הם ברובם לא הצליחו ליצור גידולים, בניגוד נחרץ לתאים בקבוצת הבקרה. דפוס שינויי הגנים לאחר שיבוש המגבר משקף בקירוב את ההשפעות של חסימת HIF‑2α באופן ישיר באמצעות תרופה קלינית, ומבליט שגם אלמנט DNA יחיד זה הוא מניע מרכזי של מסלול HIF‑2α בסרטנים אלה.
מה זה אומר עבור חולים וטיפולים
ללא מומחים, המסר המרכזי הוא שהמחברים גילו מתג DNA מחזק את עצמו ששומר חלבון מעורר סרטן מרכזי, HIF‑2α, דלוק בגידולי כליה מסוג תא צלול. מתג זה תלוי גם באובדן הבלם הבטיחותי VHL וגם בחלבוני עזר ספציפיים לכליה, והוא מושפע מווריאנטים גנטיים תורשתיים. מאחר שהמגבר פעיל מאוד ברבים מהגידולים מסוג תא צלול וקושר בחוזקה את עוצמת הפעלת מסלול HIF‑2α, מדידת פעילותו — או מיקוד ישיר בו — עשויה לעזור לזהות חולים שייהנו הכי הרבה מהמעכבים הקיימים של HIF‑2α ואף להציע דרכים חדשות לכבות את המסלול הזה כאשר הגידולים מפתחים עמידות לתרופות.
ציטוט: Naas, S., Krüger, R., Grampp, S. et al. HIF sustain a transcriptional regulatory circuit of EPAS1 expression in renal clear cell carcinoma. Nat Commun 17, 1764 (2026). https://doi.org/10.1038/s41467-026-68576-0
מילות מפתח: קרצינומת כליה מסוג תא צלול, HIF-2α, מגביר EPAS1, מוטציית VHL, גנטיקה של סרטן הכליה