Clear Sky Science · he
ליפידים אתריים משפיעים על גורל תאי סרטן על־ידי ויסות קליטת ברזל
איך שומן ידוע מעט עשוי לחשוף את נקודת התורפה של הסרטן
לעתים קרובות מתארים את הסרטן כ"מחלה של גנים", אך המחקר הזה מראה כי השומנים שמרכיבים את קליפת התא החיצונית יכולים להיות בעלי חשיבות דומה. החוקרים מציגים כיצד קבוצה מיוחדת של שומנים, הנקראת ליפידים אתריים, מסייעת לתאי סרטן מסוכנים למשוך ברזל מהסביבה שלהם — דבר שמזין הן את היכולת שלהם להתפשט והן את הרגישות שלהם לצורת מוות תאית שזוהתה לאחרונה. הבנת הקשר המוסתר הזה בין ממברנות התא, ברזל והתנהגות הגידול עשויה לפתוח דלתות לטיפולים שמחסלים באופן סלקטיבי את תאי הסרטן האגרסיביים ביותר.
דרך אחרת לחשוב על תאי סרטן
מרבית מחקרי הסרטן מתמקדים במוטציות בדנ"א ובחלבונים שהם מקודדים. עבודה זו מזיזה את תשומת הלב לממברנת התא — הקליפה השמנונית הדקה שסובבת כל תא. בתוך קליפה זו ישנם סוגים רבים של ליפידים (שומנים), לכל אחד צורות ותכונות פיזיקליות שונות. המחברים מתמקדים בליפידים אתריים, שמרכיבים כמות של כ‑20% מהפוספוליפידים ברבים מתאי היונקים אך זכו למחקר מוגבל יחסית. הם מגלים שתאי סרטן ממטסטטיים ומחקים־גזע מארגנים את ממברנותיהם בעומס ליפידים אתריים גבוה, מה שמוריד את המתיחות של הממברנה ומעלה את נִבְחִיוּתָה. התכונות הפיזיקליות האלה, בתורן, משנות את אופן קליטת הברזל על ידי התאים — מתכת שמניעה הן גדילת גידול והן תהליך הרסני הנקרא פרופתוזיס, צורת מוות תאית התלויה בברזל.
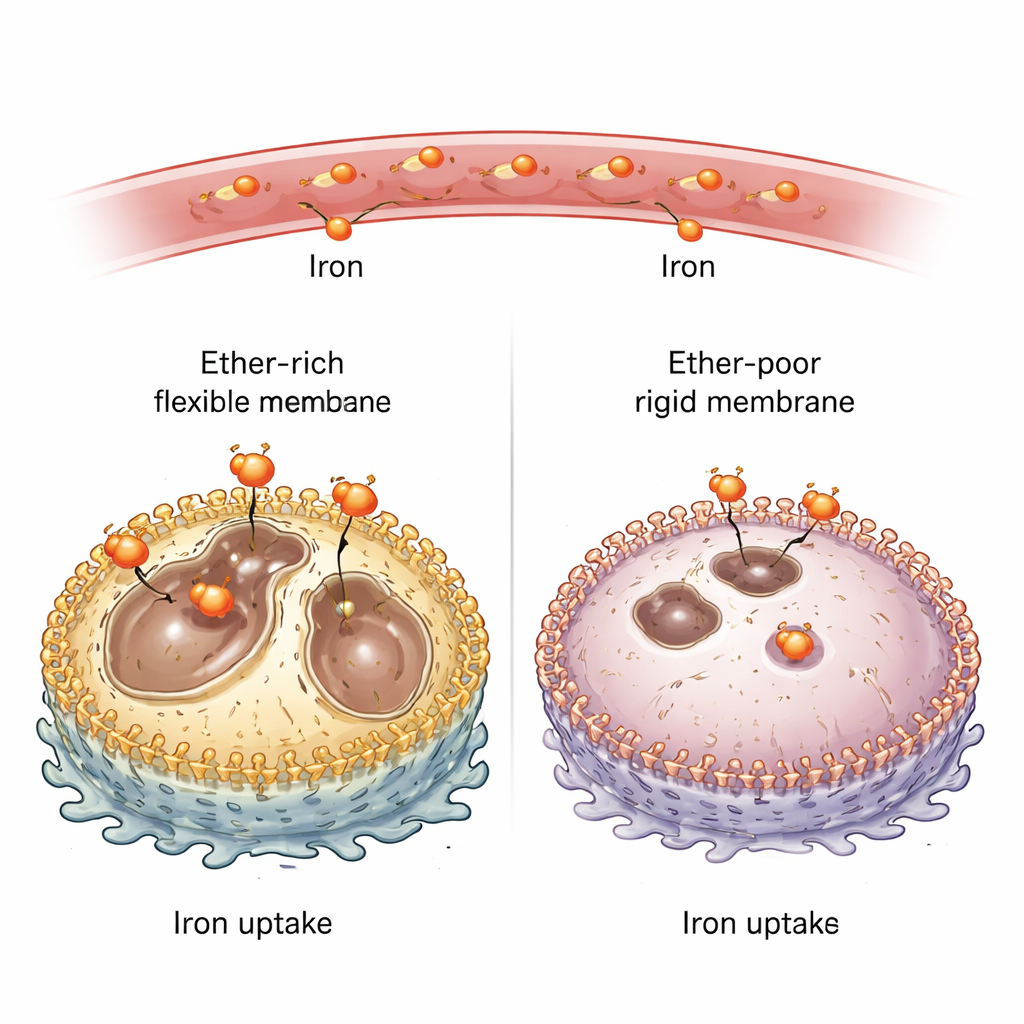
קישור בין שומני הממברנה לקליטת ברזל
כדי לבדוק את תפקיד הליפידים האתריים, הצוות השבית אנזימים מרכזיים הנדרשים לייצורם בכמה קווי תאים סרטניים של עכבר ואדם. ללא אנזימים אלה, רמת הליפידים האתריים בממברנת הפלזמה צללה מכ‑כ‑25% מכלל הליפידים לכמה אחוזים בלבד. באופן מפתיע, תאים דלים באתררים נשאו מעט מאוד ברזל "אדוקס־פעיל" — הצורה הכימית הריאקטיבית של הברזל שמשתתפת בתגובות חמצון — הן בתרבית והן בגידולים מושתלים בעכברים. כאשר המדענים סיפקו ברזל חיצוני נוסף, רמות הברזל בתאים עלו שוב והם חזרו להיות רגישים לתרופות שמעוררות פרופתוזיס. ממצא זה הראה שליפידים אתריים עושים יותר מאשר לשמש דלק לחמצון; הם שולטים באופן פעיל בכמות הברזל שנכנסת לתא.
שער ברזל מיוחד: מסלול CD44
החוקרים שאלו אז כיצד הרכב הממברנה משנה את קליטת הברזל. תאים בדרך כלל מייבאים ברזל דרך חלבון ידוע בשם קולטן הטרנספרין, אך תאי סרטן אגרסיביים ומחקי‑גזע תלויים גם במסלול אחר: חלבון פני שטח בשם CD44 שמושך ברזל הקשור למולקולת סוכר הנקראת חומצה היאלורונית. בעזרת גלאים פלואורסצנטיים הראו הצוות שהשבתת הליפידים האתריים משפיעה במידה מזערית על קליטת הטרנספרין אך מעכבת בחדות אנדוציטוזה מתווכת‑CD44 — מסלול חילוף חומרים חלופי, בלתי תלוי־כלטרין, להחדרת חומר לתא. שיקום הליפידים האתריים, או הוספתם מחדש בצורת ליפוזומים, החזיר את פעילות מסלול CD44. שיבוש CD44 עצמה או עיכול של חומצה היאלורונית הורידו את רמות הברזל בתא, ואישרו שמסלול התלוי־אתרים הזה הוא שער ברזל מרכזי בתאי סרטן אלה.
כיצד ממברנות רכות יותר משנות את התנהגות התא
מדוע ליפידים אתריים חשובים כל כך ל‑CD44 אך פחות לקולטן הטרנספרין הקלאסי? התשובה טמונה בפיזיקה. בעזרת כלים מדויקים שמשכו נכסים זעירים מפני התא הראו המחברים שממברנות עשירות באתררים מאופיינות במתיחות נמוכה ובקלות עיוות גבוהה יותר. כאשר הסירו את הליפידים האתריים, מתיחת הממברנה עלתה והליפידים נארזו בצפיפות רבה יותר, מה שהקשיח את הממברנה. שינויים אלה פגעו קשות בצורות אנדוציטוזה שתלויות בקטעי ממברנה גמישים ודמויי־רף — בדיוק סוג המסלול ש‑CD44 משתמש בו — בעוד שקליטת תלויה־כלטרין נותרה ברובה שלמה. ליפידים אתריים גם סייעו לייצב "ראפטים" ליפידים, איים מסודרים זעירים בממברנה שבהם CD44 מצטבר לפני שנכנס פנימה. בקיצור, הליפידים האתריים מכוונים את הנוף הפיזי של הממברנה לטובת קליטת ברזל מונעת‑CD44.
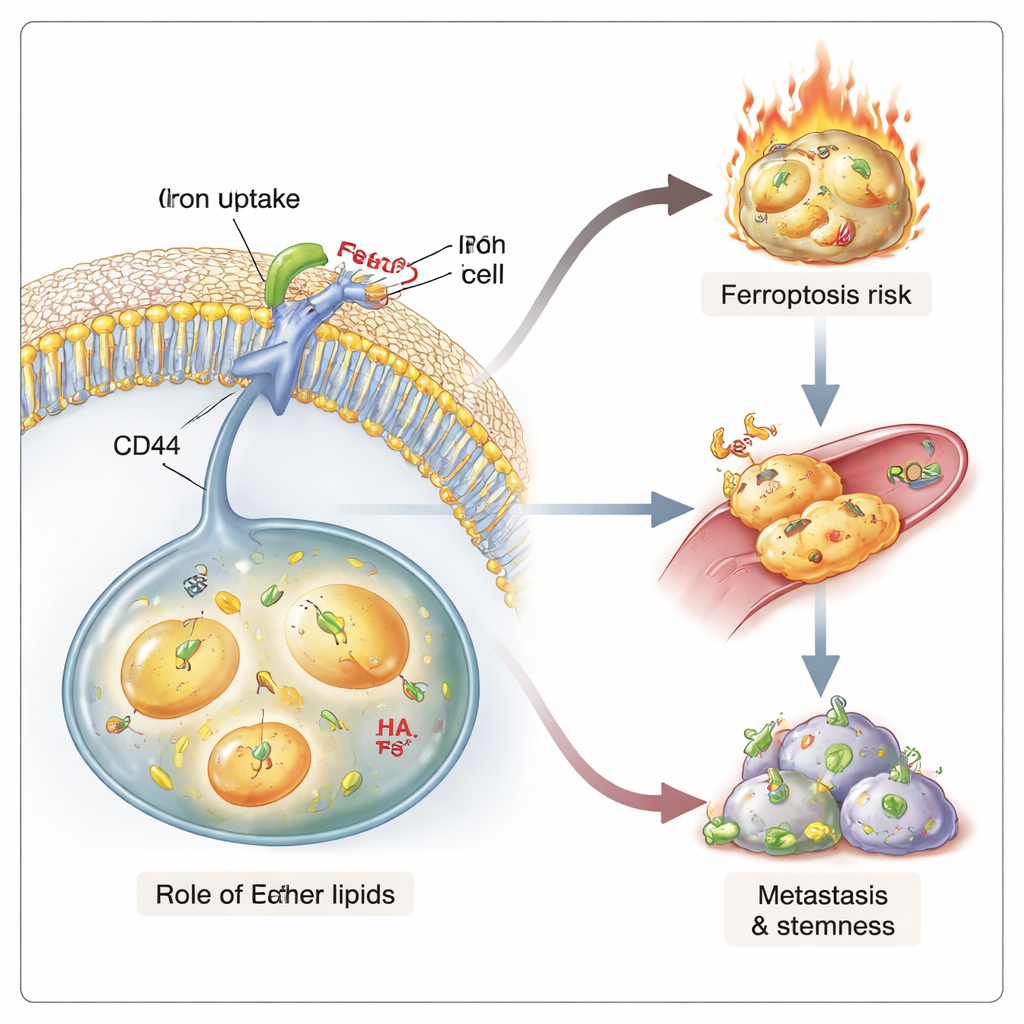
מדללים גם את ההפצה וגם את ההרס העצמי
רמות ברזל גבוהות ומתיחת ממברנה נמוכה מקושרות לתכונות שהופכות סרטן לקטלני: היכולת לשתול גידולים חדשים ולהישאר בחיים לאחר טיפול. במודלים תלת‑ממדיים של כלי דם זעירים, תאי סרטן עשירים באתררים ברחו ביתר קלות ממבנים דמויי‑כלי דם — שלב ראשוני במטסטזיס. בעכברים, תאי סרטן דלים באתררים יצרו פחות גרורות, אף על פי שהגידולים הראשוניים שלהם גדלו בקצב דומה. תאים אלה הראו גם ירידה ב"מאפייני גזע", כפי שנמדד ביכולתם המוקטנת ליצור ממוספרות בתרבית ולהשיג היווצרות גידולים בהשתלות במינון מוגבל. במקביל, תאים עשירים באתררים, עם עומס ברזל גבוה וליפידים שניתנים לחמצון בקלות, היו פגיעים יותר לפרופתוזיס כשאתגרו אותם בתרופות ספציפיות או ברמיזות חיסוניות. לפיכך, ליפידים אתריים יוצרים מצב דו‑חרבי: הם תומכים בהתנהגות אגרסיבית ודמוית‑גזע אך הופכים את אותם תאים להרוגים באופן ייחודי על‑ידי נזק ליפידי מונע‑ברזל.
מדוע זה משמעותי לטיפולי סרטן בעתיד
ללא מומחיות רבה, המסר המהותי הוא שלא כל תאי הסרטן שווים מבחינה מסוכנות, והממברנות החיצוניות שלהם עוזרות לקבוע הן כמה הם מסכנים והן כמה הם פגיעים. ליפידים אתריים מעצבים מחדש את פני התא כך שברזל יוכל לזרום דרכו דרך דלת מיוחדת, מה שממריץ תאים ממטסטטיים ודמויי‑גזע אך גם ממלא אותם בחומרי הגלם להרס עצמי. טיפולים שמשנים את ייצור הליפידים האתריים, שמפריעים לקליטת ברזל מבוססת‑CD44, או שמפעילים פרופתוזיס באופן מבוקר עשויים לטרגט באופן סלקטיבי אוכלוסיות תאי סרטן קשות‑לטיפול תוך חיסכון ברקמות בריאות. על ידי חשיפת האופן שבו קבוצת שומנים ידועה מועט מקשרת בין פיזיקת הממברנה, חילוף חומרים של מתכות וגורל התא, המחקר הזה פותח נתיב חדש לעבר התערבויות סרטן חכמות ומדויקות יותר.
ציטוט: Mansell, R.P., Müller, S., Yang, JS. et al. Ether lipids influence cancer cell fate by modulating iron uptake. Nat Commun 17, 1835 (2026). https://doi.org/10.1038/s41467-026-68547-5
מילות מפתח: ליפידים אתריים, תאי גזע סרטניים, קליטת ברזל, פרופתוזיס, גרורות