Clear Sky Science · he
פאלמיטואית חומצה שמפעילה פאלמיטואילציה של B7H3 מקדמת בריחת מערכת החיסון
מדוע המחקר הזה חשוב לחולי סרטן
רוב האנשים יודעים שתרופות אימונו‑תרפיה חדשות יכולות לסייע למערכת החיסון לתקוף סרטן, אך מטופלים רבים עם סרטן מעי גס שכיח נהנים ממעט תועלת. מחקר זה חושף תחבולה ביוכימית שממאירות המעי משתמשות בה כדי להגן על עצמן מפני התקפה חיסונית, ומצביע על סוג חדש של תרופה — פפטיד קצר — שעשוי להעצים את יעילות האימונו‑תרפיה עבור מטופלים אלה.
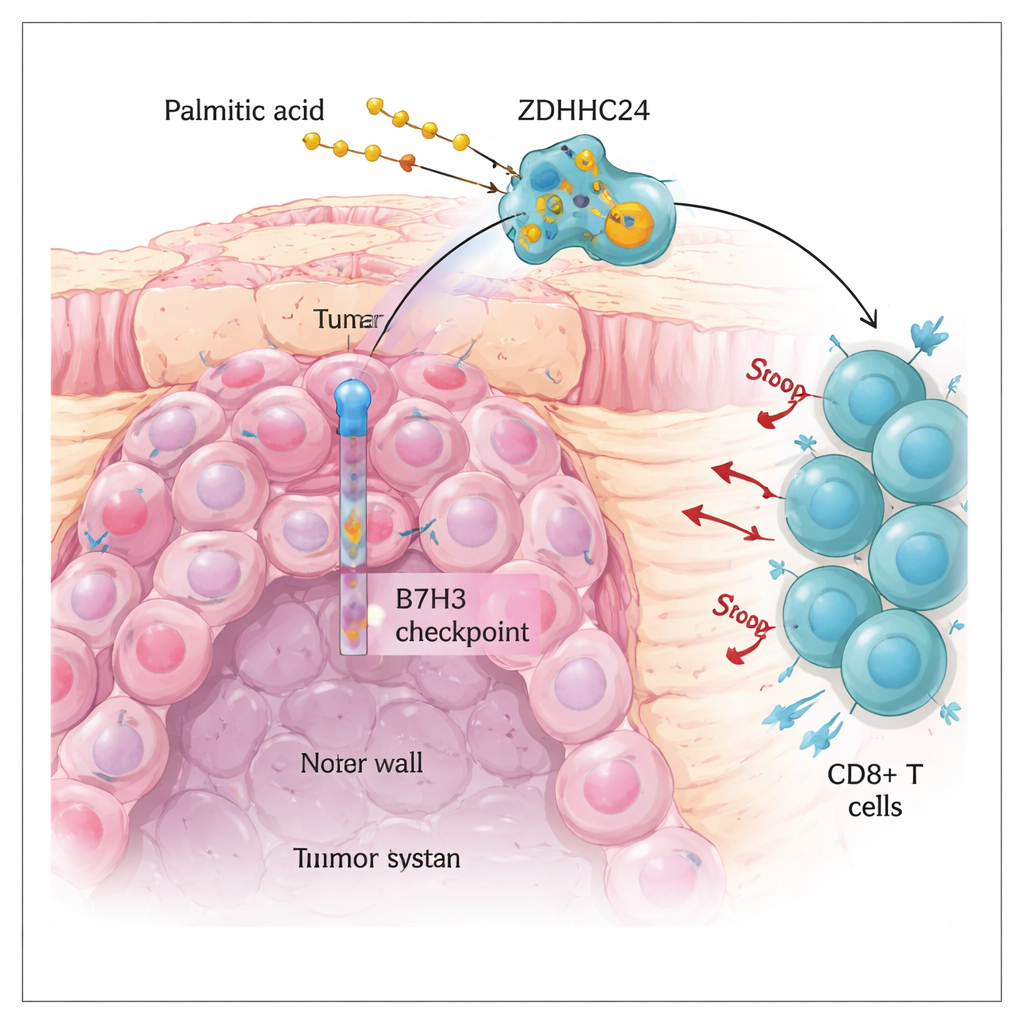
מחסום באימונו‑תרפיה הנוכחית של סרטן המעי
סרטן המעי הגס הוא אחד מסוגי הסרטן הנפוצים ביותר בעולם. תרופות אימונו‑תרפיה המשחררות את "הבלמים" החיסוניים, כגון מעכבי PD‑1 ו‑PD‑L1, שינו את הטיפול עבור מיעוט של מטופלים שמגTumors שלהם מכילים שגיאות רבות בדנ"א (הנקראים MSI‑H). למרבה הצער, רוב מקרי סרטן המעי הם יציבים במיקרוסטלייטים (MSS) ומגיבים באופן לקוי לטיפולים אלה. החוקרים התמקדו במולקולה מעכבת נוספת בשם B7H3, שנמצאת על פני תאי הגידול ומדכאת את פעילות התאים הקוטלים, ובפרט תאי CD8+. הם מצאו שרמות החלבון B7H3 גבוהות במיוחד בגידולי MSS ומקושרות להישרדות גרועה, על אף שהגן הבסיסי של B7H3 אינו פעיל יותר. הפער הזה העלה שאלה חשובה: מה שומר על רמות גבוהות כל כך של חלבון B7H3 על תאי הגידול?
איך שומן נפוץ עוזר לגידולים להסתתר
החוקרים חשדו שחילוף החומרים של הגידול עשוי לייצב את B7H3. בהשוואת פעילות גנים ופרופילים של מולקולות קטנות בין גידולי MSS ל‑MSI‑H של המעי הגס, הם גילו שמסלולי שומן רבים שונים, וביוחד חומצת שומן אחת, חומצה פאלמית (palmitic acid), בולטת. כשהגבירו חשיפה של תאי סרטן מעי למספר תוצרי פירוק שומניים במעבדה, רק חומצה פאלמית הביאה לעלייה ברורה ברמות חלבון B7H3. ניסויים נוספים הסבירו מדוע: חומצה פאלמית מזינה תהליך כימי שנקרא פאלמיטואילציה, שבו שרשרת שומנית מצמידה לנקודות ספציפיות בחלבונים. שינוי זה, שמתבצע על ידי אנזים בשם ZDHHC24 באתר ציסטאין יחיד בתוך B7H3, הפך את B7H3 ליציב יותר ולשכיח יותר על פני התא הגידולי.
חסימת מסלול הפסולת עבור "הבלם" החיסוני
תאים בדרך כלל מסלקים חלבונים לא רצויים או פגומים באמצעות מערכות הפועלות כמו מיחזור ופינוי אשפה. החוקרים הראו ש‑B7H3 מפורק בעיקר על ידי מסלול "אכילה עצמית" תאי הנקרא אוטופגיה, המשתמש בחלבון רצפטור בשם SQSTM1/p62 כדי לסמן מטען להשמדה. כאשר B7H3 עבר פאלמיטואילציה, הוא התקשר באופן גרוע יותר לרצפטור זה ונמנע מהרס באמצעות אוטופגיה, מה שהוביל לרמות גבוהות ומתמשכות של ה"בלם" החיסוני. כאשר אתר הפאלמיטואילציה עובר מוטציה כך שאינו יכול לשאת את התג השומני, או כאשר מחקו את אנזים ZDHHC24, B7H3 נשלח ביעילות רבה יותר לשקיות הפסולת התאית ונפרק. בעכברים, גידולים שחסרו B7H3 מפאלמיטואילציה גדלו לאט יותר, לא שינו את קצב הצמיחה הפנימי שלהם בבעלי חיים חסרי חיסון, והראו באופן דרמטי יותר תאי CD8+ ופעילות קטילת גידול חזקה יותר. ממצאים אלה מראים שהשינוי פועל בעיקר על ידי נטרול המערכת החיסונית, ולא על ידי שינוי קצב חלוקת תאי הסרטן.
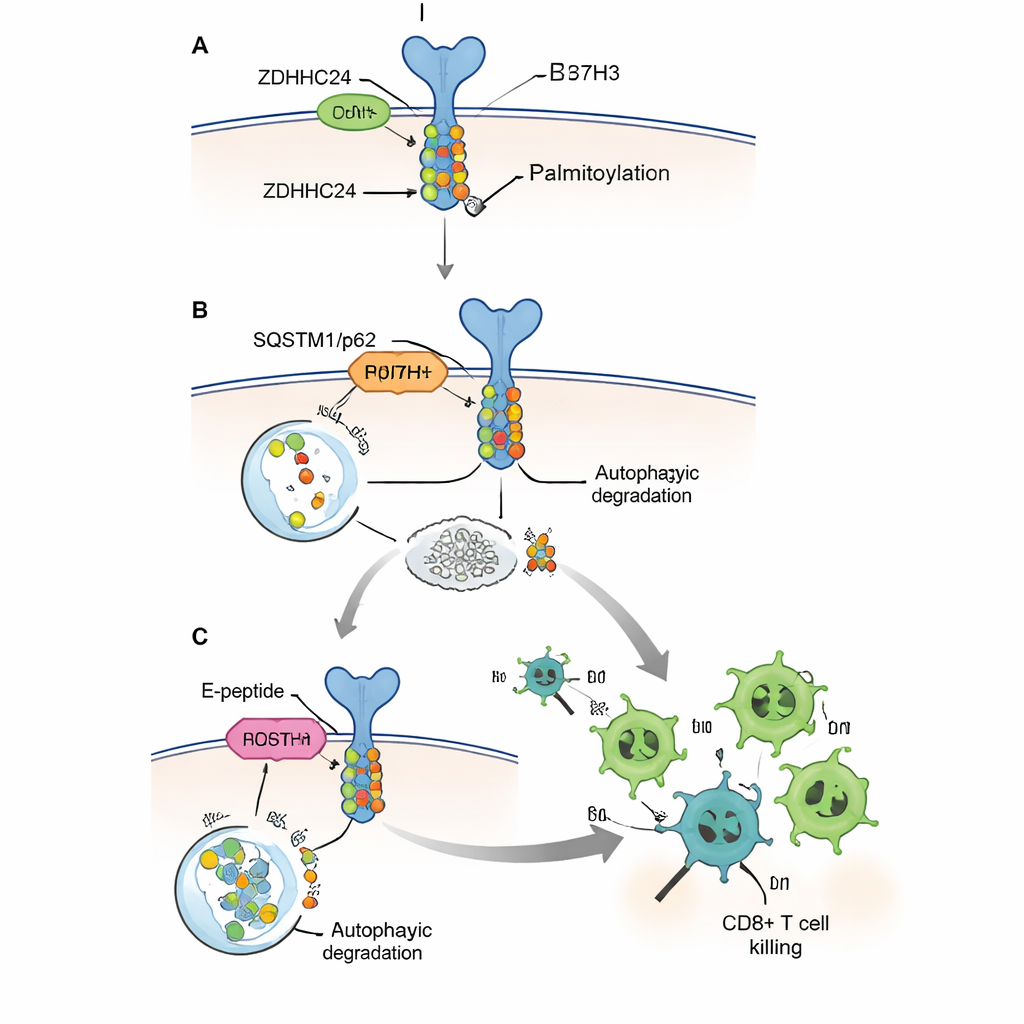
החלשת המגן והעצמת תאי T
מאחר שמחיקת ZDHHC24 או B7H3 באופן גנטי אינה טיפול מעשי בחולים, החוקרים תכננו פפטיד קצר בעל חדירות תאית שהם קוראים לו E‑peptide. הוא מחקה מקטע קטן של חלבון B7H3 שמקשר בדרך כלל ל‑ZDHHC24, ופועל כתכסיס שמונע מהאנזים למודיפ יק את מולקולות B7H3 האמיתיות. בתאים בתרבית, ה‑E‑peptide הפחית את פאלמיטואילציה ורמות החלבון של B7H3, השיב את זיהויו על ידי מכונת האוטופגיה, ואפשר לתאי CD8+ אנושיים להרוג תאי גידול ביעילות רבה יותר. במספר מודלים של עכברים, כולל עכבר האנושי שנושא תאים חיסוניים אנושיים וגידולי מעי אנושיים, הזרקות של E‑peptide הקטינו את הגידולים, הגדילו את כמות תאי CD8+ בתוכם, והגבירו את ייצור המולקולות הקוטלות המרכזיות כמו גרנזים B ואינטרפרון‑גאמא.
שותף חדש לאימונו‑תרפיה קיימת
לבסוף, החוקרים בדקו האם אסטרטגיה זו יכולה לפעול לצד חסימת PD‑1 הסטנדרטית. במודלים של סרטן המעי בעכברים, גם E‑peptide לבדו וגם נוגדן נוגד‑PD‑1 לבדו סיפקו שליטה מסוימת על הגידול. אך בשילוב, שני הטיפולים הניבו דיכוי גידולי חזק וארוך יותר, ובמקרים מסוימים גרמו להיעלמות גידולים והכפילו במעל לכך את התוחלת ההישרדות הממוצעת לעומת קבוצות הביקורת. ממצא זה מרמז ששבירת המגן של B7H3 על ידי חיתוך ה"עוגן" השומני שלה יכולה להשלים את תרופות הצ'קפוינט שמכוונות את מסלול PD‑1.
מה משמעות הדבר לטיפולי סרטן בעתיד
בקצרה, מחקר זה מראה שחומצת שומן תזונתית שכיחה, חומצה פאלמית, יכולה להיות מנוצלת על ידי גידולי מעי כדי להעניק שריון כימי לחלבון חוסם‑חיסון (B7H3) ולעזור לסרטן להסתתר. על‑ידי חסימת החיבור הכימי היחיד הזה, החוקרים הצליחו להסיר את השריון, לאפשר למערכות ההשמדה של התא להסיר את B7H3, ולפתוח שוב את הדרך לתאי CD8+ לתקוף. ה‑E‑peptide עצמו הוא כלי ניסיוני בשלבים מוקדמים, אך העבודה מזהה את פאלמיטואילציה של B7H3 — ואת האנזים ZDHHC24 — כיעדי תרופה מבטיחים. אם סוכנים דומים יוכחו כבטוחים ויעילים בבני אדם, ייתכן שיום אחד הם יהפכו עוד מקרי סרטן מעי הגס מ"קרים" שאינם מגיבים לאימונו‑תרפיה ל"חמים" שהמערכת החיסונית יכולה לזהות ולהשמיד.
ציטוט: Rao, Z., Huang, C., Wu, Q. et al. Palmitic acid-triggered B7H3 palmitoylation promotes immune escape. Nat Commun 17, 1810 (2026). https://doi.org/10.1038/s41467-026-68525-x
מילות מפתח: אימונו‑תרפיה בסרטן המעי הגס, צ'קפוינט B7H3, חילוף החומרים של חומצות שומן פלאמיטיות, פאלמיטואילציה של חלבונים, חיסון גידול על ידי תאי CD8