Clear Sky Science · he
תאי המאקרופאג'ים בדג זברה ממירים אותות פגיעה פיזית לדליפה מהירה בכלי דם
איך דג קטן מלמד אותנו על הנפיחות אחרי פציעה
כשאתה משפשף את הברך, האזור מהיר הופך לאדום, נפוח ודולף נוזלים. השינוי המהיר בכלי הדם הסמוכים חיוני להלחמה בזיהום ולהפעלת תהליכי תיקון, אך קשה היה לראות בזמן אמת כיצד הגוף חשה נזק ומגיבה בתוך שניות. באמצעות גוזלי דג זברה שקופים ודימות חי מתקדם, המחקר הזה חושף כיצד תאי חיסון מותאמים, המכסים כלי דם, ממירים את הזעזוע הפיזי של הפצע לדליפה כמעט מידית של כלי הדם — ומספק תובנה חדשה על דלקת, ריפוי ואפילו פגיעה ריאתית אצל בני אדם.
צפייה בהתפשטות הפגיעה בגוף
החוקרים עבדו עם דגי זברה צעירים, שגופם השקוף מאפשר לעקוב במיקרוסקופ אחר תאים וכלי דם בפעולה. הם חתכו את קצה סנפיר הזנב ומילאו את מחזור הדם בצבע זוהר שנשאר בתוך כלי דם בריאים. כאשר הדגים הפצועים הושבו למים מתוקים רגילים, כניסת המים לרקמות יצרה סביב הפצע "הלם אוסמוטי". בתוך דקות, כלי דם סמוכים התרחבו והחלו לדלוף את הצבע הפלואורסצנטי אל הרקמה הסמוכה, מחקה את הנפיחות והנזילה שמתרחשים סביב פצעים בבני אדם. על־ידי העברה בין מים רגילים ותמיסות מלח או סוכר מאוזנות במיוחד, הראו החוקרים כי פרמביליזציה מהירה זו של כלי הדם תלויה בעוצמה בשינויים אוסמוטיים ולא רק בקריעה הרקמתית הפשוטה.
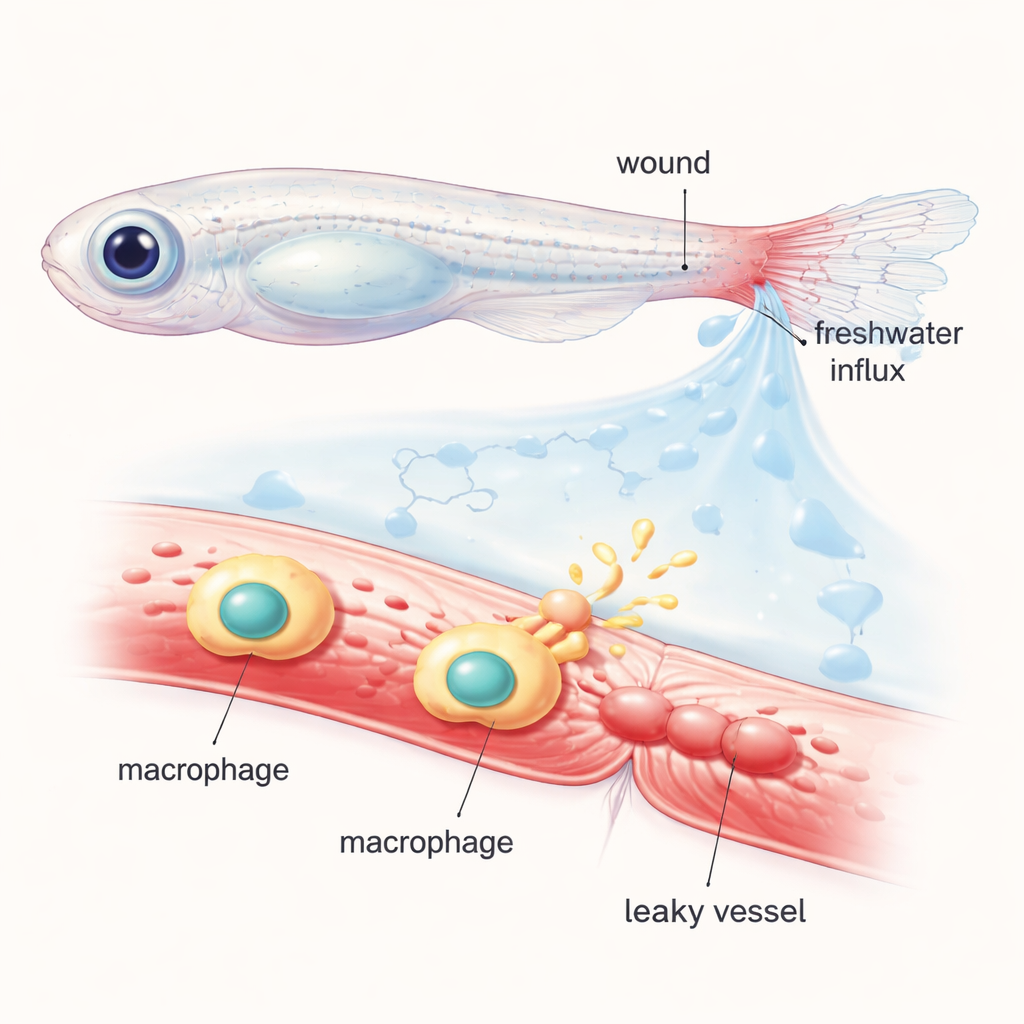
מעקב אחרי המוליכים הכימיים מאחורי הדליפה
כדי לגלות אילו מולקולות ממירות את הזעזוע הפיזי לאות דליפה, החוקרים בדקו משפחה של תרכובות שומניות הנקראות איקוסאנוידים, המיוצרות מחומצה ארכידונית. ליפידים אלה ידועים בתפקידם בדלקת ובזרימת הדם. באמצעות מוטנטים גנטיים ותרופות, נטרלו בררנית אנזימים פרטניים במסלול האיקוסאנוידים. חסימת אנזים מרכזי בשם Alox5a (5-ליפוקסיגנאז) או שותפו Lta4h הקטינה בחדות את כמות הצבע שברח מכלי הדם לאחר הלם אוסמוטי, מבלי לעצור את סגירת הפצע עצמה. לעומת זאת, הפרעה לאנזימים קשורים אחרים השפיעה במידה מועטה בלבד. ממצא זה מצביע על ענף ספציפי של מסלול הליפידים כגורם מרכזי בתגובה המהירה של הדליפה, שפועל כמעט כמו שסתום כימי שניתן לפתוח או לסגור על פי צורך.
תפקיד מפתיע של תאי חיסון היושבים על כלי הדם
בדם יש סוגים שונים של תאי חיסון, ובגוזלי דג זברה נויטרופילים ומאקרופאג'ים הם השחקנים הראשיים. הצוות השתמש במניפולציה גנטית מתוחכמת כדי להשמיד באופן בררני או את הנויטרופילים או את המאקרופאג'ים לפני הפציעה. הסרת נויטרופילים כמעט ולא שינתה את דליפת כלי הדם. אך כאשר המאקרופאג'ים הושמדו, תגובת הדליפה ירדה בכ־חצי, מה שהתאים להשפעת חסימת מסלול הליפידים Alox5a–Lta4h. חשוב לציין שהשינויים הללו לא עצרו את סגירת הפצע במהירות, מה שמעיד שניוד לויקוציטים ודליפת כלי דם יכולים להיות מבוקרים באופן חלקי בצורה עצמאית. זה חשף את המאקרופאג'ים הפרי-וסקולריים — מאקרופאג'ים היושבים צמודים מחוץ לכלי הדם — כמגשרים מרכזיים בין הפגיעה הפיזית להתנהגות הווסקולרית.
ממתיחה גרעינית לאות כימי
כיצד מאקרופאג'ים פרי-וסקולריים מזהים פצע שעשוי להיות מרוחק? התשובה טמונה באופן שבו גרעיניהם מגיבים ללחץ מכאני. כאשר ההלם האוסמוטי מהפצע משתרע ברקמה הסמוכה, כניסת מים גורמת לנפיחה תאית עדינה ולעיוות הגרעין. החוקרים תייגו אנזים מכנוסנסורי בשם cPla2 בסמן פלואורסצנטי והביעו אותו במיוחד במאקרופאג'ים. לאחר פציעה במים מתוקים רגילים, cPla2 עבר במהירות לפני השטח הפנימי של קרום הגרעין במאקרופאג'ים בגל ששוטף את הרקמה במהירות של כ־50 מיקרומטר לשנייה, בהתאמה להתפשטות המלחים המומסים. תהליך זה היה תלוי בתנאים היפוטוניים והיה חלש בהרבה בתמיסות איזוטוניות. מאקרופאג'ים סמוכים לכלי דם הראו דפוסי דופק חדים והפיכים של קשירת cPla2 לגרעין, אשר בתורו משחרר חומצה ארכידונית להמרה לליפידים שגורמים לדליפה.
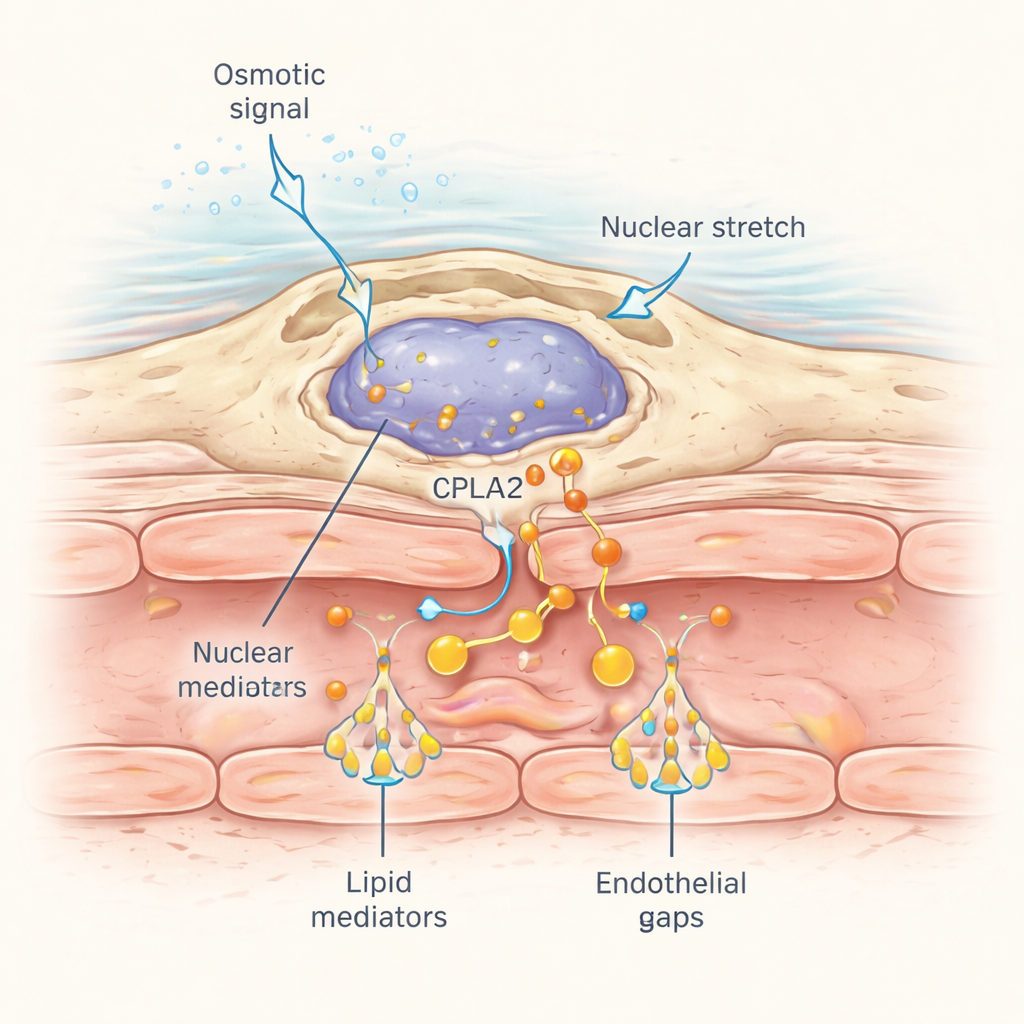
למה זה רלוונטי מעבר לדגים
במלים פשוטות, המחקר מראה כי מאקרופאג'ים מסוימים פועלים כשמירה פיזית: הם חשים את מתיחת הרקמה וממברנות הגרעין הנגרמת על־ידי שינויים אוסמוטיים בפצע, מפעילים את cPla2 על פני השטח הגרעיני ומהר מייצרים שליחים ליפידיים שמאשרים לכלי הדם הסמוכים "לפתוח את השערים" ולהתיר כניסת נוזלים וגורמי חיסון. למרות שדגי זברה חיים במים מתוקים ומתמודדים עם אתגרים אוסמוטיים ייחודיים, מסלולים מכנוסנסוריים דומים פועלים ככל הנראה ברקמות אנושיות הנחשפות לשינויים בלחצים וזרמים, כמו בריאות בזמן אשפוז במכשיר הנשמה מכנית. הבנת האופן שבו מתיחה גרעינית ואותות ליפידים שולטות בפרמביליות כלי הדם בזמן אמת עשויה בסופו של דבר להנחות טיפולים שיודעים לכוונן את הדלקת — או להפחית דליפה מזיקה במצבים כמו פגיעה ריאתית חריפה, או לחזק תגובות מועילות להאצת תיקון הרקמה.
ציטוט: Gelashvili, Z., Shen, Z., Ma, Y. et al. Zebrafish macrophages convert physical wound signals into rapid vascular permeabilization. Nat Commun 17, 1807 (2026). https://doi.org/10.1038/s41467-026-68520-2
מילות מפתח: החלמה מפציעה, כלי דם, מאקרופאג'ים, דלקת, דג זברה