Clear Sky Science · he
כוחות מכניים מהתרכבות עצמית של פפטידים בין‑תאיים מניעים היווצרות סְפֵרוֹאידים
בונים רקמות זעירות במעבדה
המדענים ממהרים ליצור גרסאות מזעריות של רקמות אנושיות שמתנהגות כמו המקור. מודלים חיים אלה יכולים להפוך ניסויים בתרופות נגד סרטן לבטוחים יותר ולהקרב טיפולים חדשים לסכרת ומחלות נוספות למציאות. המחקר הזה מציג שיטה אלגנטית לשכנע תאים להיווצר לקבצים תלת־ממדיים ריאליסטיים, כולל רשתות פרימיטיביות דמויות־כלי־דם שמשפרות אספקת חומרי מזון ותפקוד.
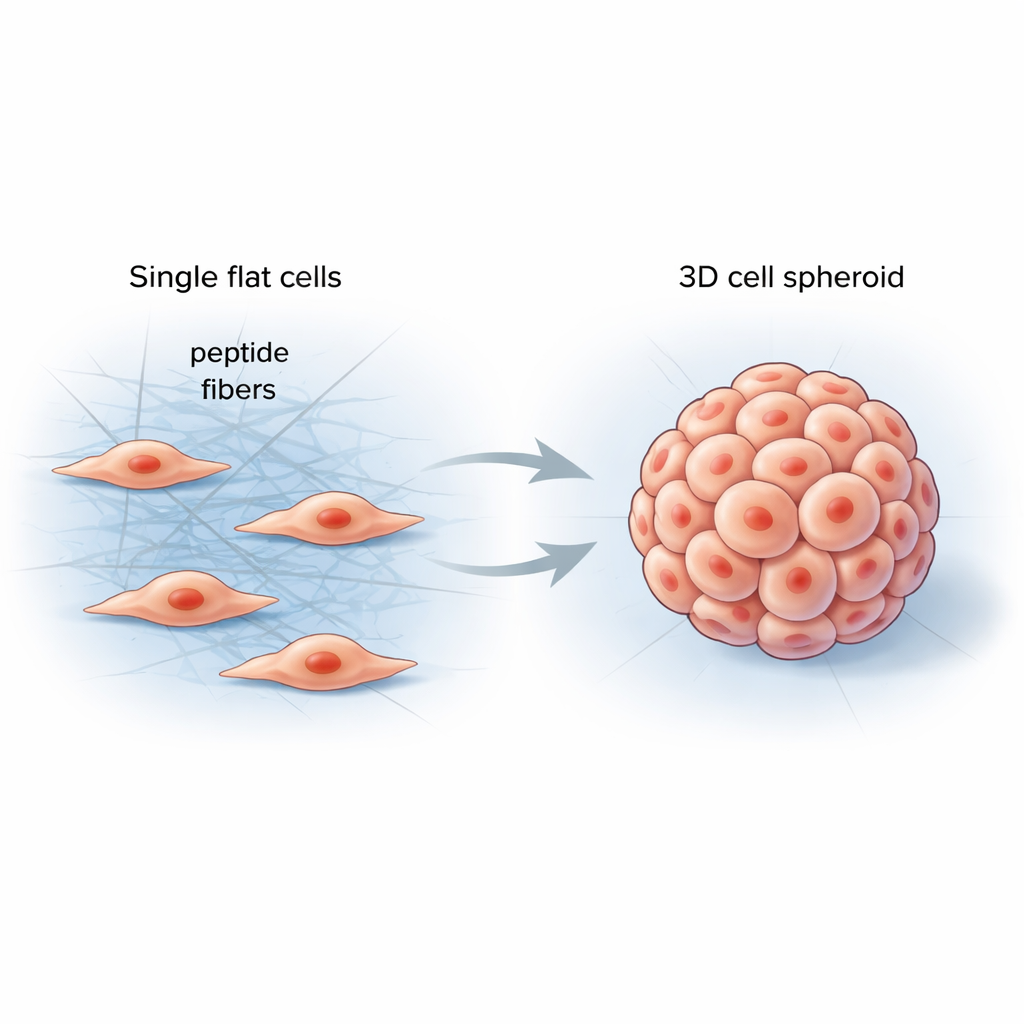
עוזרים לתאים ‘‘להרגיש’’ את סביבתם
בגופנו, התאים חיים בסביבה רכה אך מבנית הנקראת מטריצה חוץ־תאית — רשת של חלבונים התומכת ברקמות ושולחת אותות מכניים מתמידים לתאים. חומרים מקובלים במעבדה מתקשים לחקות את המורכבות הזו, ולרוב יוצרים שכבות תאים שטוחות שמתנהגות באופן שונה מאוד מאברים או גידולים אמיתיים. החוקרים חתרו לעצב חומר פשוט ותכנותי שיווצר ישירות בין תאים, יקשה את סביבתם בצורה מבוקרת וידחוף אותם לצורות תלת־ממדיות טבעיות יותר.
פפטידים חכמים שמתעצבים בין התאים
הצוות ייצר קטעי חלבון קצרים, פפטידים, היכולים לקשור זה את זה לסיבים ארוכים ודקים כשהם נתקלים באנזימים ספציפיים על משטחי התאים. כשמוסיפים את הפפטידים האלה לתאי סרטן, הם נשארים לא פעילים בתחילה, כמו תמיסה שקופה. ברגע שאנזימי התאים עצמם גוזרים חלק מהמולקולה, הפפטידים מתרכבים במהירות לרשת סיבית שעוטפת ובין התאים השכנים. רשת הסיבים החדשה שינתה את הכוחות המכניים המקומיים, עודדה את התאים למתוח זה את זה, לשנות את השלד התאים הפנימי ולהתכנס לספֵרוֹאידים עגולים תלת־ממדיים במקום להתפשט בשכבה.
מקבצי תאים לרשתות דמויות־כלי־דם
כדי להתקרב לרקמה אמיתית, המדענים הוסיפו תאי אנדותל אנושיים — הסוג שמצפה בדרך כלל כלי־דם — יחד עם פפטיד שני הנושא "תג כתובת" קטן שמושך תאים אלה. יחד יצרו הפפטידים המקורי והממוש-mod פלטפורמת ננו־סיבים משותפת. תאי האנדותל השתמשו בפלטפורמה זו כדי לנבוט לתוספים בצורת צינור שעטפו וחדרו את הספֵרוֹאידים, ויצרו מבנים דמויי קפילרות. כאשר הצוות זרם מולקולות סוכר זוהרות סביב מבנים אלה, נרשמה חדירה עמוקה יותר הרבה יותר לגרעין הספֵרוֹאיד לעומת ספֵרוֹאידים חסרי הצינורות הפנימיים — עדות לכך שהמעבר של מזון ואותות השתפר באופן ניכר.
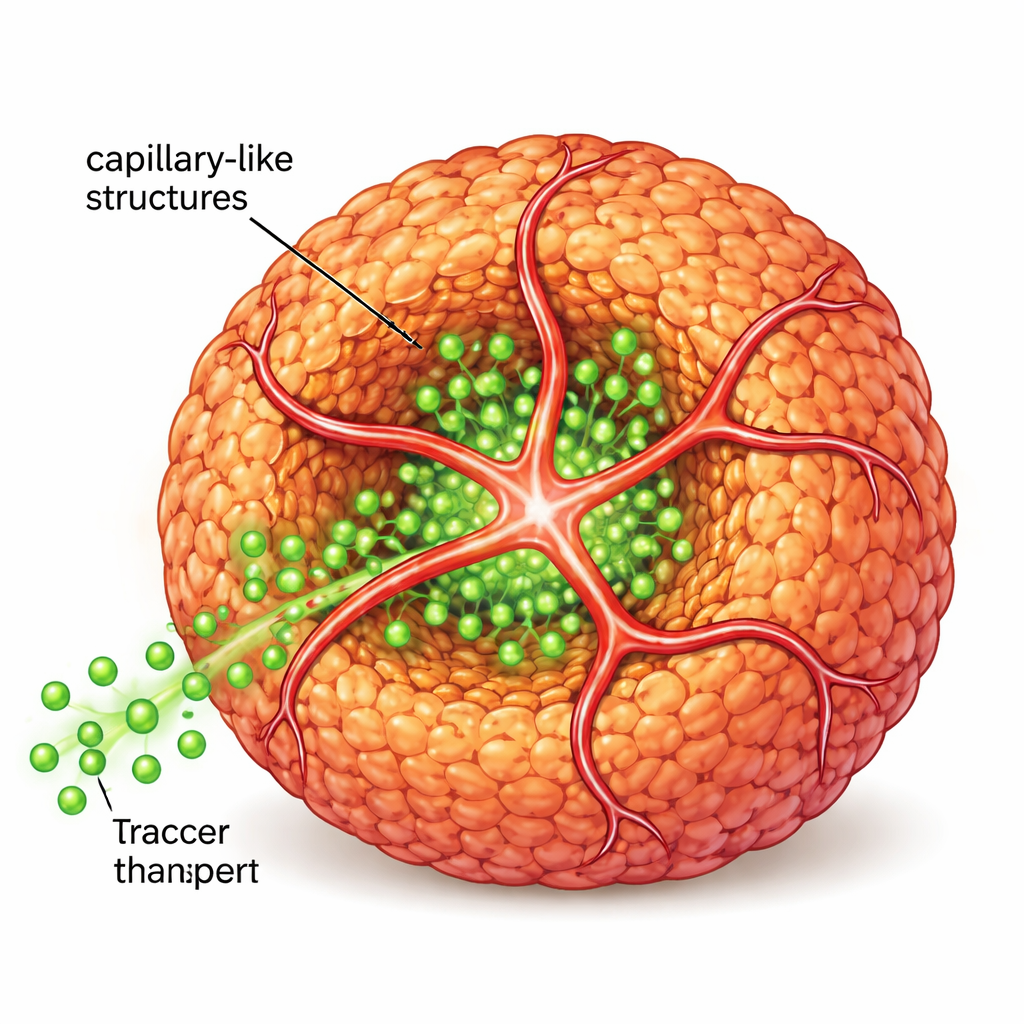
קרוב יותר לגידולים אמיתיים ולאי־לבלב פעילים
פרופיל פעילות גנטית חשף שספֵרוֹאידים של גידול עם מבני דמויי כלי־דם דמו יותר לדגימות גליאובלסטומה של חולים מאשר תרביות שטוחות מסורתיות או ספֵרוֹאידים ללא כלי־דם. בעכברים, ספֵרוֹאידים שהכילו רשתות כלי־דם פרימיטיביות גדלו לגידולים גדולים ומאובזרים יותר בכלי־דם, מה שמעיד שהמודל החוץ־גופי תופס תכונות מפתח של התנהגות גידול אמיתי. אותה אסטרטגיה יושמה גם על תאי בטא של הלבלב, הנמצאים בדרך כלל באיים עשירים בכלי־דם ומפרישים אינסולין בתגובה לגלוקוז. כאשר ספֵרוֹאידים של תאי בטא צוידו במבני דמויי־קפילרות באמצעות מערכת הפפטידים ותאי האנדותל, הם הראו שחרור אינסולין חזק ומכוון יותר, דבר המעיד על כלי עוצמתי למחקר סוכרת ורפואה מתחדשת.
מדוע זה חשוב לטיפולים בעתיד
על‑ידי מתן אפשרות לפפטידים פשוטים להתארגן בעצמם בין תאים חיים, עבודה זו מציעה נוסחה כללית לבניית רקמות מזעריות ומאווררות שמרגישות ומתפקדות יותר כמו אלה שבגוף. הספֵרוֹאידים התוצאה משקפים טוב יותר גידולים של חולים ואיים פעילים, מה שהופך אותם ליקרים לניסויי תרופות, חקירת מנגנוני מחלה ועיצוב טיפולים מבוססי תאים. עבור קהל לא‑מומחה, המסקנה המרכזית היא שלהעניק לתאים שגדלו במעבדה "תחושה נכונה" ורשתות צינוריות זעירות יכול לשפר באופן דרמטי עד כמה הם מחקים נאמנה רקמות אנושיות, ואולי לזרז את הדרך ממחקר בסיסי לטיפולים יעילים.
ציטוט: Lu, H., Li, Y., Yang, X. et al. Mechanical forces from intercellular peptide self-assembly drive spheroid formation. Nat Commun 17, 1801 (2026). https://doi.org/10.1038/s41467-026-68513-1
מילות מפתח: הנדסת רקמות, דגמי סרטן, אנגיוגנזה, אורגאואידים, התרכבות עצמית של פפטידים