Clear Sky Science · he
צום לסירוגין מעכב גליאומה מונחת Tp53 דרך ויסות מתיונין‑m6A בתיווך המיקרוביוטה המעי
מדוע לתת למעיים הפסקה עשוי להאט גידולים קטלניים במוח
גליובלסטומה היא אחד הסרטנים האגרסיביים ביותר במוח, והטיפולים הקיימים—כירורגיה, קרינה וכימותרפיה—רובם מעניקים למטופלים רק זמן נוסף מוגבל. המחקר שואל שאלה פשוטה אך בעלת משמעות רחבה לחיי היומיום: האם הדרך שבה אנו אוכלים, ובמיוחד צום לסירוגין, יכולה לשנות את חיידקי המעי וכימיה בדם בצורה שמאטה במידה משמעותית סוגים מסוימים של גידולים במוח?
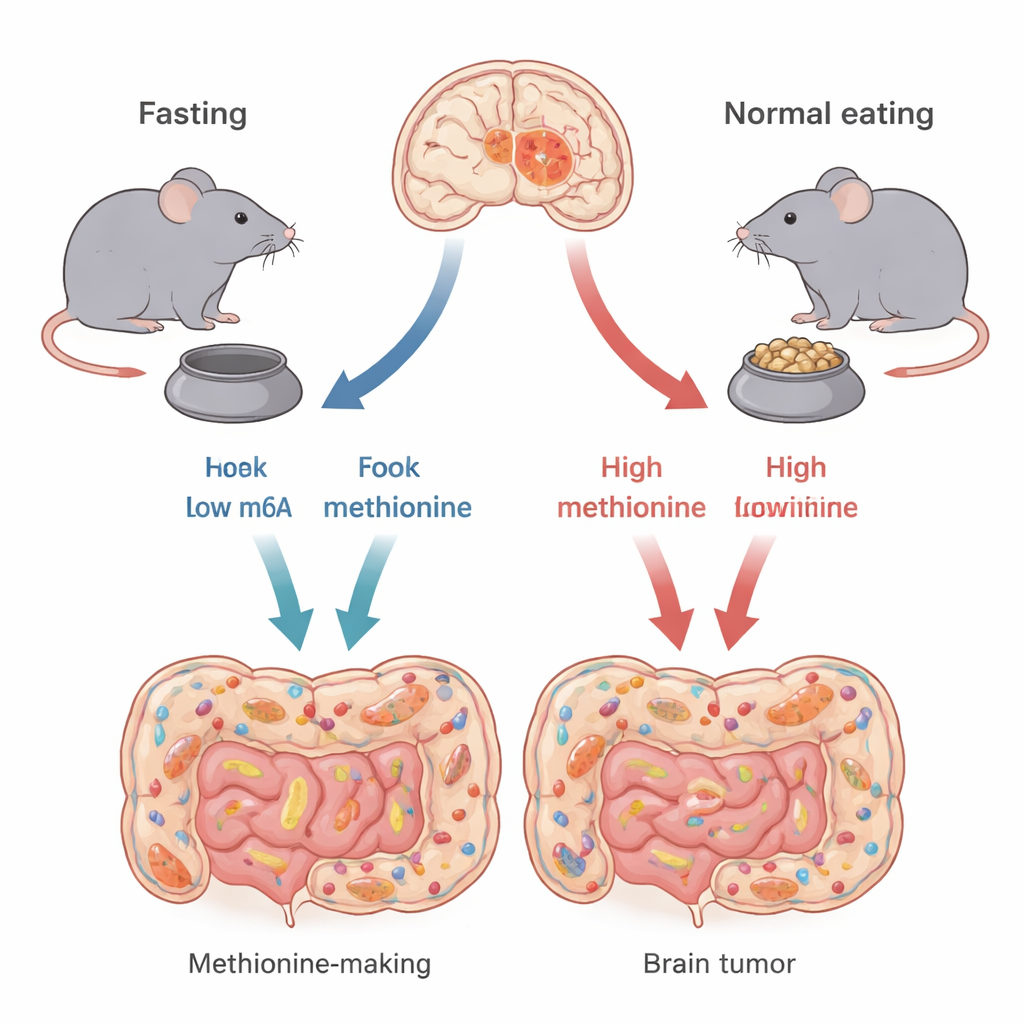
סוגים שונים של אותו סרטן מוח
לא כל גליובלסטומה זהה. המחברים מתמקדים בשני סוגים גנטיים עיקריים, המוגדרים על‑ידי שינויים בגנים הנקראים TP53 ו‑CDKN2A. גנים אלה מסייעים לשלוט באיך תאים גדלים או מתים. באמצעות מודלים של עכברים המדמים היטב כל תת‑סוג אנושי, החוקרים מצאו כי צום לסירוגין—24 שעות ללא אוכל ואחריהן 24 שעות עם אוכל—אינו מועיל לכל הגידולים באותה מידה. עכברים עם גידולים מסוג TP53 חיו זמן רב יותר והגידולים שלהם היו קטנים יותר בזמן הצום, בעוד שעכברים עם גידולים מסוג CDKN2A הראו מעט תועלת. ממצא זה מרמז כי היעילות של הצום תלויה במידה רבה בתצורת החיווט הגנטית של הגידול.
מהדפוס התזונתי ועד חיידקי המעי ולכימיה במוח
הצוות חקר כיצד הצום מפעיל את האפקט הסלקטיבי הזה. מכיוון שכמות המזון הכוללת נשמרה שווה בין הקבוצות, ההבדל המרכזי היה בזמני האכילה. זמני האכילה הללו שינו באופן חזק את המיקרוביום המעי—הקהילה הגדולה של חיידקים במעי. בעכברי TP53 בצום, קבוצות חיידקים שמייצרות ביעילות את חומצת האמינו מתיונין, כגון זנים מסוימים של Alistipes ו‑Prevotella, פחתו בשפען. מכיוון שמתיונין הוא אבני בניין חיונית שחיות חייבות לקבל מהתזונה או מהמיקרוביום, השינוי המיקרוביאלי הזה הוביל לפחות מתיונין שזורם מהמעי אל זרם הדם ולבסוף אל המוח.
כיצד גורם מזון יחיד מכוונן אותות שמניעות את הסרטן
מתיונין הוא לא רק חומר מזון; הוא גם חומר גלם ליצירת S‑adenosylmethionine (SAM), התורם המתיל האוניברסלי של התא. SAM מזין תהליך כימי של תיוג RNA הנקרא m6A. תגיות אלה עוזרות לשלוט בעוצמת הביטוי של גנים מסוימים. במודל הגידול TP53, הצום הוריד את רמות המתיונין ו‑SAM בדם ובאזורים מוחיים של הגידול. באמצעות שכבות טכנולוגיות ’אומיקס‘—ריצוף RNA סטנדרטי, פרופילינג של RNA בתא יחיד ומפות מרחביות של פעילות גנים ומטבוליטים—החוקרים מצאו פחות תגיות m6A על RNAים המקושרים לסרטן תחת מצב הצום. מטרה חשובה אחת הייתה TGFB2, גן במסלול האיתות TGF‑β, הידוע כמעודד גדילה וחדירה של גידולים. בצום, האנזים METTL3 (שכונס m6A) ו‑TGFB2 שניהם ירדו, ואיתות TGF‑β התחלש.
הוכחת סיבה ותוצאה באמצעות התערבויות ממוקדות
כדי לצאת מהקורלציה, המדענים ערכו ניסויי ״הצלה״. הם חסמו את METTL3 בעזרת תרופה, או העבירו חיידקי מעי מעכברים בצום לעכברים שאכלו כרגיל, וראו שהגידול האט לגדול גם בלי צום—תמיכה ברעיון שגם המיקרוביום וגם מכניזם ה‑m6A הם שחקנים מרכזיים. לעומת זאת, כאשר עכברים בצום קיבלו מתיונין נוסף או טופלו בתרופה שמגבירה תגיות m6A, גידוליהם גדלו בדומה לאלה של עכברים שאכלו כרגיל, והיתרון בהישרדות נעלם. חשוב לציין כי שיבוש חיידקי המעי בעזרת אנטיביוטיקה רחבת‑טווח המקפּא המון מהשינויים הקשורים לצום, מה שמדגיש שהקהילה המיקרוביאלית במעי היא צומת מרכזית בשרשרת האירועים הזו.
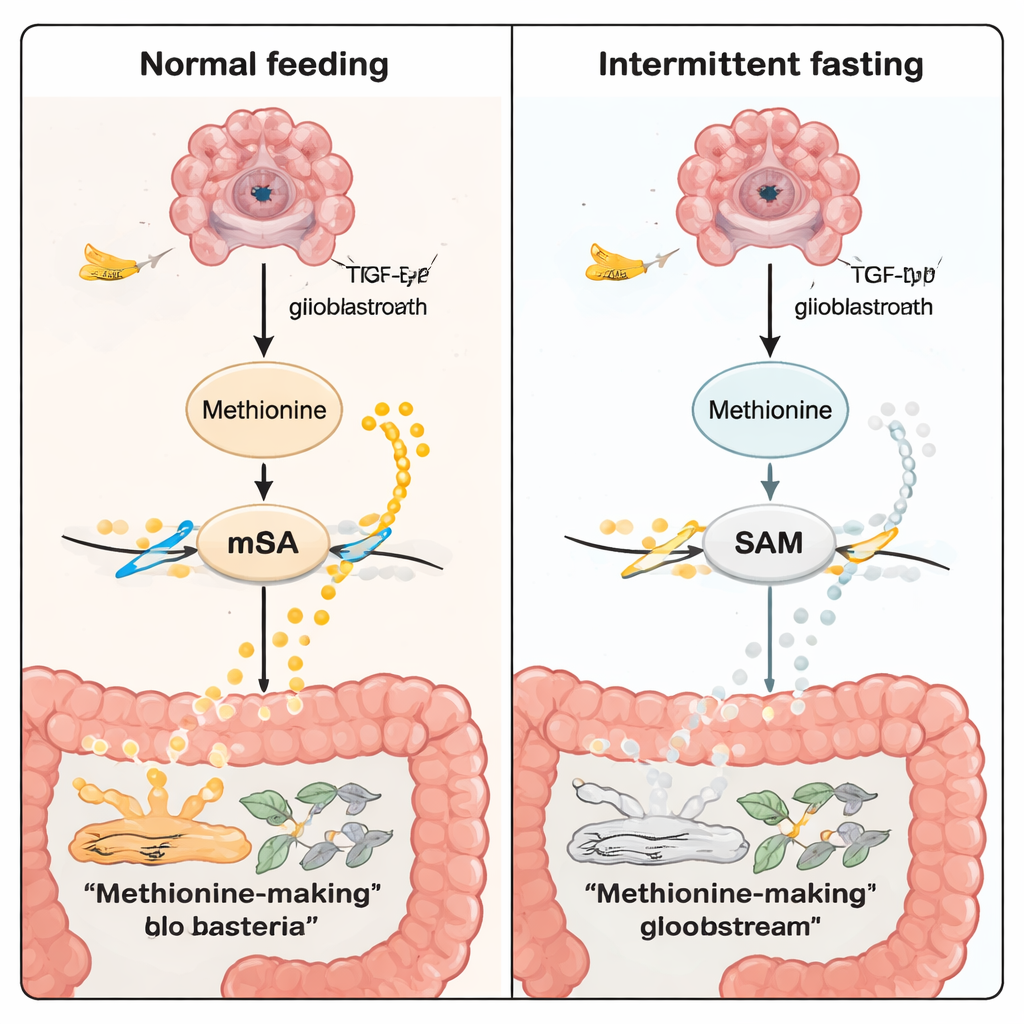
מה משמעות הדבר לבני אדם ולטיפולים עתידיים
עבור הקורא הרחב, המסר המרכזי הוא שלא כל סרטנים, ואפילו לא כל גליובלסטומות, יגיבו אותו הדבר לאסטרטגיה תזונתית כמו צום לסירוגין. בגידולי TP53, נראה שהצום ״מדבר״ עם המוח דרך המעי: הוא משנה את חיידקי המעי, מה שמפחית את ייצור המתיונין, מוריד את תיוג ה‑RNA הכימי ומבלם אותות עוצמתיים של גדילה בתוך תאי הגידול. אמנם העבודה נערכה בעכברים ודורשת תרגום קליני זהיר, אך היא מצביעה על עתיד שבו דפוסי חיים פשוטים, טיפולים מבוססי מיקרוביוטה של המעי ותרופות המכוונות את מסלולי המתיונין או ה‑m6A יוכלו להיות מותאמים לתת‑הסוג הגנטי של גידול המטופל.
ציטוט: Lin, Y., Li, S., Xu, X. et al. Intermittent fasting inhibits Tp53-driven glioma through gut microbiota-mediated methionine-m6A regulation. Nat Commun 17, 1804 (2026). https://doi.org/10.1038/s41467-026-68512-2
מילות מפתח: צום לסירוגין, גליובלסטומה, מיקרוביום המעי, מטבוליזם מתיונין, שינויי RNA מסוג m6A