Clear Sky Science · he
TET1 כרגולטור מרכזי השולט על משמרות הפרו-פרוסטוזיס התלויה והלא תלויה ב-GPX4 בלוקמיה מיאלואידית חריפה
מדוע המחקר הזה חשוב לטיפול בסרטן
תרופות סרטניות רבות חדשות מנסות לדחוף תאים ממאירים למצב השמדה עצמית הנקרא פרורפטוזיס, סוג של מוות תאי מונע על ידי ברזל ונזק לשומנים. עם זאת, חלק מהגידולים מתעקשים להתנגד לגישה זו. המחקר הזה חושף כיצד חלבון שמשנה את ה-DNA בשם TET1 מסייע לתאי לוקמיה להתחמק מפרורפטוזיס באמצעות שתי מערכות הגנה ביוכימיות נפרדות — ומראה כי חסימת ההגנות האלה יכולה להפוך גם סרטן עמיד לפגיע.
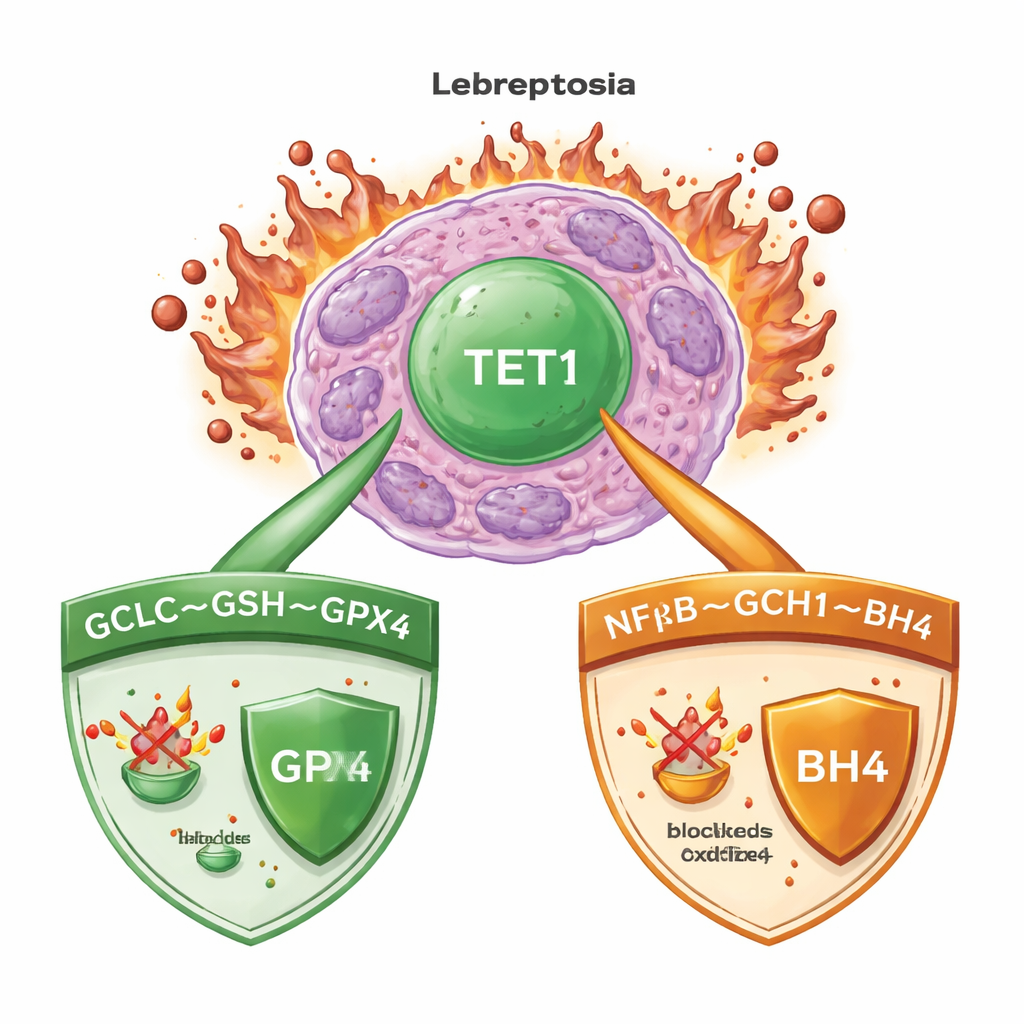
תערובת קטלנית של ברזל ושומנים פגומים
פרורפטוזיס מתרחש כאשר ברזל מסייע בחמצון בלתי מבוקר של שומנים בממברנות התאים, מה שמוביל בסופו של דבר לקריעת התאים. בלוקמיה מיאלואידית חריפה (AML), כמו ברבים מסוגי הסרטן, תאים מפעילים מערכות משמר חזקות כדי לשמור על תהליך זה תחת שליטה. שומר מפתח אחד הוא האנזים GPX4, שמשתמש במולקולה קטנה בשם גלוטתיון כדי לנטרל פרוקסידים שומניים מזיקים. מערכות גיבוי נוספות מייצרות מולקולות נוגדות חמצון היכולות ללכוד רדיקלים מסוכנים גם כאשר GPX4 מוחלש. הבנת איזה מתגים ראשיים מתאמים את ההגנות האלה קריטית לתכנון טיפולים שמפעילים פרורפטוזיס באופן אמין בתאי סרטן תוך שמירה על רקמות בריאות.
TET1 בולט כמרכז שליטה מרכזי
החוקרים השוו עשרות דגימות תאים סרטניים, כולל שורות רבות של AML ותאים שמקורם בחולים, ושימו לב לדפוס ברור: תאים שהתנגדו לפרורפטוזיס הפגינו רמות גבוהות של TET1, אנזים שמשנה סימני כימיים על ה-DNA ומשפיע על פעילות גנים. כאשר הורידו את רמות TET1 באמצעות כלים גנטיים או עיכבו את פעילותו מולקולרית, התאים הסרטניים הפכו רגישים בהרבה לתרופות שמפעילות פרורפטוזיס. התופעה הופיעה גם במבחנות מעבדה וגם במודלים של עכברים ל-AML. להיפך, הגדלת ביטוי TET1 הגנה על התאים מפני מוות פרורפטוטי והגבילה את הצטברות המולקולות החמצוניות-פעילות (ROS), תוצרי לוואי כימיים שתוקפים את הממברנה.
חיזוק המגן הנוגד חמצון העיקרי
בחקירה מעמיקה יותר, הצוות מיפה היכן TET1 פועל על הגנום ומצא שהוא מפעיל ישירות גן בשם GCLC. GCLC מקודד אנזים חיוני שמשגר את ייצור הגלוטתיון, הדלק של GPX4. על ידי הגדלת סימן DNA ספציפי (5-הידרוקסימתילציטוזין) באזור הפרומוטר של GCLC, TET1 מעלה את סינתזת הגלוטתיון. בתנאי תזונה תקינים זה מגדיל את מאגר נוגדי החמצון המרכזי של התא. בתנאי רעב ל-cystine, אותו קומפלקס אנזימטי גם מייצר פפטידים γ-גלוטמיל יוצאי דופן שעוזרים לקלוט עודף גלוטמט — דרך נוספת לטשטש פרורפטוזיס. הן בתרביות תאים והן בעכברים, אובדן TET1 או עיכוב פרמקולוגי של סינתזת גלוטתיון הורידו במידה חדה את רמות הגלוטתיון והפפטידים המגנים הללו, והפכו תאי לוקמיה לפגיעים הרבה יותר למפעילי פרורפטוזיס.
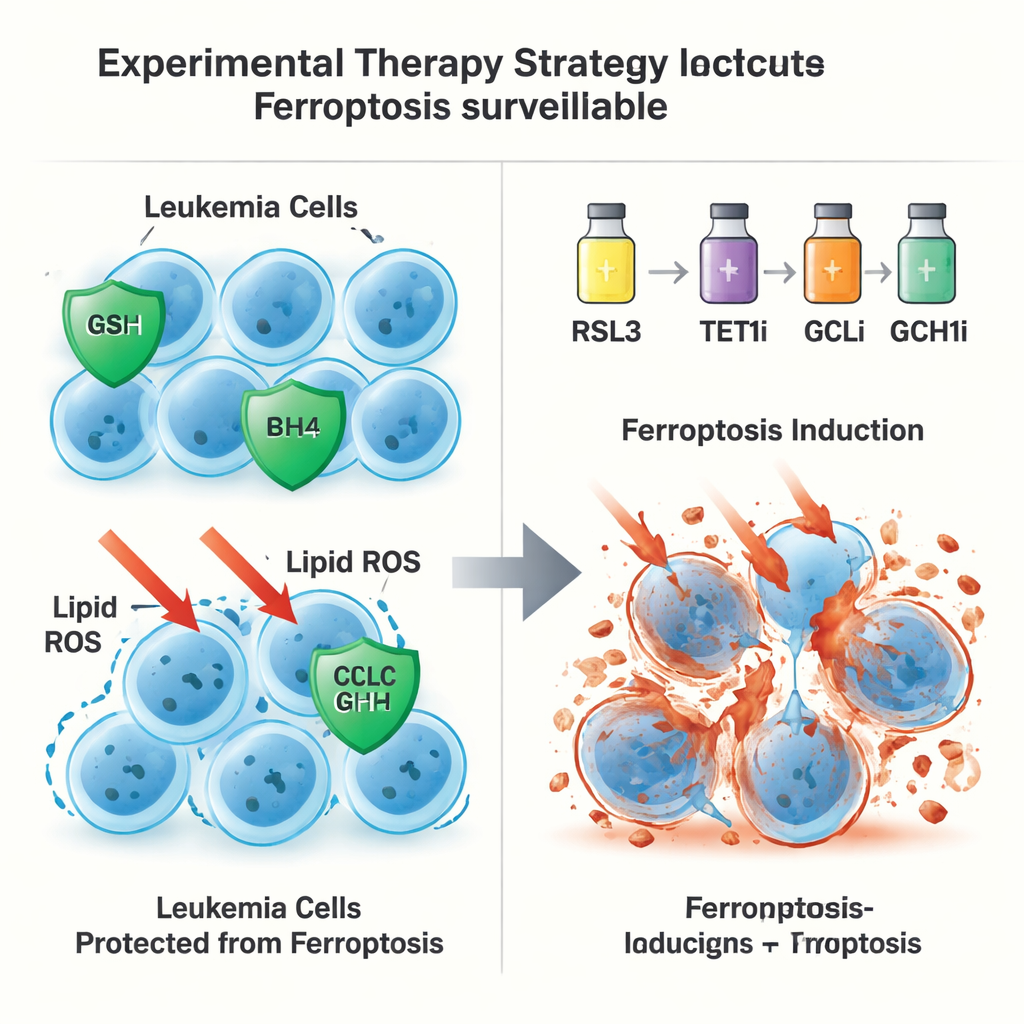
נתיב אדיש ל-GPX4 כדרך בריחה שנייה
באופן מפתיע, תפקיד ההגנה של TET1 לא הסתיים בציר הגלוטתיון–GPX4. גם כאשר GPX4 הוסר מתאי לוקמיה, רמות נוספות של TET1 יכלו עדיין למנוע מוות פרורפטוטי, מה שהצביע על קו הגנה שני. המחברים עקבו והציגו כי זה נובע מהפעלה על ידי TET1 של מסלול איתות NFκB, ובפרט מרכיב שנקרא NFKB2. זה, בתורו, מגביר את הביטוי של GCH1, אנזים שמייצר את מולקולת הנוגדת חמצון BH4. BH4 יכולה להגן על ליפידים מממברנת החלקה מפני חמצון ללא תלות ב-GPX4. כאשר GCH1 השתקע גנטית או נחסם כימית, יכולתו של TET1 להגן על התאים מפני פרורפטוזיס נפגעה חלקית. יחד, ממצאים אלה מגדירים את מסלול TET1–NFKB2–GCH1 שיוצר מערכת משמרת לפרורפטוזיס שאינה תלוייה ב-GPX4.
לנצל חולשה להזדמנות טיפולית
עם מפה זו של שני הנתיבים, החוקרים בחנו האם דחיפה סימולטנית של פרורפטוזיס והחלשת ההגנות הנשלטות על ידי TET1 עשויות לספק יתרון טיפולי. במודלים של עכברים עם AML ובשתלי לוקמיה שמקורם בחולים בתוך עכברים, מינונים נמוכים של תרופה שמפעילה פרורפטוזיס בשילוב עם מעכבים של TET1, סינתזת GSH (דרך GCLC), או GCH1 הפחיתו באופן דרמטי את העומס הסרטני, האריכו את ההישרדות ורוקנו את אוכלוסיות התאים שיזמו את הלוקמיה. חשוב לציין כי המפעיל של הפרורפטוזיס שימש במינון שהוא חלק מהמינונים שתוארו במחקרים קודמים, מה שמפחית דאגות לגבי רעילות לתאי גזע דם נורמליים.
מה זה אומר לטיפולים עתידיים בסרטן
ללא מומחיות, המסר המרכזי הוא שתאי לוקמיה שורדים על ידי הפעלה של שתי מערכות מגן נוגדות חמצון חופפות, שתיהן מתואמות על ידי TET1: אחת מתמקדת בגלוטתיון וב-GPX4, והשנייה מבוססת על GCH1 ו-BH4. עבודה זו מראה כי על ידי הפעלת פרורפטוזיס במידה מתונה ובמקביל חסימת TET1 ושותפיו המורידים, יתאפשר פעם אחת לגרש עמידות ולדחוף תאי סרטן מעבר לקצה באופן סלקטיבי, מבלי להציף רקמות בריאות. אם כי אסטרטגיות אלה עדיין לא מוכנות לשימוש קליני, המחקר מזהה את TET1 כנקודת בקרה חזקה ומטרה מבטיחה לטיפולים משולבים ב-AML ובאולי בסוגי סרטן קשים נוספים.
ציטוט: Yang, L., Lu, J., Yun, W. et al. TET1 as a master regulator controlling GPX4-dependent and -independent ferroptosis surveillance in acute myeloid leukemia. Nat Commun 17, 1800 (2026). https://doi.org/10.1038/s41467-026-68509-x
מילות מפתח: פרורפטוזיס, לוקמיה מיאלואידית חריפה, TET1, גלוטתיון, אפיגנטיקה של סרטן