Clear Sky Science · he
תא מלאכותי המסוגל להעברת אותות בתיווך ADRB2 לצורך ויסות גליקוגנוליזה
ללמד בועיות קטנטנות לדבר
דמיינו בועת סבון מיקרוסקופית שיכולה לחוש אות דמוי‑הורמון מחוץ לה ואז "להחליט" לשרוף דלק מאוחסן בתוכה, בדומה לתא אנושי אמיתי. המחקר הזה בונה במדויק סוג כזה של תא מלאכותי, ומראה כיצד דמויי‑תא מלאכותיים שיוצרו בידי אדם יכולים לקבל מסר כימי ולהפכו לכימיה מבוקרת הקשורה לאנרגיה. עבודה כזו מקרבת אותנו לנושאים כמו נשאי תרופות חכמים, רקמות שיצרנו במעבדה וצורות חיים סינתטיות פשוטות שיכולות להגיב לסביבתן.
לבנות תא מהחוץ פנימה
תאים אמיתיים מאזנים את סביבתם כל הזמן דרך קולטנים בממברנה החיצונית שלהם. המחברים ביקשו להעתיק אחת מהנתיבים הטבעיים האלה באמצעות רכיבים מזוקקים ובועות שומניות פשוטות הנקראות וניקולות ענקיות. הם התמקדו בקולטן אנושי שכיח, קולטן β2‑אדרנרגי (ADRB2), שבעמנו מסייע לשלוט בקצב הלב, בפונקציית הריאות ובשימוש בדלק. כאשר קולטן זה פוגש תרופה כמו איזופרוטנול (ISO), הוא בדרך כלל מפעיל שרשרת פנימית שיוצרת מולקולת שליח בשם cAMP, אשר בתורה שולטת בדרך שבה תאים מפרקים גליקוגן — צורת האחסון של גלוקוז בגוף. שיכפול כל הרצף הזה בתא מלאכותי לא הושג קודם לכן.
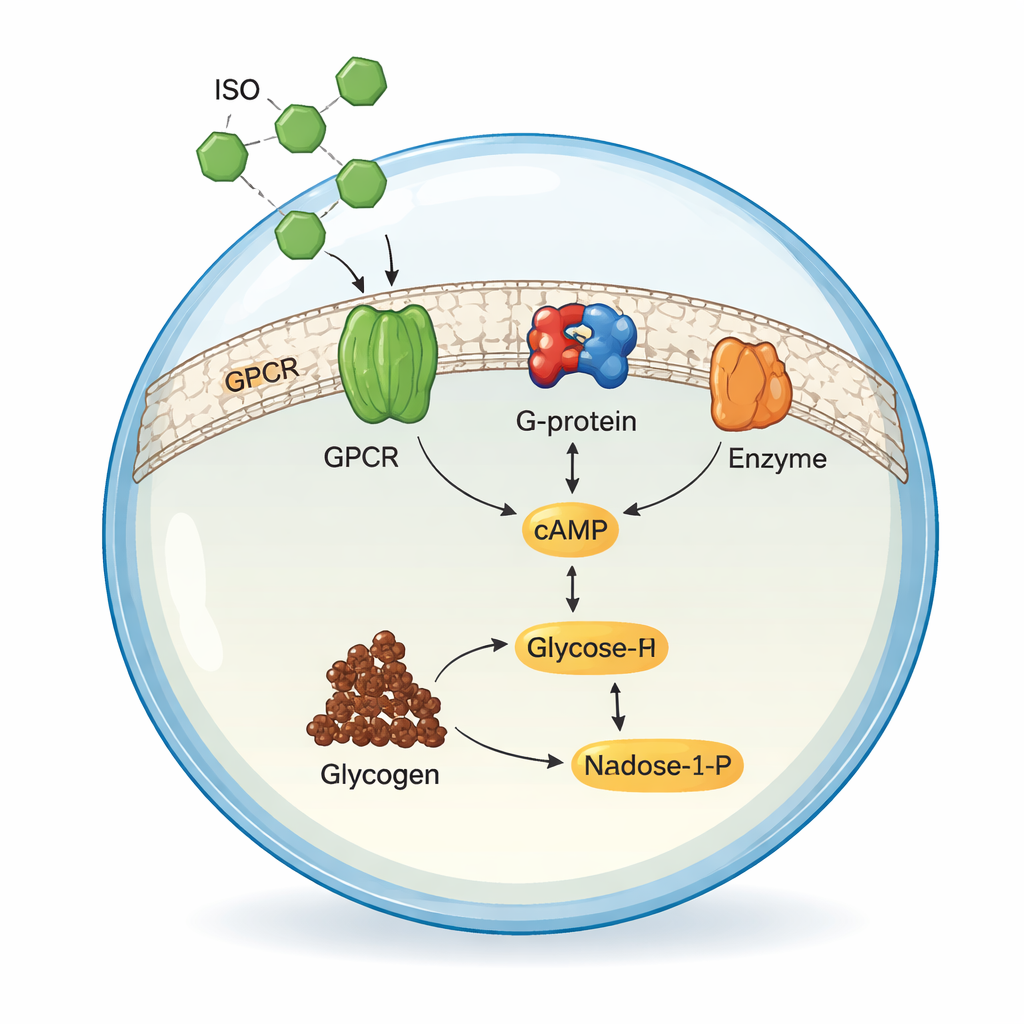
להשחזר את שידור האות הראשוני
הצוות קודם לכן שחזר את שלבי ההתחלה של נתיב ההעברה בתמיסה, מחוץ לכל ממברנה. הם הפיקו שלושה חלבונים אנושיים בתאי חרקים: ADRB2, תת‑יחידת חלבון‑G שותפה (Gsα), ואנזים בשם אדנילט ציקלז V (ADCY5), שמייצר cAMP מ‑ATP. כאשר ערבבו את הרכיבים האלה עם ISO בתנאים מכוונים בקפידה, הפעלת הקולטן האדרנרגי הובילה ל־ADCY5 שהפך ATP ל‑cAMP. על ידי מדידת cAMP בעזרת כרומטוגרפיה נוזלית בעלת ביצועים גבוהים, החוקרים אופטימיזו pH, טמפרטורה ורמות מגנזיום ומצאו שהמערכת המשוחזרת שלהם עבדה ביעילות זהה או טובה מזו של הכנות קודמות רבות, ובכך אישרו שהכימיה הליבה של ההעברה נמצאת במקום הנכון.
להתקין קולטנים אמיתיים בממברנות מלאכותיות
בהמשך, המחברים טמענו את שלושת החלבונים בממברנות של וניקולות חד‑שכבתיות ענקיות — בועות ליפיד בגודל תא המשמשות כשלדה לתאים מלאכותיים. הם תייגו בפלואורופור את ADRB2 ואת ADCY5 כדי לוודא שהחלבונים ישבו בממברנה, נעים בחופשיות ונמצאים במספרים גדולים, עם כ‑1.8 מיליון קולטנים לכל וניקולה בקירוב. טיפול אנזימטי הראה שיותר מ‑94% מהקולטנים פנו בכיוון הנכון, עם אתרי הקשירה החשופים כלפי חוץ. גלאי GTP פלואורוסצנטי אישר שקישור ISO בממברנה באמת הפעיל חלבוני G בתוך הוניקולות. משמעות הדבר היא שהתאים המלאכותיים יכלו, בעקרון, להעביר אות ISO חיצוני דרך ממברנתם בדיוק כפי שתאים טבעיים עושים.
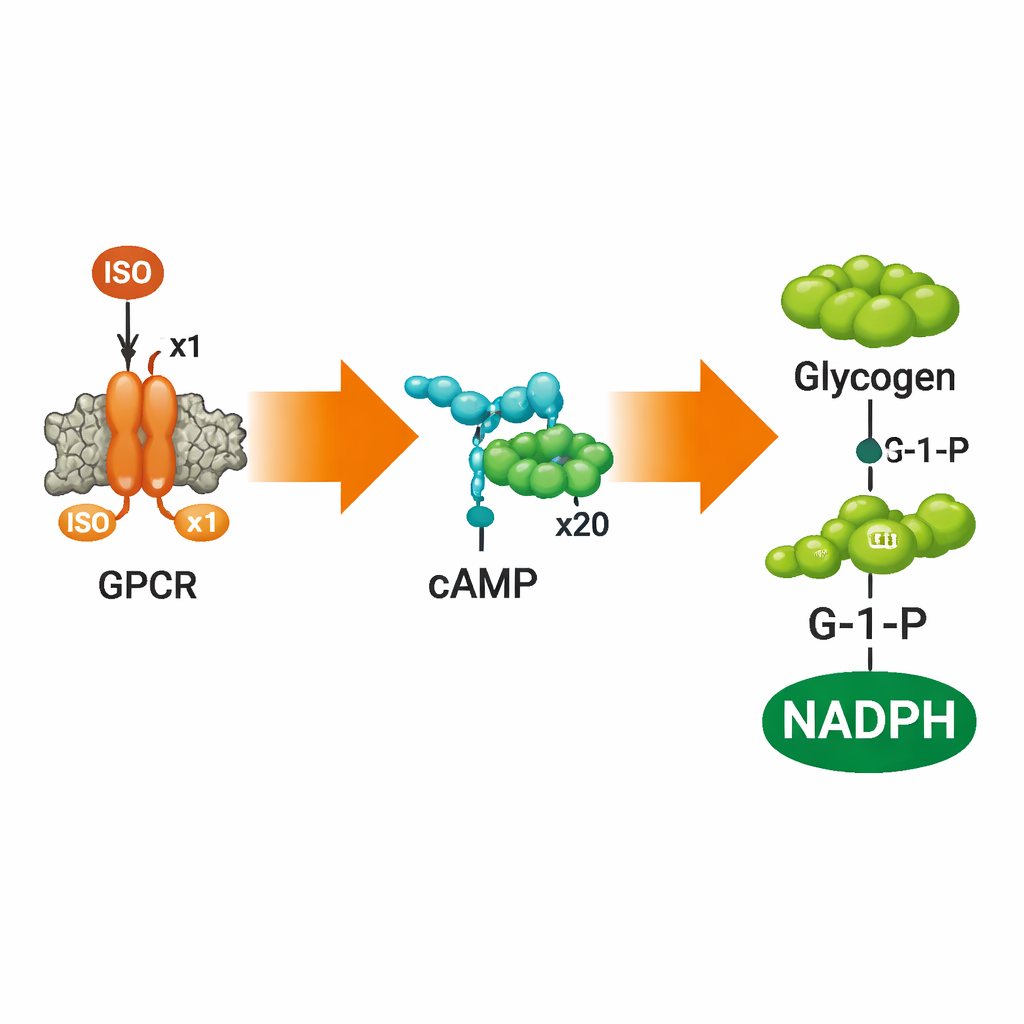
להפוך אות לפירוק דלק
כדי לבדוק האם תאים סינתטיים אלה יכולים לעשות משהו שימושי עם האות, הצוות הוסיף חיישן ל‑cAMP ואז מסלול מלא של פירוק גליקוגן בתוך הוניקולות. באמצעות חיישן cAMP מבוסס FRET, הם הראו שהוספת ISO מחוץ לוניקולות גרמה לעלייה ברמות cAMP מבפנים באופן תלוי מינון ואז הצטמצמות כאשר הקולטנים רוויים, משקפת התנהגות קלאסית של קולטני חלבון‑G. תרופות החוסמות או משתיקות את ADRB2 — אלפרנולול וקרזולול — כיבו את התגובה בדיוק כמצופה. כאשר המחברים גם כללו בחלל הווניקולות חמישה אנזימים שהופכים בדרך רגילה גליקוגן לגלוקוז‑1‑פוספט (G‑1‑P) ולאחר מכן ל‑NADPH, גירוי ב‑ISO הוביל לייצור מדיד של שניים אלה בתוך התאים המלאכותיים, כפי שעוקבו בעזרת ספקטרומטריה מסה, כרומטוגרפיה ופלואורוסנציה.
להגביר לחישה לחלישה רועמת
ממצא מרכזי הוא עד כמה התגובה הפנימית הוגברה. כמות מתונה של ISO מחוץ לוניקולות ייצרה בערך פי 22 יותר מולקולות cAMP מאשר מולקולות ISO, וההגברה הזו התעצמה עוד יותר לאורך הנתיב. כאשר האות הוביל לפירוק גליקוגן והמרה ל‑6‑פוספוגלוקונולקטון עם NADPH נלווה, ההגברה הכוללת עלתה על פי מאה. ההגברה הצעד‑אחר‑צעד הזו היא סימן היכר של איתות הורמונלי טבעי ומראה שהמערכת המלאכותית עושה יותר מאשר רק לגלות ISO — היא מעבדת ומגבירה את המסר לתוצר מטבולי איתן.
מדוע זה חשוב עבור חיים סינתטיים עתידיים
לא‑מומחה, הפרטים הטכניים מתמצים לרעיון פשוט: החוקרים לימדו תא מינימלי שנעשה בידי אדם להקשיב ולהגיב כמו תא חי. מולקולת תרופה חיצונית מתקינה על קולטן אנושי ריאליסטי, אות עובר דרך ממברנה סינתטית, ורשת אנזימטית פנימית מגיבה על‑ידי ניוד אנרגיה כימית מאוחסנת. הדגמת שרשרת מלאה זו — מהפעלת הקולטן ועד מטבוליזם מבוקר — במערכת מלאכותית מצומצמת היא צעד משמעותי לקראת תאים סינתטיים אוטונומיים שיכולים לחוש, להחליט ולפעול בדרכים שימושיות, כמו להתאים את אספקת האנרגיה שלהם או לשחרר טיפולים רק כאשר הם מזהים רמזים כימיים מתאימים.
ציטוט: Liu, Y., Zhao, W., Zhao, Y. et al. An artificial cell capable of signal transduction mediated by ADRB2 for the regulation of glycogenolysis. Nat Commun 17, 1795 (2026). https://doi.org/10.1038/s41467-026-68503-3
מילות מפתח: תאים מלאכותיים, העברת אותות, GPCR, גליקוגנוליזה, ביולוגיה סינתטית