Clear Sky Science · he
שחרור תרופות מבוקר מקום־זמן באמצעות מערכת "קליק־שחרור" המשתמשת בכימיה של מונו‑אלקיל‑הידרוקסילאמין וציקלואקטין
להפעיל תרופות עוצמתיות רק במקום בו הן נחוצות
תרופות מודרניות רבות חזקות מאוד — דבר מועיל להתגברות על סרטן או להקלה בכאב, אך מסוכן לשאר הגוף. מחקר זה מתאר "מתג" מבוסס כימיה שמאפשר לחוקרים להניח תרופות במצב בלתי־פעיל ובטוח ולהדליק אותן רק במקום ובזמן מבוקשים, למשל בתוך גידול או באזור קטן שצריך הרדמה מקומית.
סוג חדש של מתג כימי
החוקרים בונים על רעיון "כימיית קליק", משפחת תגובות שמוערכת בזכות היותה מהירה, מדויקת ובטוחה לתפקוד בסביבה ביולוגית. תגובות קליק קלאסיות מקבעות שני מולקולות זו לזו באופן קבוע. כאן, הקבוצה הופכת את ההגיון: תגובת ה"קליק" שלהם קשורה ישירות לשבירת קשר ולשחרור תרופה או מולקולת איתות. השחקנים המרכזיים הם מולקולה טבעתית הנקראת ציקלואקטין ושותף קטן בשם מונו‑אלקיל‑הידרוקסילאמין. כשהשניים נפגשים, הם נקשרים במהירות ואז עוברים ארגון מחדש כך ש"מטען" מקושר משתחרר. על‑ידי חיבור תרופות שונות או צבעים פלורסנטיים כמטען, אותה תגובה בסיסית ניתנת לשימוש למגוון מטרות. 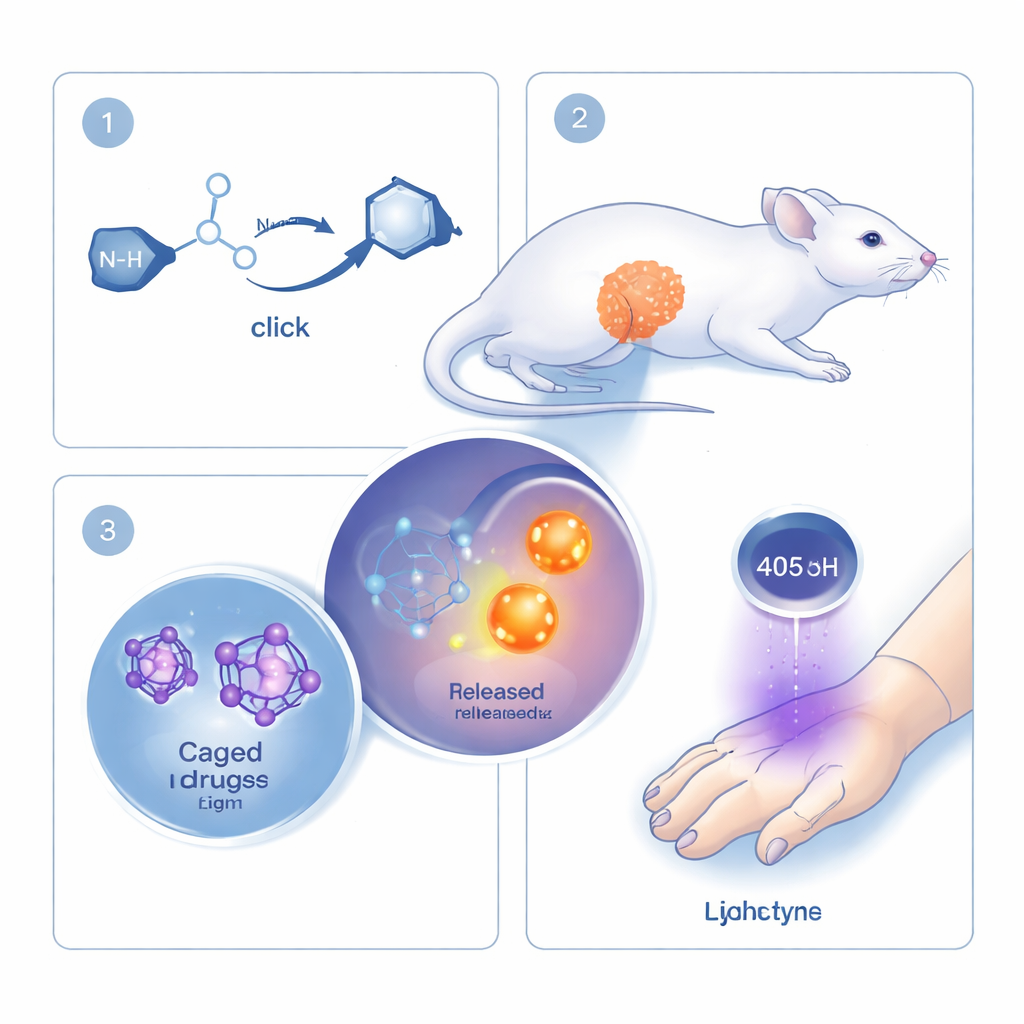
שחרור מהיר ונקי בתוך ותוך־תאי
כדי לוודא שהמתג יהיה מעשי, הצוות מדד עד כמה מהר התגובה מתקדמת וכמה באופן מלא משתחרר המטען המחובר. הם גילו שמונו‑אלקיל‑הידרוקסילאמינים שנבחרו בקפידה מגיבים הרבה יותר מהר מהידרוקסילאמין הפשוט, ומשיגים המרה כמעט‑מלאה בתוך דקות עד שעות, תלוי במבנה. באופן חשוב, השלבים הכימיים המפרקים בפועל את הקשר מהירים וסלקטיביים כל כך שכמעט כל המולקולה המחוברת משתחררת, עם פסולת נדירה. המחברים בדקו מגוון מטענים, כולל צבעים פלורסנטיים ואפילו יון פלואוריד, והראו שהמערכת יכולה לשבור כמה סוגי קשרים שכיחים בעיצוב תרופות, כגון קרבמטים ואתרים.
הארת תאים והפעלה לפי דרישה של תרופות לסרטן
בהמשך, החוקרים עברו לניסויים בתאים חיים. הם הסתירו תחילה צבעים פלורסנטיים בוהקים מאחורי המתג הכימי והוסיפו את "החומר הכלוא" הזה לתאי סרטן. כשלעצמם, הגלאים נשארו כבויים, מה שהראה שהתאים לא הפעילו אותם בשוגג. כשהתווסף שותף המונו‑אלקיל‑הידרוקסילאמין, הצבעים שוחררו והתאים נדלקו בכחול, ירוק או קרוב‑אדום, מאשר שהתגובה עובדת באופן אמין בסביבה ביולוגית. הם יישמו את הרעיון גם על דוקסורוביצין, תרופת כימותרפיה נפוצה. בצורתה הכלואה הפרודרוג הייתה בעלת רעילות נמוכה בהרבה לתאים, אך בנוכחות שותף ה"קליק" השתחררה התרופה הפעילה בצורה יעילה והשיבה את יכולתה להרוג תאים סרטניים כמעט בעוצמה של דוקסורוביצין חופשי.
בניית טריגרים חכמים למקום ולזמן
מגבלה של מערכות קליק רבות היא שהחלקים הריאקטיביים תמיד "פועלים", מה שמקשה על שליטה מדויקת במקום ובזמן. כדי לפתור זאת, הקבוצה החסימה זמנית את ריאקטיביות המונו‑אלקיל‑הידרוקסילאמין באמצעות קפסים קטנים שמוסרים רק על ידי טריגרים ספציפיים. הם יצרו גרסאות הרגישות לרמות גבוהות של גלוטתיון (מולקולה קטנה השכיחה בגידולים רבים), לאנזימים, ולמהדורות אור סגול. בתאים ובעכברים נשאים־גידול, הגרסה הרגישה לגלוטתיון נותרה שקטה בתנאים נורמליים אך הופעלה בסביבה המחזירה חמצון‑חסר של הגידול, ושחררה צבעים פלורסנטיים או הפעילה את פרודרוג הדוקסורוביצין בדיוק במקום בו הסרטן גדל. עכברים שקיבלו את השילוב של פרודרוג ועוד טריגר הראו הצטמקות גידול חזקה יותר מזו של מקבלים דוקסורוביצין סטנדרטי, תוך חשיפה פחותה של איברים רגישים כגון הלב לתרופה.
הרדמה מקומית נשלטת מרחוק באמצעות אור
כדי להדגים שליטה בזמן, המחברים תכננו יישום שני: הרדמה מקומית מונחית אור. הם חיברו את חומר ההרדמה טטרקאאין לרקמת הציקלואקטין שלהם, מה שהפך אותו לבטוי, וערבבו את הפרודרוג הזה עם גרסה רגישת אור של ההידרוקסילאמין בתוך ג'ל רגיש לטמפרטורה. הוזרק לכף רגל של עכבר, התערובת לא עשתה דבר עד שהעור נחשף לאור באורך גל 405 ננומטר. ההאדרה שיגרה את תגובת ה"קליק‑שחרור", שחררה את הטטרקאאין ויצרה הירדמות המושווית להזרקה ישירה של טטרקאאין. על‑ידי שינוי משך ועוצמת האור הם יכלו לכוון כמה זמן המשך הבלוק העצבתי, ואף הצליחו לעורר גלויים חוזרים של הרדמה מזריקה יחידה. 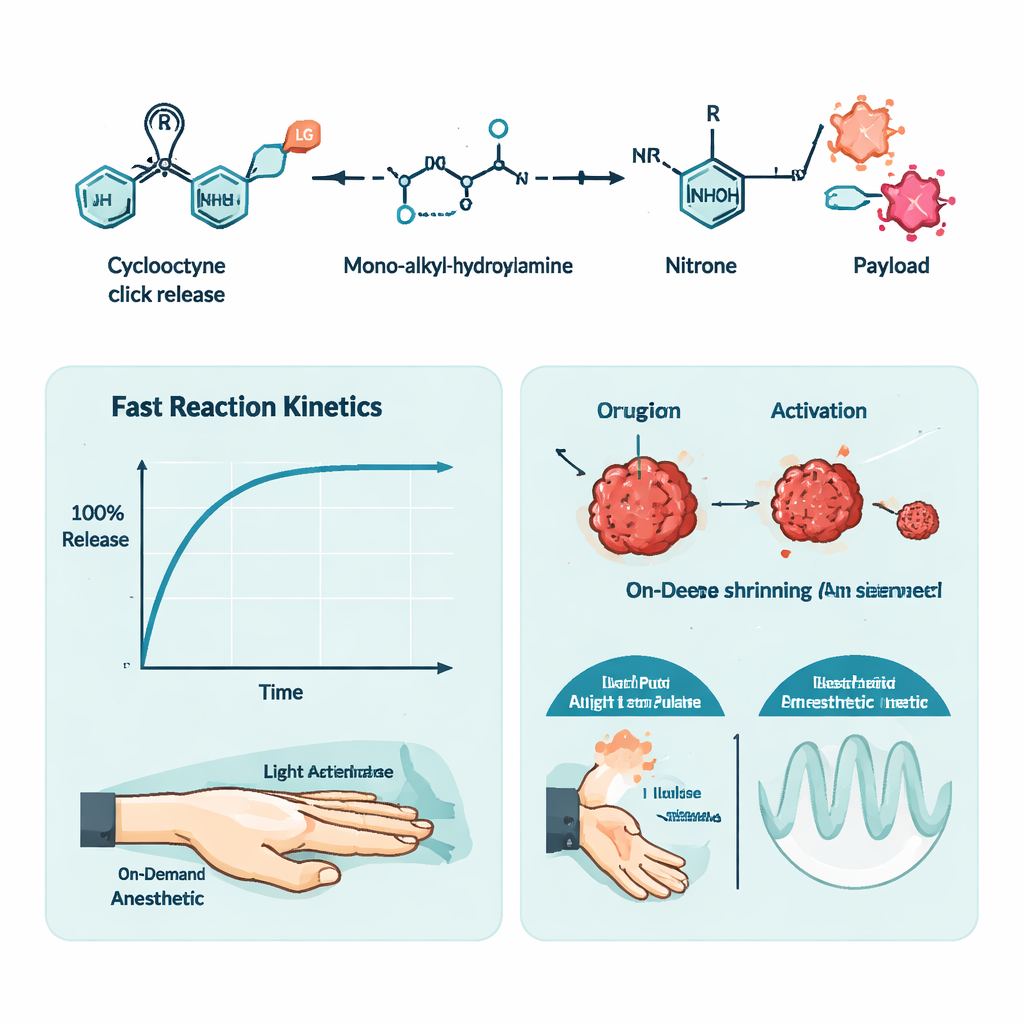
מה המשמעות של זה עבור טיפולים עתידיים
בעיני הלא‑מומחים, המסר המרכזי הוא שעבודה זו מציעה שלט כימי גמיש מרחוק לתרופות: ניתן למסור תרופות בצורה בטוחה ושקטה ואז להפעיל אותן רק בנקודה ובזמן הנכונים, באמצעות אותות שמגיעים מהגוף עצמו או ממקור אור חיצוני. בעוד שצריך עוד בדיקות לפני שימוש קליני, הגישה עשויה בסופו של דבר להפוך טיפולי סרטן לממוקדים ופחות רעילים, לאפשר שליטה מותאמת בכאב לאחר ניתוח, ולתמוך בטווח רחב של טיפולים שתועלתם קשורה לשליטה מדוייקת במקום ובזמן.
ציטוט: Xu, X., Tong, X., Shi, Y. et al. Spatiotemporally controlled drug release via a click-release system utilizing mono-alkyl-hydroxylamine and cyclooctyne chemistry. Nat Commun 17, 1794 (2026). https://doi.org/10.1038/s41467-026-68502-4
מילות מפתח: כימיית קליק, העברת תרופות ממוקדת, פרודרגות, מיקרו‑סביבה של הגידול, הרדמה נשלטת באור