Clear Sky Science · he
מטרת קסקדת UFL1–AKT מדכאת התקדמות סרטן השד המשולש-שלילי
למה מחקר זה חשוב
סרטן השד המשולש-שלילי (TNBC) הוא אחד הצורות הקטלניות ביותר של סרטן השד, מאחר שהוא חסר את מתגי ההורמונים והגורמי הצמיחה שאליהם פונות תרופות מודרניות רבות. מטופלים לעתים קרובות מקבלים רק כימותרפיה מסורתית, שיכולה להפסיק להשפיע כאשר הגידולים מפתחים עמידות. המחקר הזה חושף “מנוע” מולקולרי חבוי שמסייע לתאי TNBC לגדול ולהתנגד לכימותרפיה, ומציע סוג חדש של תרופה שמפריעה ישירות למנגנון זה.
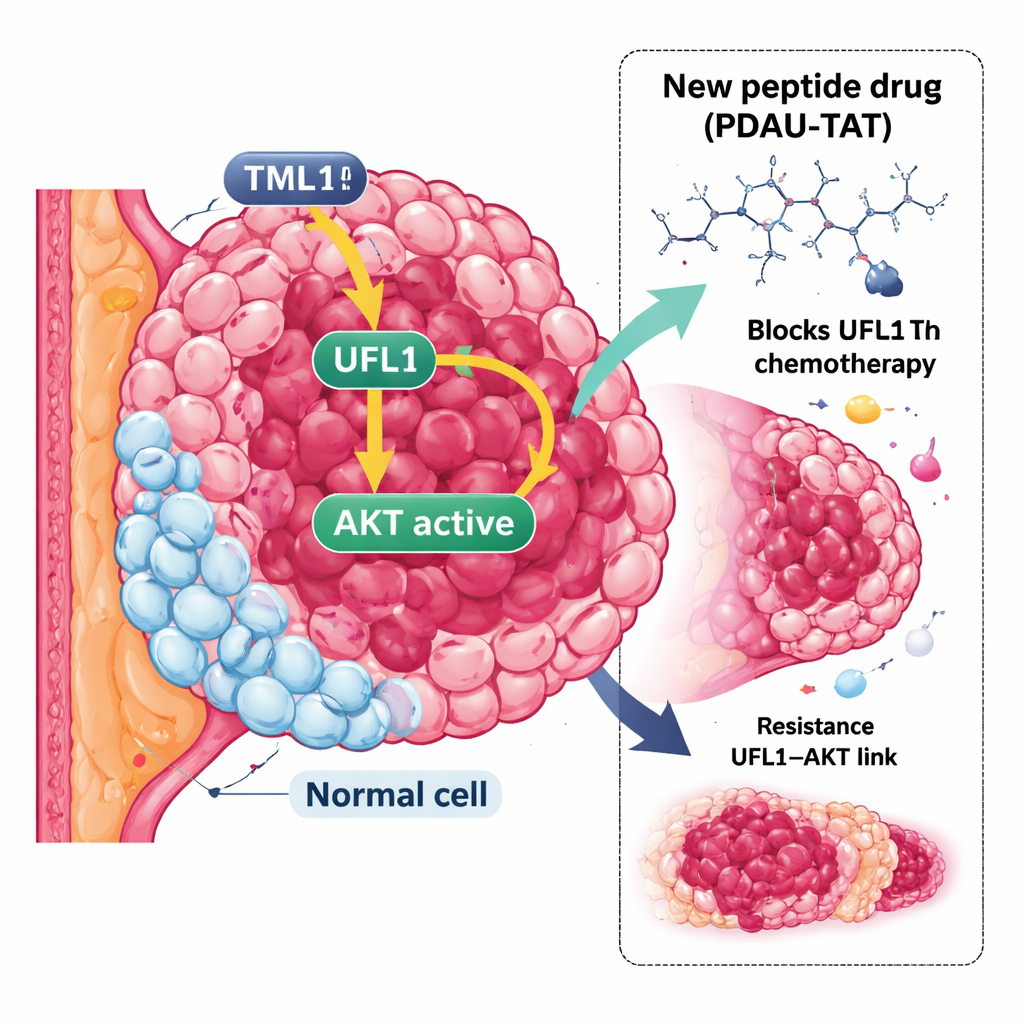
צורה עיקשת של סרטן השד
TNBC מוגדר בחסרונם של שלושה סימנים נפוצים: קולטן אסטרוגן, קולטן פרוגסטרון וקולטן הגידול HER2. ללא סימנים אלה, רבות מהתרופות הממוקדות המוצלחות פשוט אינן חלות. במקום זאת משתמשים בתרופות סטנדרטיות כגון ציספלטין ודוקסורוביצין, אך גידולי TNBC לעתים קרובות מפתחים עמידות או מסתגלים במהירות לטיפולים אלה ונמצאים בסיכון גבוה יותר להתפשטות. הדבר יוצר צורך דחוף באסטרטגיות חדשות שמחפשות חולשות אחרות במערכות הבקרה של הגידול.
חלבון מוכר-מעט בעל השפעה גדולה
החוקרים התמקמו ב-UFL1, חלבון שמחבר תג קטן הנקרא UFM1 לחלבונים אחרים בתהליך הידוע כ-UFMylation. מערכת התגיות הזו התגלתה רק לאחרונה ותפקידה בסרטן היה מעורפל ולעתים אף סותר. באמצעות ניתוח נתוני מטופלים ודגימות גידול, הצוות הראה ש-UFL1 מוגבר משמעותית ב-TNBC בהשוואה לרקמת שד נורמלית. כאשר הקטינו את רמות UFL1 בקווי תאים של TNBC ובדגמי גידול בעכברים, תאי הסרטן התרבו לאט יותר והפכו לרגישים הרבה יותר לכימותרפיה, מה שמרמז כי ל-UFL1 תפקיד מקדם-גידול בהקשר זה.
חיבור של UFL1 למתג הצמיחה המרכזי
בחקר מעמיק יותר, המדענים גילו ש-UFL1 נקשר ישירות ל-AKT, חלבון איתות מרכזי שמניע גדילה, הישרדות ומטבוליזם של תאים ולעתים קרובות פעיל מדי בסרטן. ב-TNBC, AKT פעיל לעתים קרובות גם כאשר המוטציות המקוריות שמפעילותו חסרות. הצוות מצא כי UFL1 מתייג כימית את AKT בשלושה אתרים ספציפיים, מה שמקל על הפעלתו על ידי שותפיו המפעילים ובמקביל מגן עליו מפני אנזימים שאחרת יכבו אותו. תאים חסרי UFL1 או מבטאים צורת AKT מהונדסת שאינה יכולה לקבל תגיות אלו הראו פעילות AKT נמוכה בהרבה, גדילה איטית יותר ופגיעות מוגברת לכימותרפיה הן בתרביות תאים והן בדגמי בע״ח.
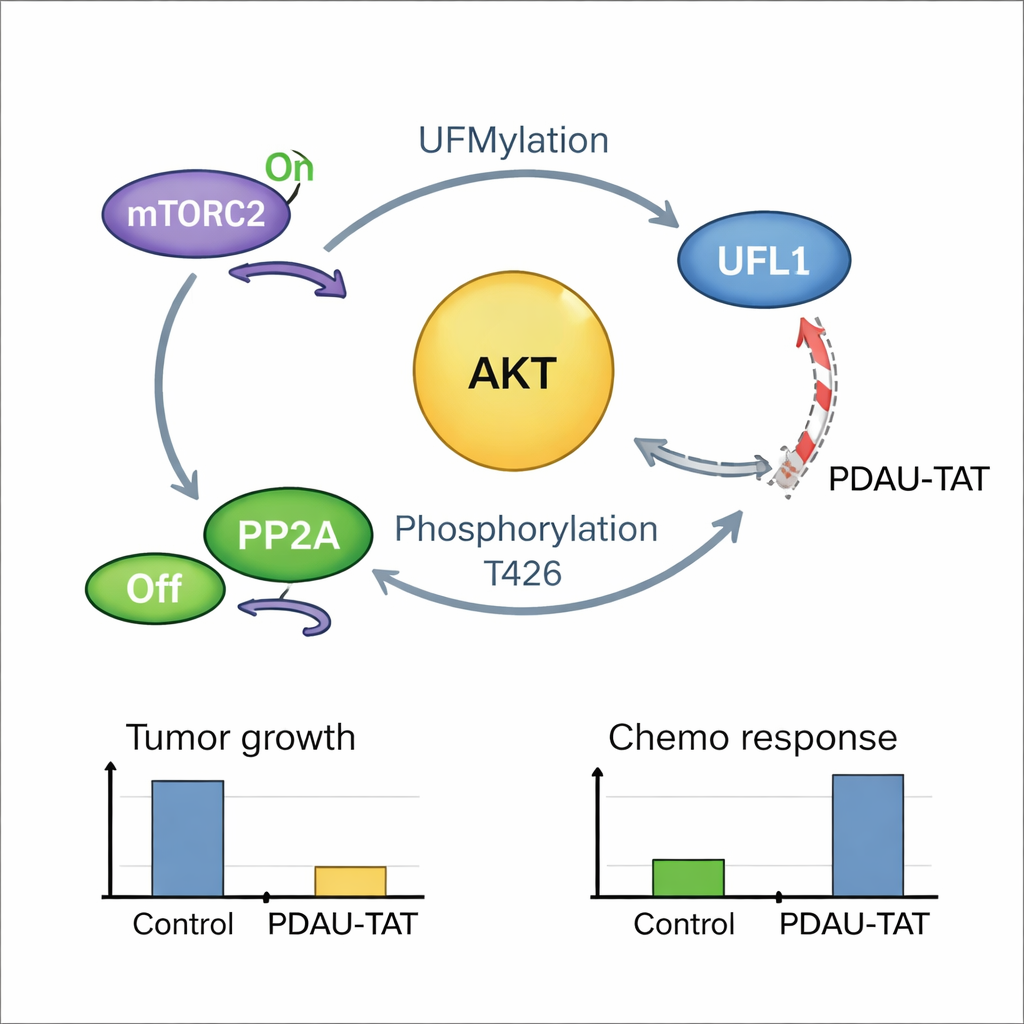
מעגל מחזק-עצמו של סרטן ודרך לשבורו
הסיפור התגלה כקשור אף יותר זה לזה: לאחר ש-AKT פעיל, הוא חוזר ומשנה את UFL1 באתר קריטי אחד, ומגביר את פעילות התיוג של UFL1 על AKT ומטרות נוספות. זה יוצר לולאת משוב חיובית שבה UFL1 מפעיל את AKT, ו-AKT הפעיל בתורו מחזק את UFL1. דגימות מטופלים הראו שרמות גבוהות של UFL1 הממוטב קשורות בחוזקה לרמות גבוהות של AKT פעיל, מה שתומך בקיומה של הלולאה במחלה האנושית. כדי לנצל את הפגיעות הזו, הצוות עיצב פפטיד קצר החודר־תאים, שנקרא PDAU-TAT, המחקה אזור קטן של UFL1 וננעץ בין UFL1 ל-AKT. פפטיד זה מפריע לאינטראקציה ביניהם, מצמצם את הפעלת AKT, מאט את גדילת הגידול ומשפר את תגובת תאי ה-TNBC וגידולים שמקורם בחולים לכימותרפיה, כל זאת ללא נזק ברור לאיברים מרכזיים בעכברים.
מה משמעות הדבר עבור מטופלים
במונחים פשוטים, החוקרים חשפו שרטוט חיבור פנימי בתאי TNBC: UFL1 ו-AKT תקועים בלולאה מחזקת-עצמה ששומרת על אותות הגדילה במצב "פועל" ועוזרת לגידולים להתנגד לטיפול. על ידי בניית פפטיד קטן שמחליק לתוך הלולאה ומנתק את UFL1 מ-AKT, הם מציגים דרך אפשרית להחליש גידולי TNBC תוך שמירה על תאי הרקמה הרגילים, שלרוב בעלי רמות UFL1 נמוכות יותר. למרות שהעבודה עדיין נמצאת בשלבי טרום-קליניים, היא מצביעה לכיוון של מחלקת טיפולים ממוקדים חדשה שמטרתה לא את הקולטנים הרגילים אלא את הקשרים בין חלבונים שמניעים כמה מהגידולים האגרסיביים ביותר של השד.
ציטוט: Yang, X., Wen, Y., Ma, X. et al. Targeting the UFL1-AKT cascade suppresses triple-negative breast cancer progression. Nat Commun 17, 613 (2026). https://doi.org/10.1038/s41467-026-68493-2
מילות מפתח: סרטן השד המשולש-שלילי, אותות AKT, UFMylation, UFL1, תרפיית פפטיד בסרטן