Clear Sky Science · he
לולאת המשוב החיובית UFL1‑AKT מקדמת התקדמות סרטן השד על ידי הגברת סינתזת השומנים
למה תאי סרטן כל כך זקוקים לשומן
תאי סרטן השד, כמו כל תאים שמתרבים במהירות, זקוקים לאספקה קבועה של בלוקים בנייה כדי לבנות ממברנות חדשות ולהכין מולקולות איתות. שומנים, או ליפידים, מהווים מרכיב מרכזי באספקה הזו. המחקר חושף כיצד מערכת חלבונית שנשכחה עד כה מזיזה את תאי הסרטן ל"מצב ייצור שומן מוגבר", מה שעוזר לגידולים לגדול ולהתחמק מטיפולים. הבנת צינור הדלק החבוי הזה עשויה לפתוח דרכים חדשות להאטה או הרעבת סרטן השד.
תג חלבוני מוסתר עם השלכות גדולות
התאים שלנו מתאימים בהתמדה את התנהגות החלבונים שלהם בעזרת תגיות כימיות זעירות. אחת התגיות האלה, שנקראת UFM1, מוספת על ידי אנזים בשם UFL1. תגיות UFM1 (UFMylation) נקשרו בעבר לתיקון DNA ולהתמודדות עם סטרס, אך תפקידן בסרטן היה לא ברור. המחברים מראים ש‑UFL1 פעיל הרבה יותר בגידולי שד אנושיים מאשר ברקמה שדית נורמלית, בכל תת‑הסוגים העיקריים. חולים שגידוליהם מבטאים רמות גבוהות יותר של UFL1 נוטים להישרדות גרועה יותר. כאשר החוקרים צמצמו את רמות UFL1 בתאי סרטן השד או בגידולים בעכברים, קצב הגדילה האט, חלוקה תאית ירדה ושיעור המוות התאי עלה, מה שמרמז ש‑UFL1 מתصرف כגורם מקדם‑סרטן.
כיצד צומת איתות משתנה למצב ייצור שומן
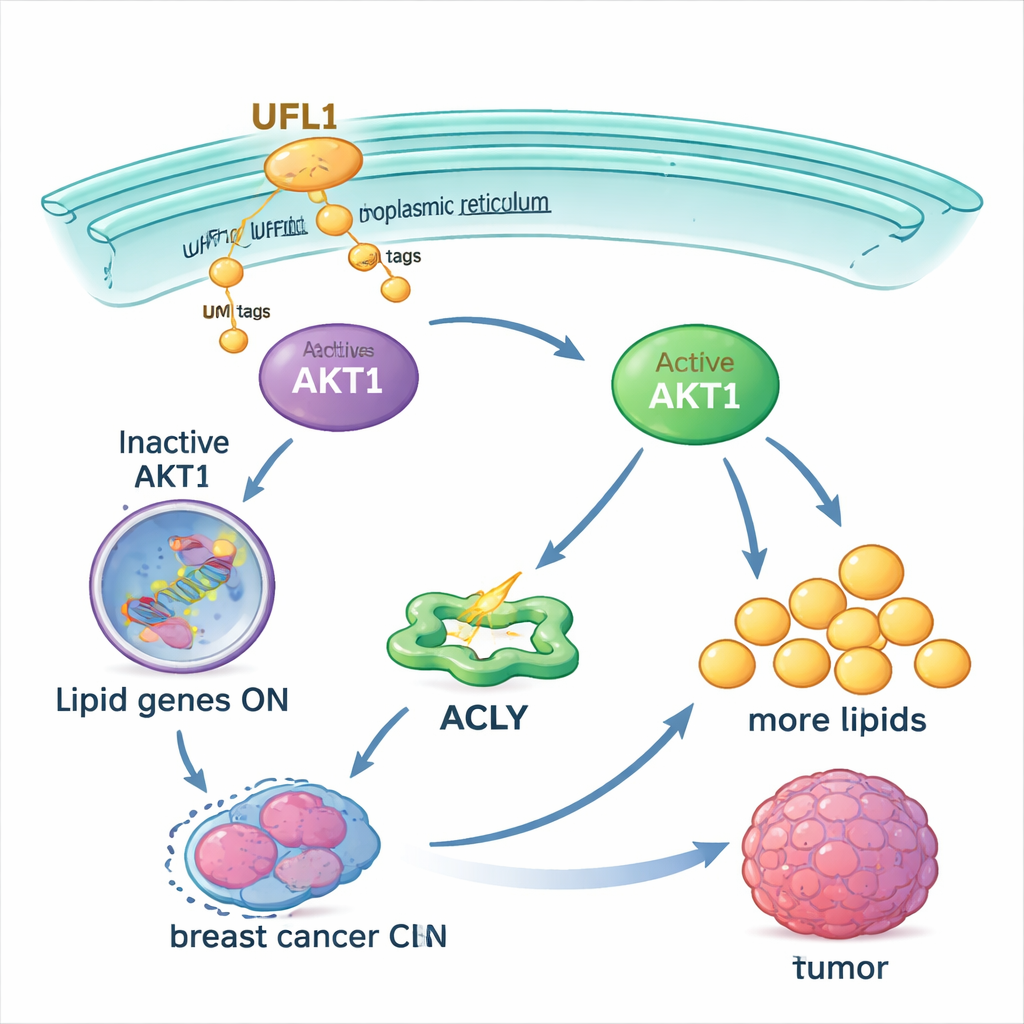
כדי להבין כיצד UFL1 מסייע לגידולים, הצוות חיפש את שותפיו המולקולריים וגילה חלבון בקרה מרכזי שנקרא AKT1. AKT1 הוא מתג מרכזי שאומר לתאים לגדול ולייצר ליפידים חדשים. המחקר מראה ש‑UFL1 נקשר פיזית ל‑AKT1 ומסמן אותו בתגיות UFM1 בכמה אתרים ספציפיים. תגיות אלה משנות את צורתו של AKT1, משחררות "מעצור" פנימי שבדרך כלל משמור על שקטו, ומסייעות להעבירו למחסום ממברנלי בתוך התא — הרשתית האנדופלסמית — שם אנזימים אחרים יכולים להפעילו במלואן על‑ידי הוספת קבוצות פוספט. בלי תגיות UFM1 באתרים אלה, קשה הרבה יותר להפעיל את AKT1.
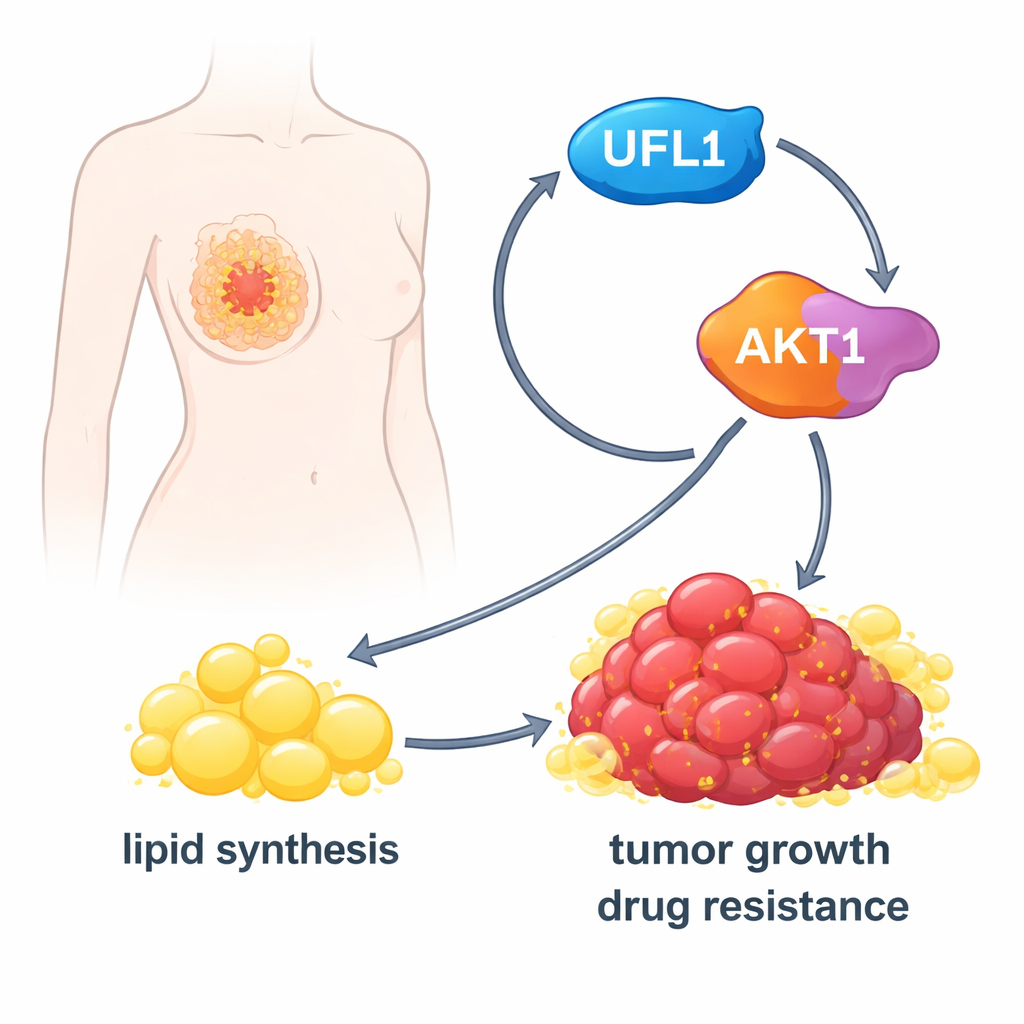
הפעלת "מפעל השומן" של הסרטן
ברגע שמופעל, AKT1 מדרבן את התאים להגביר את ייצור השומנים שלהם. הוא מגביר את פעילותו של אנזים מטבולי מפתח, ACLY, ומעלה את רמות של רגולטורים מרכזיים כגון SREBP1 שמפעילים רבים מהגנים ליצירת שומן. בתאי סרטן השד שגודלו במעבדה, UFL1 גרם להצטברות טיפות שומן, חומצות שומן חופשיות וכולסטרול. הסרת UFL1 צמצמה באופן ניכר מאגרים אלה של ליפידים, הן בתרבית והן בגידולים שגודלו בעכברים. אספקת חומצות שומן חיצוניות הגיעה במידה רבה להציל את גדילת תאים חסרי UFL1, דבר שמעיד שההשפעה המרכזית של UFL1 היא להבטיח מספיק ליפידים לתמיכה בהתרחבות הגידולית.
לולאה מתעצמת שמניעה את גדילת הגידול
בהפתעה, היחסים בין UFL1 ל‑AKT1 הם דו‑כיווניים. החוקרים גילו שברגע ש‑AKT1 פעיל, הוא בתורו מוסיף תג פוספט ל‑UFL1 באתר מסוים. השינוי הזה מגדיל עוד יותר את יכולתו של UFL1 לתג‑את AKT1 ב‑UFM1, ובכך יוצר לולאת משוב חיובית: UFL1 מפעיל את AKT1, ו‑AKT1 מפעיל את UFL1. שיבוש או מוטציה באתרי התגובה ל‑UFM1 ב‑AKT1 או באתר הפוספט ב‑UFL1 שוברים את הלולאה. בעכברים, גידולים שנשאבו וריאנטים מוטנטיים אלה גדלו באופן לקוי, הכילו פחות ליפידים והצגתו תמותה תאית גבוהה יותר. בדוגמיות מחולים עם סרטן שד טריפל‑נגטיבי, רמות גבוהות של UFL1 מופעל וצירוף של AKT1 מופעל נטו להופיע יחד, מה שמדגיש שהלולאה פועלת גם בגידולים אמיתיים.
החלשת הלולאה כדי לסייע לטיפולים
מכיוון שמחקרים רבים כבר ממוקדים ב‑AKT, המחברים בדקו האם חסימת UFMylation יכולה לשפר את האפקטיביות של טיפולים אלה. בתאי סרטן השד, מעכב קטן של UFMylation ומעכב של AKT הורידו כל אחד בנפרד את פעילות AKT1 והצטברות הליפידים, אך השימוש בשניהם יחד עבד טוב בהרבה מאשר כל אחד בנפרד. השילוב גם האט את גדילת הגידולים והפחית את תכולת השומן בגידולים בעכברים מבלי לגרום לאובדן משקל מורגש בבעלי החיים. חסימת UFMylation גם הגבירה את הרגישות של תאי הסרטן לכימותרפיות סטנדרטיות כמו ציספלטין ואתופוסיד, שהן לעיתים כושלות כאשר AKT פעיל מאוד.
מה זה אומר לחולים
במילים פשוטות, המחקר מראה כי סוגים מסוימים של סרטן השד בונים לעצמם לולאת חיזוק עצמית שמזינה הן את גידולם והן את מאגרי השומן שלהם. UFL1 ו‑AKT1 פועלים יחד כמו שני דוושות שנלחצות בו‑זמנית: אחד מתייג, השני מעביר אותות, וביחד הם מזרזים ייצור ליפידים והתרחבות גידולית. מציאת תרופות שמפריעות ללולאה הזו — בין אם על‑ידי חסימת UFMylation, חסימת AKT1 או פגיעה באינטראקציה ביניהם — עשויה לאפשר טיפולים שיראו האטה בגדילת הגידול ויחזקו את האפקטיביות של טיפולים קיימים, במיוחד בסוגים אגרסיביים של סרטן השד.
ציטוט: Meng, F., Du, Y., Liang, J. et al. The UFL1-AKT positive feedback loop promotes breast cancer progression by enhancing lipid synthesis. Nat Commun 17, 614 (2026). https://doi.org/10.1038/s41467-026-68492-3
מילות מפתח: סרטן השד, מטבוליזם שומנים, אותות AKT, UFMylation, טיפול ממוקד