Clear Sky Science · he
הידרוג’ל מאוגד בתאי המטען בתוך האתר לטיפול רדיואימונותרפי רב-שלבי
להפוך את הקרינה לכלי חכם יותר נגד סרטן
טיפולי קרינה הם מבין הטיפולים הנפוצים ביותר בסרטן, אך גידולים לעתים שורדים על ידי התחמקות ממערכת החיסון ועל ידי גדילה בתנאי חוסר חמצן (היפוקסיה) שמחלישים את השפעת הקרינה. המחקר הזה מתאר הידרוג׳ל «חכם» שניתן להזרקה ונבנה ישירות בתוך הגידול ופועל כמפעל תרופות קטן וייצרן חמצן. על ידי אספקת קרינה לצד אותות מעוררי חיסון במינון ובזמני שחרור מבוקרים, המערכת שואפת להפוך גידול שקשה לטפל בו למטרה שמערכת ההגנה של הגוף יכולה לזהות ולהשמיד.
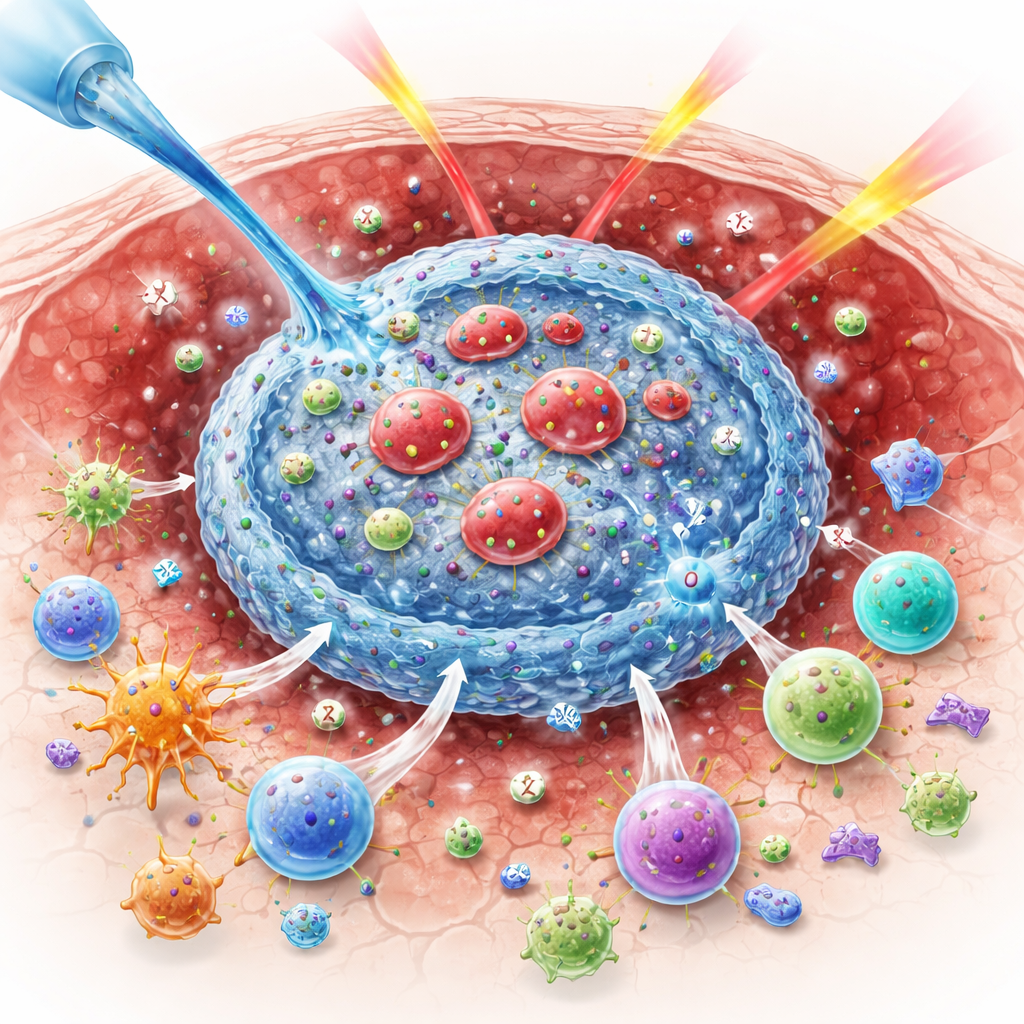
מדוע החמצן חשוב להכריע גידולים
קרינה הורגת תאי סרטן חלקית על ידי יצירת מולקולות חמצן פעילות במיוחד שמשבשות את ה-DNA. כאשר הגידולים סובלים ממחסור בחמצן, הכימיה הזו פוחתת ביעילותה ולכן יותר תאי סרטן שורדים. במקביל, הקרינה משדרת מסר מעורב למערכת החיסון: היא יכולה לחשוף חלבוני גידול שמסמנים את הסרטן כמסוכן, אך גם להגביר מעצורים על תאי חיסון, כגון חלבון הביקורת CTLA-4, ולטפח תאי T רגולטוריים שמדכאים התקפה. ההשפעות הנגדיות האלה מסבירות מדוע שילוב קרינה עם תרופות אימוניות לא תמיד עבד אצל מטופלים כפי שעבד בעכברים.
ג’ל חי הנבנה בתוך הגידול
החוקרים תכננו חומר שמתאסף עצמי רק בסביבה החומצית של הגידול. הוא מורכב משלושה חלקים מרכזיים: פולימר טבעי מבוסס סוכר שנקרא אלגינט, אבקה אי-אורגנית בשם פרוקסיד בריום ותאי דם אדומים שעובדו בעדינות לשאת שתי תרופות אימוניות. כשהתערובת מוזרקת לגידול, התנאים החומציים מפעילים פירוק של פרוקסיד הבריום, שמשחרר יוני בריום ומימן פרוקסיד. יוני הבריום מחליפים קשרים מידיים וגורמים לצמיגות האלגינט להצטלב ולהפוך להידרוג׳ל רך, הכלוא את תאי הדם האדומים המתוכננים ומונע מהתרופות להישטף החוצה. בו־בזמן, אנזימים שנמצאים באופן טבעי בתאי הדם האדומים ממירים את המימן פרוקסיד לחמצן, מה שמסייע להקל על ההיפוקסיה בגידול ומכין את הגידול לקרינה יעילה יותר.
שחרור מתוזמן של שני אותות חיסוניים
עוצמת המערכת טמונה בדרך שבה היא מתזמנת את שחרור שני הגורמים החיסוניים: נוגדן החוסם את CTLA-4 וציטוקין בשם אינטרלויקין-12 (IL-12). הנוגדן נטען בתוך תאי הדם האדומים, בעוד IL-12 מעוגן על המשטח שלהם. ככל שהחמצן מיוצר, נפתחות נקבוביות בממברנת תאי הדם האדומים, ומאפשרות לנוגדן החוסם CTLA-4 להיחלץ במהירות. הפרץ המוקדם הזה מוריד את הדיכוי החיסוני, מעודד תאי דנדריט לשאת אנטיגנים של הגידול לבלוטות הלימפה סמוכות ועוזר להפעיל תאי T ספציפיים לגידול. לעומת זאת, ה-IL-12 נזיל באיטיות כשהמבנה של ההידרוג׳ל מתרפה בהדרגה. האות המאוחר הזה דוחף תאי T ותאי NK לייצר אינטרפרון-גאמה, מזין גיוס נוסף של תאי חיסון קטלניים אל תוך הגידול ומחזק לולאת משוב חיובית בין השומרים החיסוניים למבצעים.
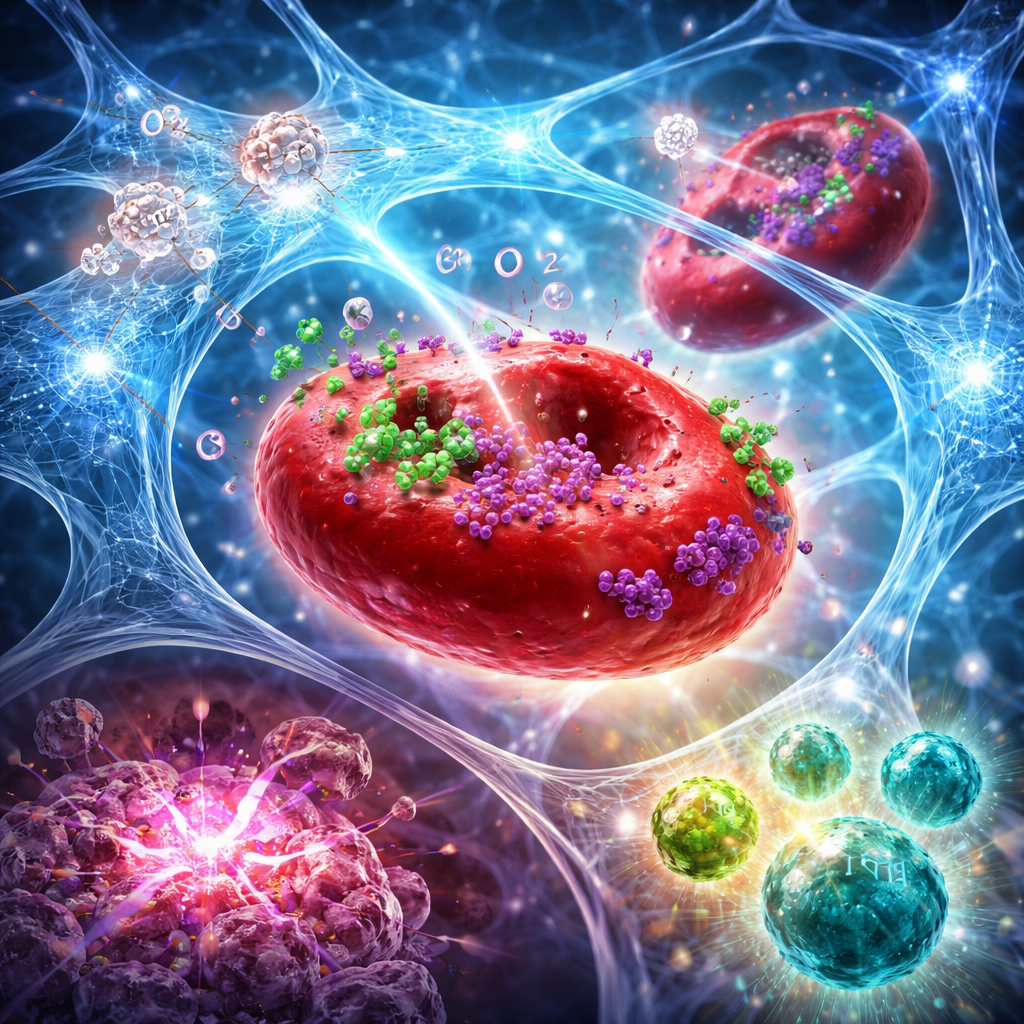
מהזרקה מקומית להתקפת חיסון מערכתית
בדגמי עכברים של סרטן שד ולבלב אגרסיביים, שילוב ההידרוג׳ל עם קרינה ממוקדת עשה יותר מהקטנת הגידול הטופל בלבד. הגישה המשולבת העלתה את רמות החמצן בגידולים למשך ימים, הגברה את נזק ה-DNA המושרה על ידי הקרינה והובילה לצורת מוות תאית חזקה יותר שמסמנת את הגידול לזיהוי חיסוני. ציטומטריית זרימה וצביעות רקמות הראו שינוי בולט במיקרו-סביבה של הגידול: יותר תאי T קטלניים מסוג CD8 ותאי NK, פחות תאי T רגולטוריים, ושיעור גבוה יותר של תאים «מעשיים» לעומת «מדכאים». תאי דנדריט מיוחדים בבלוטות הלימפה גם עלו במספרם, מעיד על הצגה טובה יותר של אנטיגנים. אצל עכברים רבים נצפתה נסיגה מלאה של הגידול, וכמה אפילו הוגנו מפני התחדשות הגידול כשהוכנסו מחדש תאי סרטן שבועות אחר כך, מה שמרמז על היווצרות זיכרון חיסוני עמיד.
בטיחות, נוחות וכיוונים עתידיים
מאחר שהג’ל נוצר באופן מקומי ושומר על המטען שלו, רק כמויות קטנות של IL-12 ונוגדן נגד CTLA-4 דולפות למחזור הדם, דבר שמפחית את הסיכון לתופעות לוואי חמורות כגון סערות ציטוקינים או נזק לאיברים שהגבילו את השימוש בסוכנים אלה בעבר. מרכיבי הבנייה—אלגינט, תאי דם אדומים ופרוקסיד בריום—זולים ביחסית וניתנים להגדלה בקנה מידה, מה שמעורר תקווה שאסטרטגיה זו ניתנת להתאמה לסרטן שונה. למרות שעומדות בפני הייצור, בקרת איכות והעברת הג’ל לגידולים עמוקים או מפושטים אתגרים, העבודה מציגה דרך מבטיחה לסנכרן קרינה עם תזמון מדויק של הפעלת חיסון, ולהפוך טיפול פיזי בסרטן לדקירה שמפעילה תגובת חיסון אנטי-גידולית בגוף כולו.
מה המשמעות הזו לחולים
במונחים פשוטים, המחקר מציע שבמקום לתת קרינה ותרופות אימוניות בנפרד ולתקוות שהן ישתפו פעולה, ניתן לארוז את שניהם בתוך חומר חכם שיושב בתוך הגידול, מייצר חמצן בעצמו ומשחרר אותות חיסוניים ברצף מתוזמן במדויק. בבעלי חיים, הגישה הזו לא רק הגבירה את קטלנות הקרינה כלפי תאי הסרטן אלא גם אימנה את מערכת החיסון לזהות ולזכור את הגידול, ובכך סייעה למנוע הישנות. אם ניתן להגיע לתוצאות דומות בבני אדם, הידרוג׳לים מסוג זה יוכלו יום אחד להפוך גידולים שקשה לטפל בהם למטרות שמערכת ההגנה של הגוף יכולה לזהות ולהשמיד באופן אמין.
ציטוט: Chen, Y., Chen, Q., Ma, Y. et al. In situ self-assembled cell reservoir hydrogel for maneuvering multistage radioimmunotherapy. Nat Commun 17, 1784 (2026). https://doi.org/10.1038/s41467-026-68490-5
מילות מפתח: רדיואימונותרפיה, הידרוג׳ל, אימונותרפיה של סרטן, מיקרו-סביבת גידול, הקרנות