Clear Sky Science · he
בסיס מבני לעיכוב בררני של נשא ה‑GABA האנושי GAT3
מדוע איתותים מעכבים במוח חשובים
המוחות שלנו מסתמכים על איזון עדין בין אותות שמגרה לבין אלה שמרגיעים. שליח עיקרי שמרגיע הוא GABA, מולקולה שעוזרת למנוע פעילות בלתי מבוקרת המקושרת למצבים כגון אפילפסיה, נזק שבץ ומחלת אלצהיימר. המחקר הזה מתמקד בחלבון בשם GAT3, שמנקז GABA מאזורי התא העצביים. על ידי גילוי, בפרטים אטומיים, כיצד מולקולה חדשה נקשרת ל‑GAT3 ומכבה אותו, החוקרים מספקים מפת דרכים מבנית לעיצוב תרופות דור הבא שיכולות להגביר בעדינות את מערכת הבלם הטבעית של המוח.
דוושה של המוח
GABA הוא המוליך המעכב המרכזי במערכת העצבים המרכזית. לאחר ש‑GABA משתחרר מקצות עצב, יש להסירו במהירות כדי שהמעגלים המוחיים יוכלו לאפס את עצמם. הניקיון הזה מתבצע על ידי חלבוני נשא שמשאבים את ה‑GABA חזרה לתאים. שני נשאים דומיננטיים במוח הם GAT1, המצוי בעיקר בניורונים, ו‑GAT3, המצוי בתאי תמיכה הנקראים אסטרוציטים. אף שבעבר נעשה שימוש בתרופה החוסמת GAT1 (טיאגאבין) במשך עשורים לטיפול באפילפסיה, תרופות מקבילות המכוונות ל‑GAT3 לא התפתחו באותה מהירות. עם זאת, GAT3 מעניין במיוחד משום שהוא שולט ברמות GABA מחוץ לסינפסות ועיצב עיכוב רקע ממושך שיכול לכוונן בפירוט את פעילות המוח. 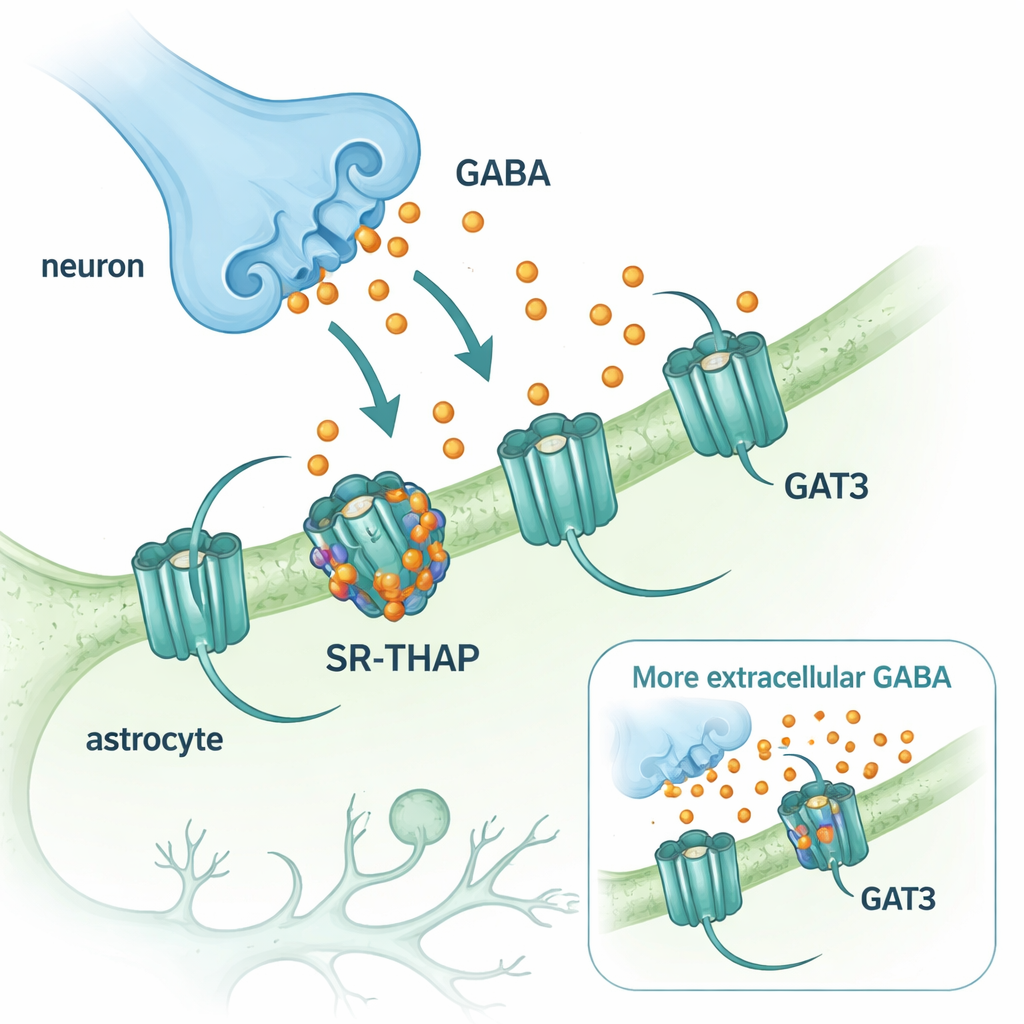
עיצוב מנעול מולקולרי מדויק יותר
ניסיונות לעכב את GAT3 הסתבכו מחוסר מידע מבני מפורט. רבים מהתרכובות הקודמות נוצרו בניסוי וטעיה, לעיתים על ידי יצירת וריאציות מסיביות של מולקולות דמו‑GABA ידועות. אחת הידועות ביותר, (S)‑SNAP‑5114, התגלתה ככימית לא יציבה וקשה לשימוש בחיות חיות. בהתבסס על קרוב יציב יותר של תרכובת זו, החוקרים פיתחו את SR‑THAP, מולקולה קטנה חדשה שעוצבה להתאים ל‑GAT3 ביתר דיוק ולעמוד בפני פירוק. ניסויים בתרביות תאים אנושיות הראו כי SR‑THAP חוסמת בחוזקה את GAT3 ופועלת באופן לא תחרותי: במקום להתחרות פשוט עם GABA באתר המוכר, היא משנה את אופן הפעולה של הנשא ומקטינה את קיבולת ההובלה המקסימלית שלו.
צפייה ב‑GAT3 ברזולוציה כמעט אטומית
כדי להבין בדיוק כיצד SR‑THAP פועל, הצוות פנה למיקרוסקופ אלקטרונים קריוגני (cryo‑EM), טכניקה שמדמה קפיאה מהירה לחלבונים ומאפשרת לשחזר את צורתם התלת־ממדית. הם פתרו שלוש תמורות של GAT3 האנושי: קשור ל‑SR‑THAP, קשור ל‑GABA, ובמצב ללא סובסטרט. שלושתם חושפים את האדריכלות הטיפוסית שנמצאת בנשאי מוליכים עצביים משויכים: 12 הליקסים צפופים שחוצים את הממברנה ויוצרים נתיב מרכזי ל‑GABA ויוניו הלווים, נתרן וכלוריד. במבנה הקשור ל‑GABA, הנשא נמצא במצב "סגור‑פנימה" — GABA ויון נתרן מהודקים במרכז, מבודדים הן מהחוץ והן מהפנים. חומצה אמינית ארומטית מרכזית יוצרת אינטראקציה מיוחדת עם קבוצת האמין של ה‑GABA, ומסבירה כיצד GAT3 מזהה את הסובסטרט שלו.
כיצד SR‑THAP מייבש את הנשא פתוח
בניגוד מרשים, המבנה הקשור ל‑SR‑THAP לוכד את GAT3 במצב "פתוח‑פנימה", כשהצד הפנימי של החלבון פונה ומתרחק כלפי פנים התא. SR‑THAP משובץ עמוק במערה הפנימית הזו, בין מספר הליקסים שלרוב זזים במהלך מחזור ההובלה. הוא תופס שלושה כיסים קטנים בעלי אופי כימי שונה, ומתחבר לרשת של קשרי מימן ומגעים הידרופוביים. מיקום זה למעשה תוקע את הנשא כך ש‑GABA והיונים לא יכולים להשלים את מסעם. המחברים מראים שמספר חומצות אמינו ספציפיות המצפות את המערה הזו שונות בין GAT3 לקרוביו; החלפת אחת מהשיירים האלה משנה הן את פעילות ההובלה והן את עוצמת ה‑SR‑THAP, וכך מסבירה מדוע המעכב סלקטיבי הרבה יותר ל‑GAT3 מאשר ל‑GAT1 או לנשאים קרובים אחרים. 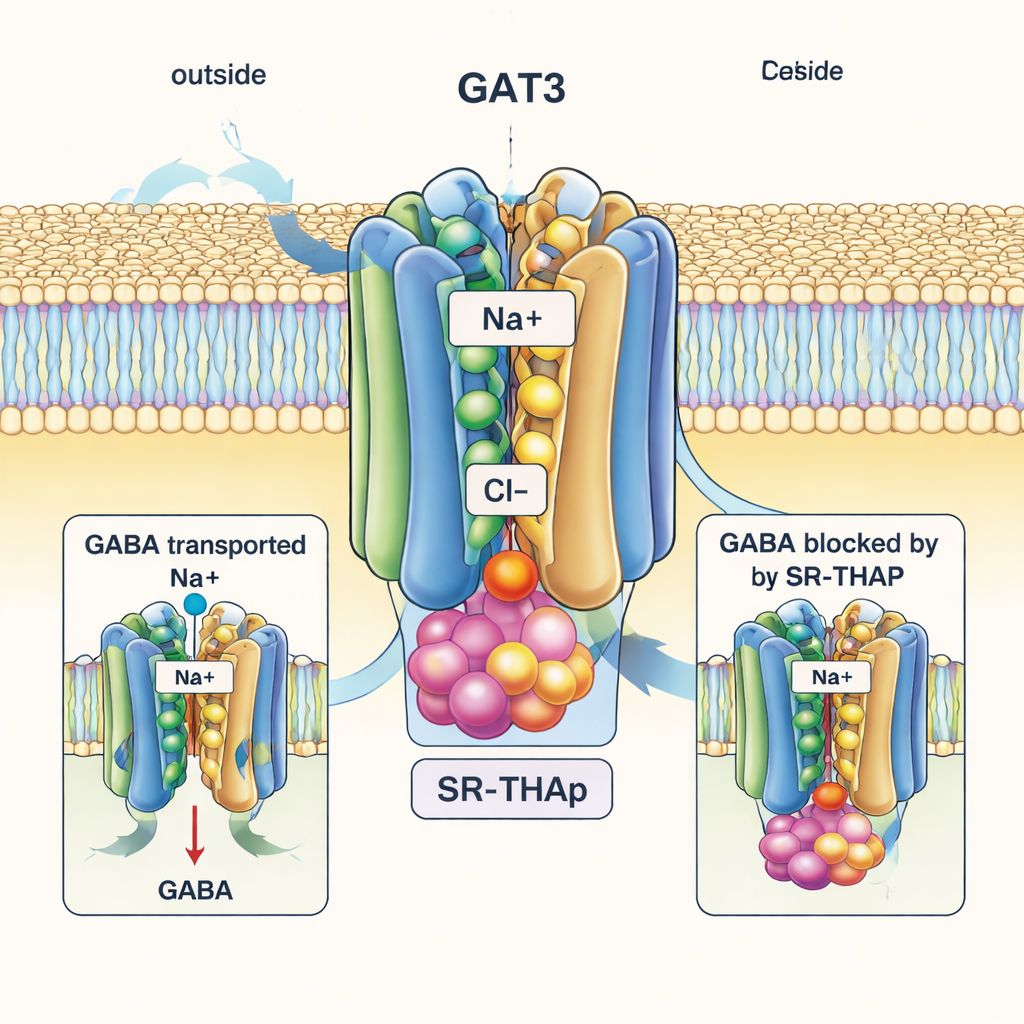
פתיחת דלתות לתרופות חדשות לאפילפסיה ולבריאות המוח
ביחד, המבנים הללו מגלים כיצד GAT3 מחליף בין צורות שונות כדי להזיז GABA, וכיצד SR‑THAP מנצל כיס פנימי פחות שמור כדי להקפיא את המחזור הזה. עבור הקוראים שאינם מתמחים, הנקודה המרכזית היא שהמחקר מספק תכנית מולקולרית מפורטת לכיבוי בררני של GAT3. תרכובות כאלה יכולות להעלות את רמות ה‑GABA המרגיעות בצורה מתוחכמת יותר מאשר תרופות קיימות, וייתכן שיובילו לטיפולים חדשים או לכלי מחקר באפילפסיה, שיקום לאחר שבץ, מחלת אלצהיימר ומצבים אחרים שבהם האיתות המעכב מופר.
ציטוט: Mortensen, J.S., Bavo, F., Jensen, M.H. et al. Structural basis for selective inhibition of human GABA transporter GAT3. Nat Commun 17, 1774 (2026). https://doi.org/10.1038/s41467-026-68479-0
מילות מפתח: נשא GABA, GAT3, אפילפסיה, cryo‑EM, עיכוב מוליך עצבי