Clear Sky Science · he
מערכות עריכת בסיסים מפוצלות בתיווך הטרודימרים סליל‑לולאה מאפשרות החלפות נוקלאוטיד גמישות וחזקות
תיקון DNA עם תופעות לוואי מועטות יותר
מחלות רבות נגרמות מטעות טיפוגרפית קטנה ב‑DNA שלנו — טעות של אות בודדת שיכולה להוביל להשלכות מסכנות חיים. למדענים יש כלים רבי‑עוצמה, שמכונים עורכי בסיסים, שיכולים לתקן טעויות כאלה מבלי לחתוך את ה‑DNA, אך כלים אלה גדולים וקשים למסירה בטוחה לגוף. מאמר זה מציג שיטה חדשה לפצל עורכי בסיסים לחלקים קטנים וחכמים יותר שעדיין פועלים בעוצמה שווה או אפילו טובה יותר מהמקור, ופותחים נתיבים חדשים לטיפול במחלות גנטיות בכבד, בשרירים ובאיברים נוספים.
מדוע הגודל מהווה בעיה לכלי תיקון גנים
עורכי בסיסים משלבים חלקים של מערכת CRISPR עם אנזימים שיכולים להחליף אות אחת ב‑DNA באחרת, כגון החלפת A ב‑G או C ב‑T. החלפות מדויקות אלה מבטיחות טיפולים למצבים כמו כולסטרול גבוה או דיסטרופיית שרירים. עם זאת, כלי מסירה מובילים לגנים, הווירוס הנקרא adeno‑associated virus (AAV), יכול לשאת רק כ‑4.7 אלף זוגות בסיסים, בעוד שעורכי הבסיס הסטנדרטיים גדולים יותר. עבודות קודמות ניסו לפצל את העורכים בעזרת אינטאינים — “מספריים” חלבוניים מיוחדים — או על ידי כיווץ עם אנזימים מוקטנים, אך גישות אלה לעתים הפחיתו יעילות, הוסיפו מורכבות בעיצוב או הגבילו היכן בגנום הכלים יכולים לפעול.
שימוש ב"וולקרו" מולקולרי כדי להרכיב מחדש את העורך
כדי לפתור זאת, החוקרים תכננו עורך בסיס מפוצל שמוחזק יחד בעזרת רוכסני חלבון קטנים הידועים כהטרודימרים סליל‑לולאה — כמו חתיכת וולקרו מולקולרית. הם הפרידו את עורך הבסיס לשתי יחידות: אחת נושאת את ה‑Cas9 nickase שמכוון ל‑DNA והשנייה נושאת את האנזים לעריכה. פפטידים סליל‑לולאה קצרים על כל חצי מחפשים זה את זה ומתחברים ברגע ששני החצאים מגיעים לאותו מקטע DNA. כך נוצרו עורכי בסיס בסגנון סליל‑לולאה (CC‑BEs), כולל גרסאות לעריכת C (CC‑CBE), A (CC‑ABE) ווריאנטים מורכבים יותר שיכולים לבצע סוגים שונים של החלפות אותיות. 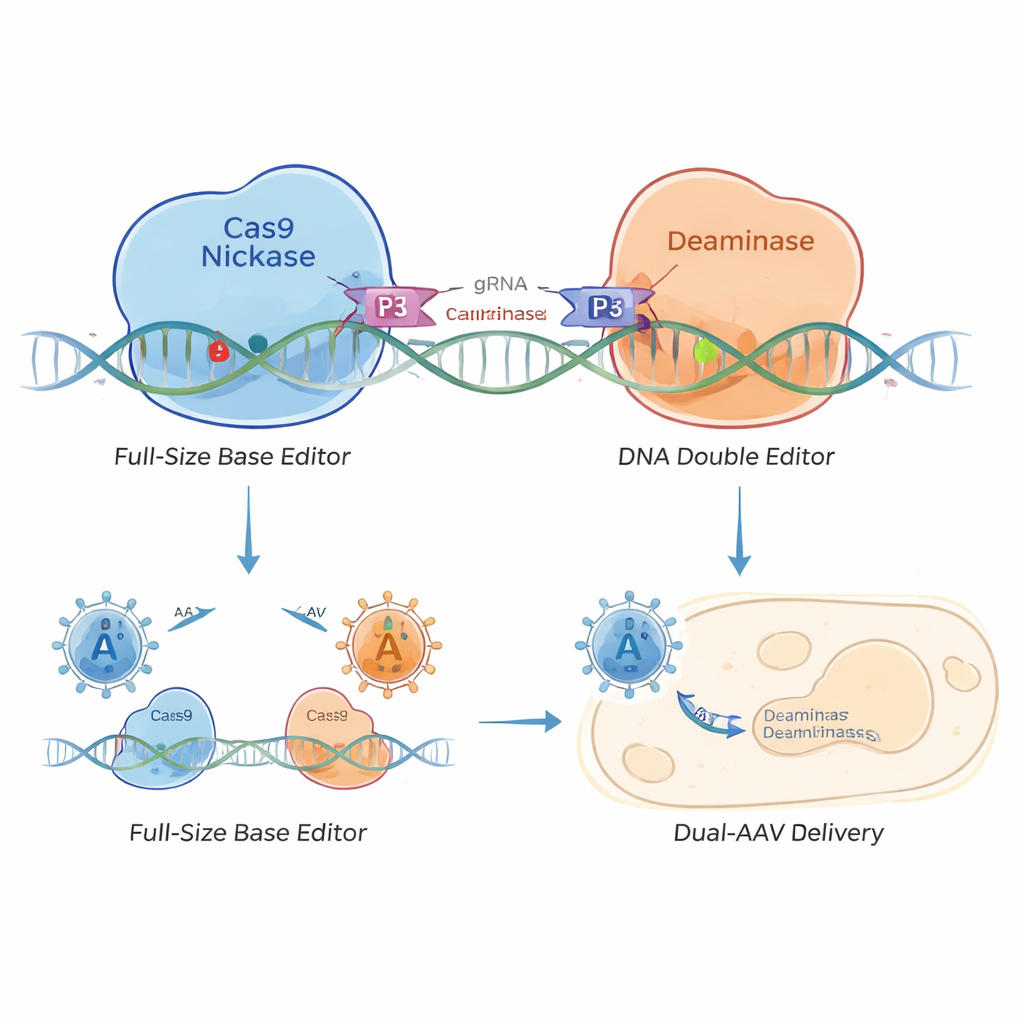
עריכה גמישה, חזקה ומדויקת
הצוות בחן את ה‑CC‑BEs בכמה סוגי תאים, כולל תאים אנושיים ותאי חזיר ראשוניים, ובצורות שונות של Cas9 שמכירות טווח רחב יותר של רצפים ב‑DNA. גרסאות ה‑CC‑CBE לא רק פעלו באמינות במספר רב של אתרים, אלא גם הפגינו "חלון עריכה" רחב יותר — כלומר יכולת לשנות תווים בטווח רחב יותר של DNA, מה שמעניק למדענים גמישות רבה יותר בבחירת מדריכי ה‑RNA. גרסאות ה‑CC‑ABE הגיעו ליעילות דומה לזו של עורכי האדנין הטובים ביותר הקיימים ולעיתים ייצרו פחות תוצרי לוואי לא רצויים. החוקרים גם התאימו את אסטרטגיית הסליל‑לולאה לעיצובים חדשים של עורכים — כגון TadCBE קומפקטי ו‑ABE9 המדויק — ומצאו ששוב הפיצול בעזרת זוגות סליל‑לולאה שומר על הביצועים או משפר אותם.
מצלחת תרבית לתאי חיים
בחשיבות פרקטית, המחברים הראו שעורכים מפוצלים אלה פועלים בתוך בעלי חיים חיים בעזרת העברה כפולה ב‑AAV, כאשר כל חלק של העורך נארז בנשא ויראלי נפרד. בעכברים, CC‑ABE שפעל נגד הגן Pcsk9 בכבד השיג עריכות A‑ל‑G בשיעורים של עד כ‑70%, תוך הורדה חדה של חלבון Pcsk9 ורמות LDL בדם ללא סימנים לנזק כבד. 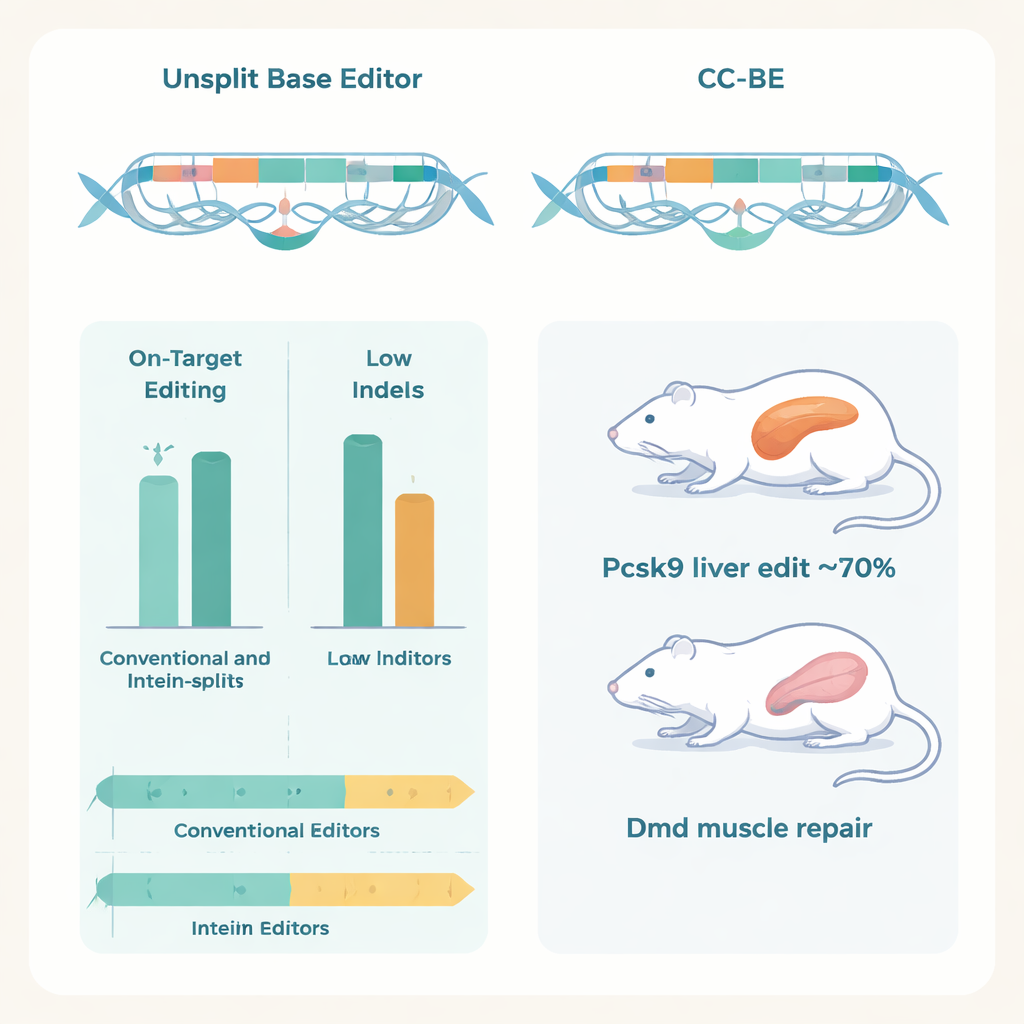
דרך חדשה לקראת תיקון DNA מעשי
בעיקרו של דבר, המחקר מציג טריק הנדסי פשוט אך חזק: שימוש ב"ווים" סליל‑לולאה קטנים כדי לפצל עורכי בסיס גדולים למודולים בגודל שמתאים ל‑AAV, שמתאחדים רק במקום שהם נחוצים. עבור קוראים לא מומחים, המסקנה היא כי כעת אפשר לארוז כלים מתקדמים לתיקון DNA בנשאים ויראליים שכבר הוכחו קלינית מבלי לוותר על דיוק או עוצמה. הגישה המבוססת סליל‑לולאה יכולה להקל על עיצוב טיפולים למגוון מחלות גנטיות של אות בודדת באיברים כמו כבד, לב ושריר, ולהביא את תיקון הגנים המכוון צעד קרוב יותר לטיפולים במציאות הקלינית.
ציטוט: Mu, S., Li, Q., Chen, M. et al. Coiled-coil heterodimer-mediated split base editing systems enable flexible and robust nucleotide substitutions. Nat Commun 17, 1765 (2026). https://doi.org/10.1038/s41467-026-68469-2
מילות מפתח: עריכת בסיסים, תרפיה גנטית, CRISPR, העברת AAV, מחלות גנטיות