Clear Sky Science · he
ניצול אימוניות מאומנת המושרת על‑ידי גלוקן לשינוי אפיגנטי ומטבולי של מאקרופאגים לחיזוק תגובת חיסון לסרטן המעי הגס
העירוי מחדש של היוצאים הראשונים להגנה בגוף
סרטן המעי הגס הוא אחד מסוגי הסרטן הקטלניים בעולם, ורוב החולים אינם נהנים מהאימונותרפיות הקיימות היום. המאמר חוקר רעיון מסקרן: מה אם נוכל "לאמן" את המערכת החיסונית המולדת — היוצאים הראשונים להגנה — לזכור סכנה ולעזור לחיסונים לפעול טוב יותר נגד גידולים במעי הגס? באמצעות סוכר טבעי ממחית שמרים, הנקרא בטא‑גלוקן, המחברים מראים כיצד ניתן לכוונן מחדש את תאי החיסון המוקדמים כך שחיסוני סרטן יעוררו התקפות חזקות וארוכות טווח יותר על הגידולים.
למה סרטן המעי הגס צריך אמצעי הגנה חדשים
סרטן המעי הגס גורם לכמעט מיליון מקרי מוות בשנה ברחבי העולם, והמקרים בקרב מבוגרים צעירים במגמת עלייה. טיפולים סטנדרטיים כמו ניתוח, כימותרפיה והקרנות יכולים להיות יעילים, אך חולים רבים חוזרים על המחלה וסובלים מתופעות לוואי חמורות. תרופות חיסוניות חדשות, כגון מעכבי נקודות בקרה, פועלות היטב רק בתת‑קבוצה קטנה של סרטן המעי הגס הנושאת ליקויי תיקון DNA מסוימים. ברוב המקרים, תרופות אלו ואפילו חיסוני סרטן ניסיוניים לא מספקים מענה מספק, כי סביבת הגידול נשלטת על‑ידי תאים ואותות המדכאים את המתקפה החיסונית.
ללמד את המערכת המולדת טריקים חדשים
תאי המערכת המולדת — ובפרט המאקרופאגים — מגיבים בדרך כלל במהירות אך לתקופה קצרה לאיומים ונחשבו חסרי זיכרון. עם זאת, עבודות בעשור האחרון חשפו את התופעה של "אימוניות מאומנת", שבה גירוי חזק ראשוני משאיר סימנים מתמשכים על תאים אלה המאפשרים להם להגיב בעוצמה רבה יותר מאוחר. החוקרים השתמשו בבטא‑גלוקן, מרכיב מדופן תאי השמרים, כדי לגרום למצב המאומן הזה. בעכברים, טיפול קצר בחלקיקי בטא‑גלוקן שלם תכנת מחדש את המאקרופאגים הן ברמת פעילות הגנים והן ברמת המטבוליזם של התא. כשבעלי החיים המאומנים קיבלו אחר כך חיסון לסרטן המעי הגס המבוסס על אדנווירוס מהונדס (שנקרא PeptiCrad), מערכות החיסון שלהם ייצרו תאי T רוצחים עוצמתיים יותר, שזיהו והתקיפו טוב יותר מטרות ספציפיות לגידול. 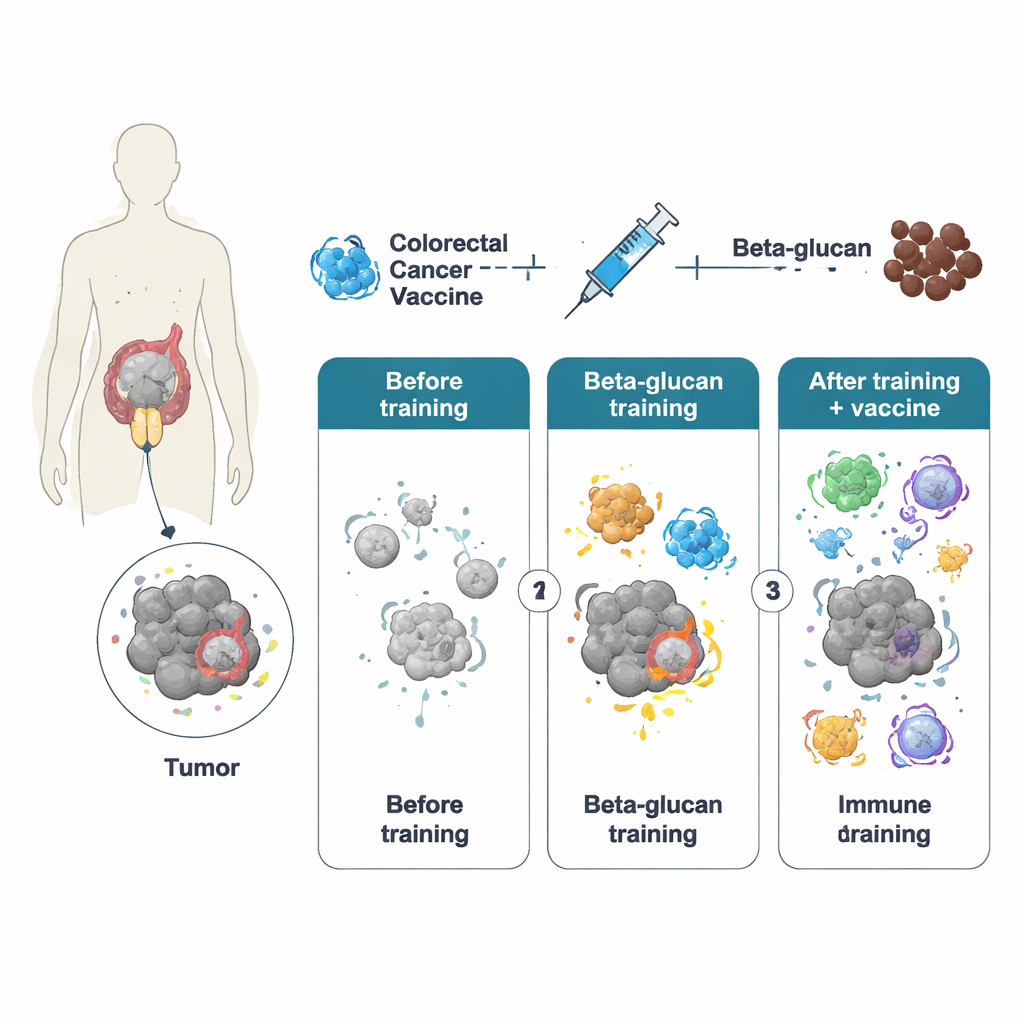
כוונון מחדש של אנרגיה ותקשורת בתוך הגידולים
בעומק המחקר, הבודקים בידדו תאי חיסון מתוך הגידולים וביצעו פרופיל מיילתמת ופעילות גנים של כל תא בנפרד. הם מצאו שמאקרופאגים מאומנים עברו למצב מטבולי עתיר פעילות המזכיר את "אפקט וורבורג", שבו תאים שורפים סוכר במהירות ומנתבים משאבים לבניית מרכיבים לצמיחה ולתפקוד. תאים אלה גם חיזקו את מטבוליזם הקריאטין — מוכר יותר מתוספי ספורט — שעזר לספק את האנרגיה הנוספת הדרושה להפקת מולקולות דלקתיות. במקביל, תגיות כימיות ספציפיות על חלבוני היסטון הקשורים ל‑DNA (בייחוד עלייה ב‑H3K4me3) סומנו על גנים המעורבים בייצור כימוקינים, ובכך נעשה נעילה של תוכנית פרו‑דלקתית ונגדית‑גידולית שנשמרת לאורך זמן.
בניית צוות רב‑שלבי חיסוני
רצף ריצוף חד‑תאי חשף העברה בשלבים בין סוגי תאי חיסון שונים בתוך הגידול. ראשית, מאקרופאגים מאומנים שחררו רמות גבוהות של שני אותות מרכזיים, CXCL9 ו‑CXCL10, שגוררים תאי טבעיים רצחניים (NK) באמצעות הקולטן CXCR3. לאחר שנקלטו, תאי ה‑NK לא רק הרגו תאים סרטניים; הם גם הפרישו גורם שליח נוסף, CCL5, שגירש תת‑קבוצה מיוחדת של תאי דנדריטית הידועים כ‑cDC1. תאי דנדריט אלה מצטיינים בהצגת חתיכות גידול לתאי T. כתוצאה מכך, יותר תאי CD8 הפכו פעילים והועברו למצב של תאי זיכרון אפקטוריים — תאים שמגיבים במהירות ובעוצמה כשהם נתקלים מחדש בגידול. חסימת שימוש בקריאטין, ניכוי מאקרופאגים או תאי NK, או הפרעה במסלולי הכימוקינים הללו החלישו את שליטת הגידול, מה שמדגיש עד כמה הצלחת החיסון תלויה במעגל המאקרופאג–NK–דנדריטי–תאי T. 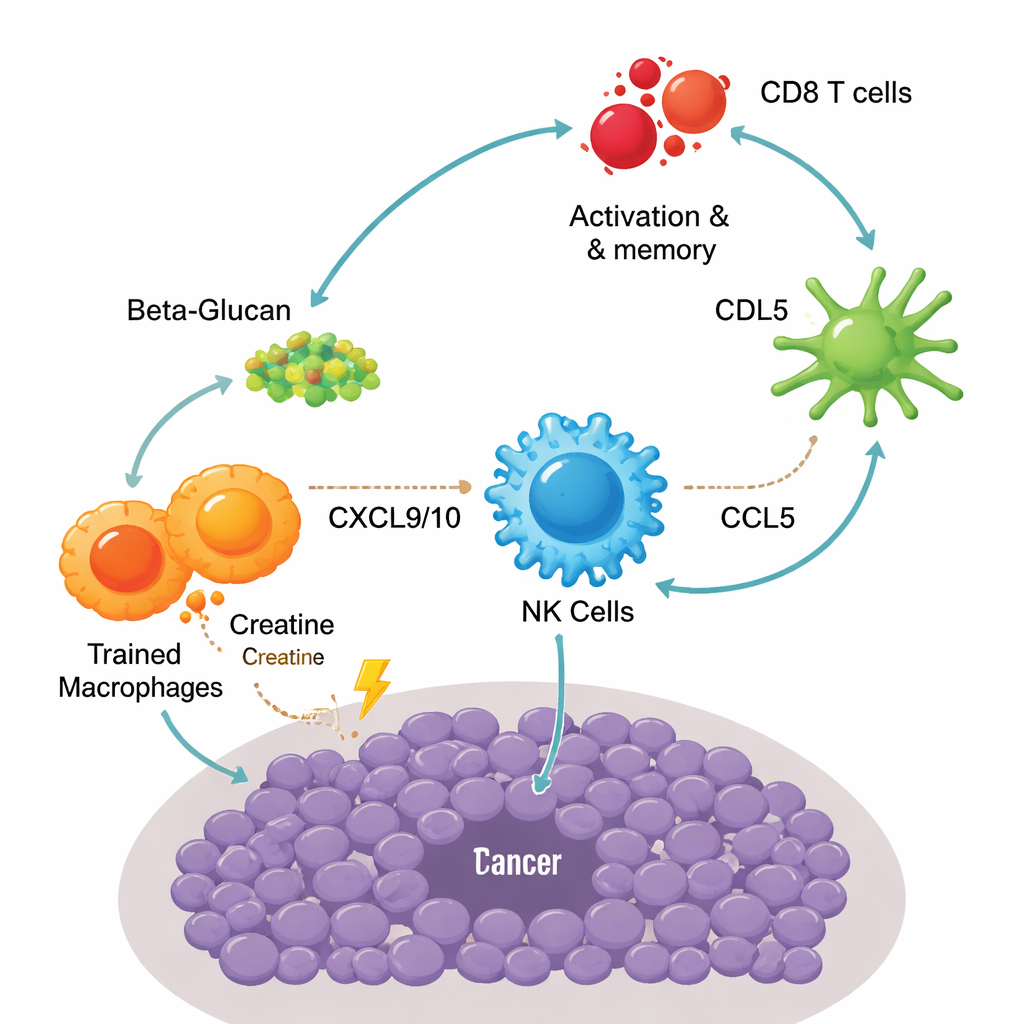
ממודלי עכבר לאורגנואידים של גידולים אנושיים
הקבוצה בחנה את הגישה במספר מודלים של עכבר לסרטן המעי הגס, כולל סוג עקשן במיוחד שעמיד לאימונותרפיות מקובלות. בכל מקרה, שילוב האימון בבטא‑גלוקן עם החיסון האט את גדילת הגידול ביתר יעילות מאשר כל טיפול לבדו. חשוב מכך, הם התקדמו מעבר לעכברים: תאי דם אנושיים שנחשפו לבטא‑גלוקן הפכו מסוגלים יותר להגיב לפפטיד חיסון לסרטן המעי הגס, והפיקו יותר ציטוקינים מעוררי חיסון. כאשר תאים חיסוניים מאומנים אלה הורחבו ושותלמו עם אורגנואידים מיקרוסקופיים שמקורם במטופלים עם סרטן המעי הגס, הם הרגום יותר תאי סרטן בהשוואה לתאים לא‑מאומנים. הוצאת מונוציטים ומאקרופאגים אנושיים מהמערכת מחקה את היתרון הזה, ואישרה שתאים מאומנים אלה הם מארגנים חיוניים ולא פשוט רוצחים ישירים של הגידול.
מה יכול הדבר להעיד על חיסוני סרטן בעתיד
במונחים פשוטים, העבודה מראה שסוכר בטוח שמקורו בשמרים יכול "לאמן" תאי חיסון מולדת לתמוך בחיסון יעיל יותר נגד סרטן המעי הגס. על‑ידי כוונון מחדש של אופן השימוש של מאקרופאגים באנרגיה ואילו גנים הם משאירים מוכנים לפעולה, אימון בבטא‑גלוקן מפעיל אפקט דומינו: מאקרופאגים מזמינים תאי NK, תאי NK מגייסים תאי דנדריט מומחים, וביחד הם בונים צבא חזק יותר של תאי CD8 זיכרוניים. בעוד שנדרשים ניסויים קליניים נוספים לבחינת בטיחות, תזמון והשילובים הטובים ביותר של חיסונים, אימוניות מאומנת מתבררת כאן כאסטרטגיית אדג'ובנט מבטיחה להפוך יותר גידולים קרים ומדכאים של המעי הגס לכאלה שהמערכת החיסונית יכולה לזהות ולשלוט בהם.
ציטוט: Hamdan, F., Gandolfi, S., D’Alessio, F. et al. Leveraging glucan-induced trained immunity for the epigenetic and metabolic rewiring of macrophages to enhance colorectal cancer vaccine response. Nat Commun 17, 1757 (2026). https://doi.org/10.1038/s41467-026-68466-5
מילות מפתח: אימונותרפיה לסרטן המעי הגס, אימוניות מאומנת, בטא‑גלוקן, מאקרופאגים ותאי NK, חיסוני סרטן