Clear Sky Science · he
DKK1 ו‑NEDD4 שמקורם בתאי הסרעפת העצבית ממודלים אות ה‑Wnt בשדה הלב השני לתיאום התפתחות נתיב היציאה
למה בוני הלב הקטנים חשובים
הלב של העובר בשלביו המוקדמים מתחיל בצינור פשוט, אך עליו במהירות לשנות צורה ולהתפתח לאיבר מסובך ששולח דם גם לגוף וגם לריאות. טעויות עדינות בתהליך הבנייה הזה יכולות לגרום למומים מולדים חמורים, כולל מצבים שמחייבים ניתוח זמן קצר לאחר הלידה. המחקר חושף כיצד שתי קבוצות תאים מתקשרות זו עם זו בעיצוב מסלול היציאה המרכזי של הלב, ומגלה שגיאה מולקולרית שיכולה לתרום למחלות לב מולדות בעכברים ובאנשים.
שתי קבוצות שבונות את מסלול היציאה של הלב
החלק של הלב שמוביל דם מן החדרים החוצה — נתיב היציאה — מתפתח מאזור הנקרא השדה הלב השני. תאים כאן חייבים להישאר כ"פרוגניטורים" גמישים זמן מספיק כדי להתווסף לנתיב היציאה המתפתח, ואז לעבור ההתבגרות לשריר בלב בזמן המתאים. סמוך להם נעים תאי הסרעפת העצבית, אוכלוסייה נודדת שעוזרת לבנות את העורקים הגדולים והמיתרים. עבודות קודמות הציעו שתאי הסרעפת העצבית משפיעים על השדה הלב השני, אך לא היה ברור כיצד מתבצעת התקשורת הזו.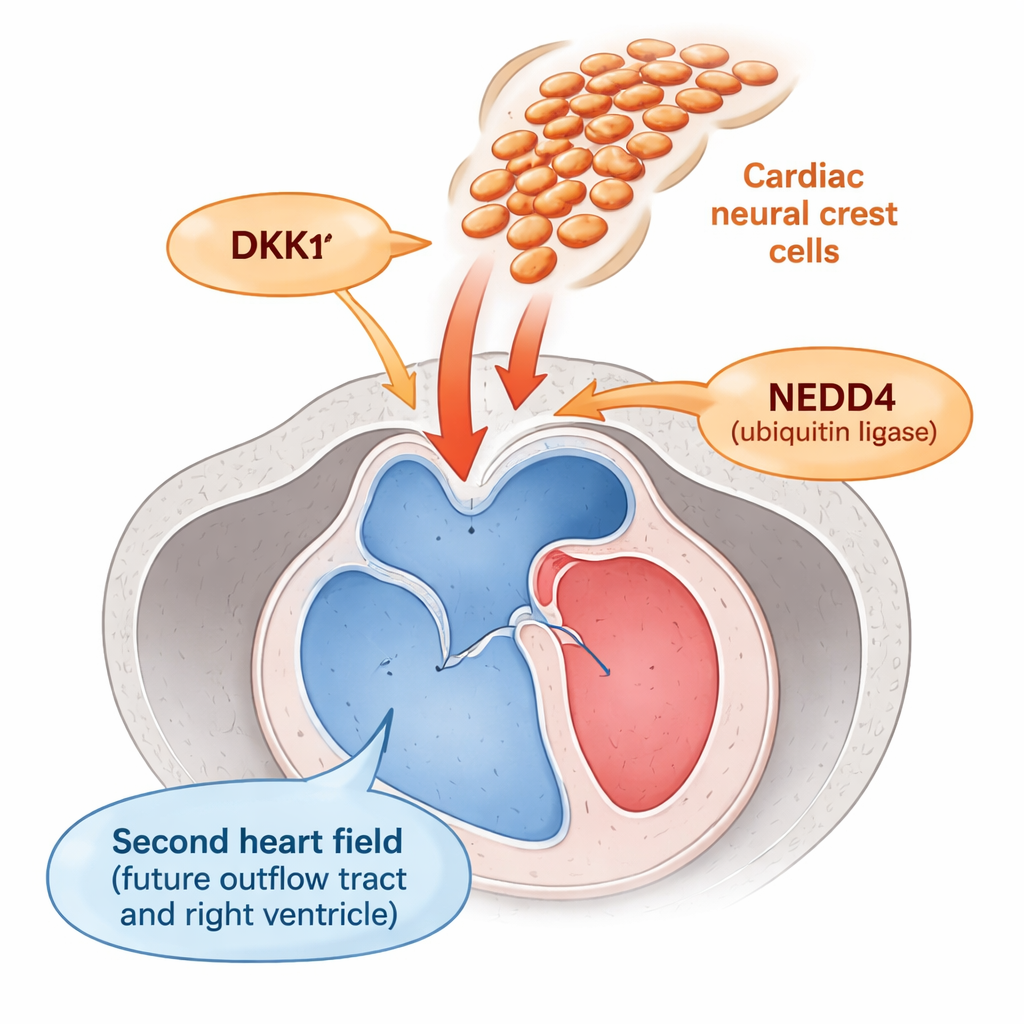
מנורה מולקולרית למידת אותות הגדילה
המחברים גילו שתאי הסרעפת העצבית פועלים כמו מנורת דימר לאות גדילה מרכזי בשם Wnt, שמשמר את חלוקת הפרוגניטורים ומעכב את בשלותם. הם מצאו שתאי הסרעפת העצבית מהווים מקור עיקרי ל‑DKK1, חלבון מוקרן קטן שמכבה את איתות ה‑Wnt בתאים סמוכים. DKK1 עצמו נשלט בדרך כלל על ידי NEDD4, חלבון המסמן את DKK1 למיחזור או לפירוק. בעוברים של עכברים שאיבדו את Nedd4 באופן ספציפי בתאי הסרעפת העצבית נצבר DKK1 ברמות בלתי תקינות. עודף זה של DKK1 דימר את פעילות ה‑Wnt בשדה הלב השני השכן, כפי שנמדד על ידי ירידה בבטא‑קטנין גרעינית — אינדיקטור סטנדרטי לאיתות Wnt — ורמות נמוכות יותר של מספר גנים הרגישים ל‑Wnt.
כשהזמנים משתבשים, הגיאומטריה של הלב נכשלה
יותר מדי DKK1 ופחות מדי Wnt הביאו לתוצאה ברורה: תאי השדה הלב השני החלו להפוך לשריר לב מוקדם מדי. סמנים של שריר בשלות הופיעו מוקדם באזור הפרוגניטורים הזה, ונשארו פחות תאים בלתי מבוססים שיכולים להאריך את נתיב היציאה. במעקב אחר תאים מתחלקים לאורך זמן הצוות הראה שפחות תאי שדה הלב השני נוספו לנתיב היציאה במוטנטים. כתוצאה מכך, נתיב היציאה היה קצר יותר והסתובב בצורה לא נכונה, מה שהוביל לחוסר יישור בין העורקים הגדולים לחדרים. שגיאות מבניות אלה דמו למומים קונוטרונקאליים בבני אדם כגון חדר ימין עם יציאות כפולות ומומים קרובים הנראים גם בעכברים עם חסר מושלם של Nedd4.
הוכחת תפקיד האות וקשר למחלות אנושיות
כדי לאשר ששינוי אותות ה‑Wnt אכן גרם לבעיות הללו, החוקרים נערכו להתערב בכיוון השליח באמצעות תרופות בעכברות הרות. חסימת Wnt בעוברים בריאים הובילה לאותה התבגרות מוקדמת ולפגמים בסיבוב כפי שנראו כאשר Nedd4 הוסרה, בעוד שהורדת עותק הגן Dkk1 ברקע של חוסר Nedd4 הצילה חלקית את גודל וזוית נתיב היציאה. לבסוף זיהו החוקרים ילד עם טטראולוגיה של פאלוט שנשא שינוי תורשתי נדיר ב‑NEDD4 שהחליש את יכולתו לתייג את DKK1 לפירוק. עכברים מהונדסים לשאת את אותו וריאנט של Nedd4 פיתחו מומים בדופן החדר הימני ובמחיצה, מה שתומך ברעיון ששיבוש בקרה על ידי NEDD4–DKK1 יכול לתרום למחלות לב מולדות אנושיות.
מה זה אומר לגבי הבנת מומים בלב
ללא מומחיות מיוחדת, המסר המרכזי הוא שמסלול היציאה של הלב תלוי בדיוק הזמנים שבו אבני הבנייה מפסיקות להתחלק ומתחילות להפוך לשריר. התזמון הזה נשלט לא רק מתוך רקמת הלב עצמה, אלא גם על ידי תאי הסרעפת העצבית השכנים שמכווננים בדייקנות את אות הגדילה דרך צמד החלבונים NEDD4–DKK1. כאשר מנורת הדימר המולקולרית הזו תקועה ברמה נמוכה מדי, נתיב היציאה נבנה פחות מדי ומאורגן בצורה לא נכונה, מה שמוביל למומים מולדים חמורים. על ידי מיפוי הנתיב הזה וקישורו לווריאנט גנטי אנושי, המחקר מספק רמזים חדשים לאופן שבו כמה מומים לב מולדים נוצרים ומצביע על מטרות מולקולריות פוטנציאליות לאבחון או להתערבות בעתיד.
ציטוט: Wiszniak, S., Alankarage, D., Lohraseb, I. et al. Neural crest cell-derived DKK1 and NEDD4 modulate Wnt signalling in the second heart field to orchestrate outflow tract development. Nat Commun 17, 1751 (2026). https://doi.org/10.1038/s41467-026-68459-4
מילות מפתח: מום מוחי לב מולד, התפתחות הלב, תאי הסרעפת העצבית, אותות Wnt, נתיב יציאת הלב