Clear Sky Science · he
מחיקה נפוצה ב‑DNA שמשנה את ה‑3’UTR של mdr1 מקושרת להפחתת הרגישות למפקלין בפרזיטים של P. vivax ממטופלים בקמבודיה
מדוע מחקר המלריה הזה חשוב
עבור אנשים החיים באזורים אנדמיים למלריה או מטיילים אליהם, תרופות יעילות הן קו חיים. עם זאת, מפריזיטים שגורמים למלריה יש יכולת להתפתח כל הזמן ולמצוא דרכים לשרוד טיפול. המחקר מתמקד ב‑Plasmodium vivax, הגורם העיקרי למלריה מחוץ לאפריקה, ומגלה שינוי גנטי דק שעלול כבר לסייע לפרזיט לשאת עמידות לתרופה חשובה אחת — מפקלין. הבנת השינוי כעת יכולה לסייע לרשויות הבריאות להקדים תרופה לעמידות מתפתחת.
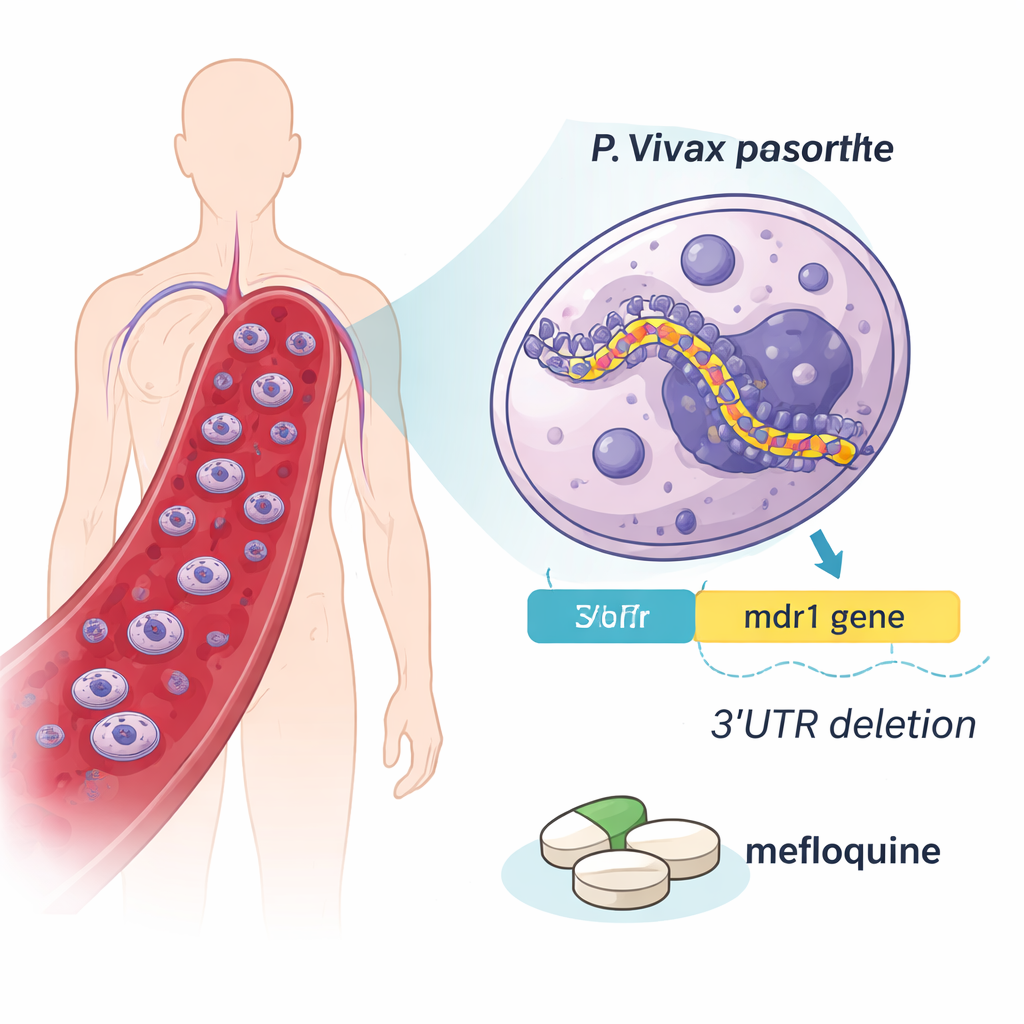
פרזיט עיקש ואופציות טיפול הולכות ונהיות מצומצמות
המלריה בבני אדם נגרמת על ידי מספר פרזיטים קרובים, אך P. vivax קשה במיוחד להשמדה. הוא יכול להיעלם בכבד למשך חודשים לפני שיחזור לדם, ולעתים מעגל בדם ברמות נמוכות מדי עבור בדיקות סטנדרטיות. במשך עשרות שנים התרופה הראשית כלורוקוין פעלה היטב נגד P. vivax, אך סימנים לעמידות התפשטו. כתוצאה מכך, ארגון הבריאות העולמי ממליץ כיום להשתמש בטיפולים משולבים מבוססי ארטימיזין (ACTs), שמצמדים תרופה מהירה עם שותף ארוך-טווח כמו מפקלין. מאחר שתרבות מעבדה של P. vivax מאתגרת, מדענים מסתמכים במידה רבה על דגימות מטופלים ועל רמזים גנטיים כדי לעקוב אחר תגובת הפרזיט לתרופות אלה.
חתיכת DNA קטנה שנעדרה בגן מרכזי של עמידות לתרופות
החוקרים רצפו את הגנומים של 206 דגימות P. vivax שנלקחו ממטופלי מלריה בקמבודיה בין 2021 ל‑2023. הם חיפשו מקטעי DNA שנמחקו או הוכפילו. בין סידורי השינויים הרבים, אחד בקע החוצה: יותר מ‑80% מהפרזיטים נשאו מחיקה קטנה של DNA שממוקמת מיד אחרי סוף אזור הקידוד של גן בשם mdr1 (multidrug resistance 1). גן זה מקודד לחלבון נשא שיכול לשאוב תרכובות שונות, כולל תרופות, דרך ממברנה בתוך הפרזיט. שלא כמו מוטציות שתוארו בעבר, מחיקה זו באורך 837 זוגות בסיסים לא שינתה את רצף החלבון עצמו. במקום זאת היא נמצאת באזור המכונה 3' untranslated region (3'UTR), מקטע שאינו מתורגם לחלבון אך יכול להשפיע בעוצמה על כמות החלבון שמיוצרת בסופו של דבר.
מחיקות עצמאיות והודעות משנה משתנות מאותו גן
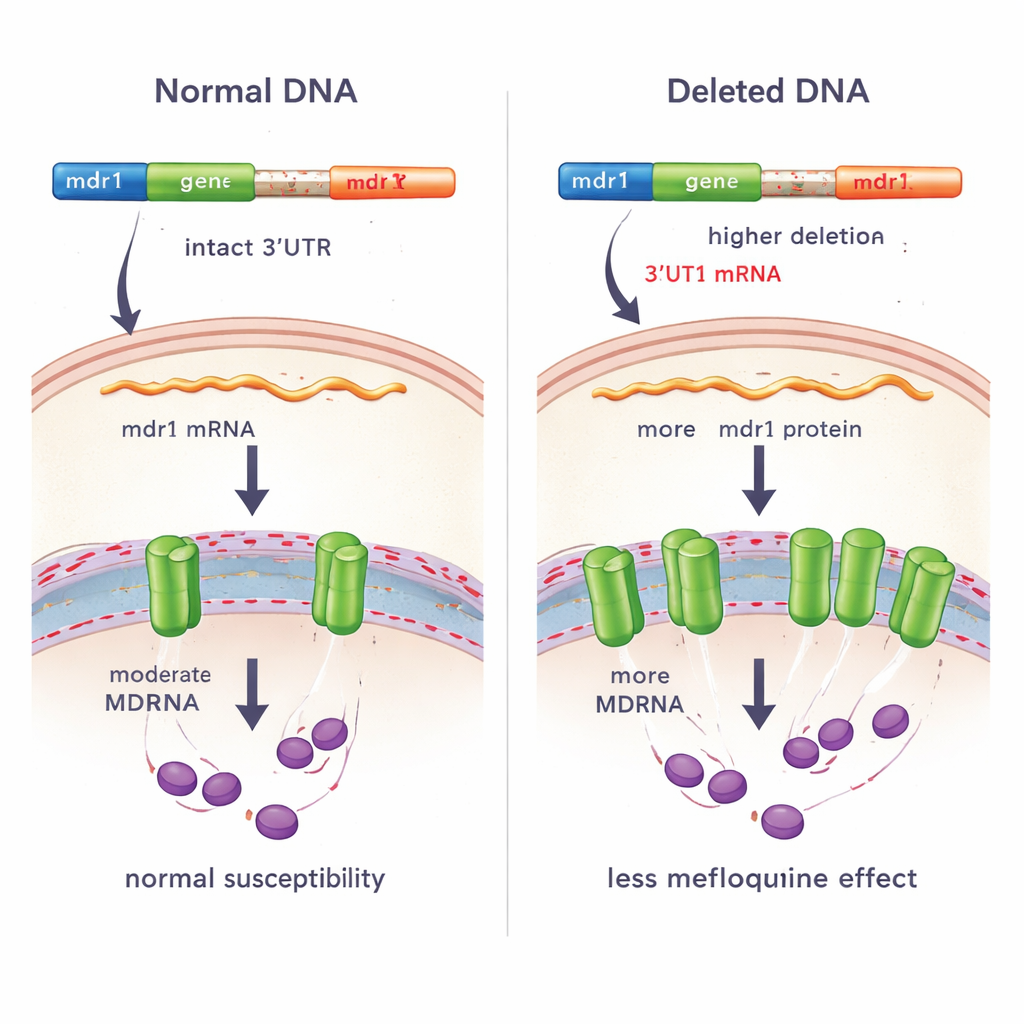
כדי לבדוק האם שינויים דומים מופיעים במקומות אחרים, הצוות ניתח מחדש כמעט 830 גנומים של P. vivax מ‑25 מדינות. הם גילו מחיקה נוספת, קצרה יותר, החופפת לאותו אזור יורד של mdr1 בפרזיטים מדרום אמריקה. השוואות מפורטות ובדיקות PCR מאשרו שמחיקות דרום מזרח אסיה ודרום אמריקה היו שונות זו מזו, מה שמרמז שהן הופיעו באופן עצמאי — אינדיקציה שעשויה להצביע על ברירת מין שמעדיפה שינויים באזור הרגולטורי הזה. באמצעות רצף RNA על 95 זיהומי קמבודיה הראו החוקרים כי פרזיטים עם המחיקה ייצרו גרסה חלופית של ה‑mRNA של mdr1, עם 3'UTR שונה. לאחר התאמת אורך הטרנסקריפט, פרזיטים נשאי המחיקה הכילו כמעט פי שניים mRNA של mdr1 לעומת אלה ללא המחיקה, מה שמעיד שה‑DNA החסר או רצף 3'UTR החדש מסייע לייצוב או להגברת הביטוי של הגן.
קישור המחיקה לתגובת לתרופות בחולים ובבדיקות מעבדה
מכיוון ש‑mdr1 הושם בקשר לעמידות למספר תרופות אנטי-מלריה, הצוות חקר האם המחיקה קשורה לאופן שבו הפרזיטים הגיבו לטיפול. הם השוו תחילה את קצב ניקוי הפרזיטים מהדם של מטופלים לאחר טיפול בארטסונאט. מבין 167 זיהומים, לא נמצאה הבדל מובהק בקצב הניקוי בין פרזיטים עם המחיקה וללאה, מה שמרמז שהשינוי הגנטי הזה אינו משפיע ישירות על הרגישות לארטסונאט עצמו. עם זאת, בקבוצת קטנה יותר של 14 זיהומים שבה החוקרים מדדו גידול פרזיטים בנוכחות מפקלין מחוץ לגוף, פרזיטים נשאי המחיקה נטו להציג ערכי IC50 גבוהים יותר — פירושו שדרושה כמות תרופה רבה יותר כדי לעכב את הגידול — מאשר פרזיטים ללא המחיקה. דפוס זה תואם להפחתת הרגישות למפקלין, אם כי גודל המדגם היה מוגבל.
עלייה מדאיגה לאורך זמן ומה זה יכול להעיד
כדי להבין כמה המחיקה נפוצה, המחברים סרקו 592 דגימות ארכיון של P. vivax שנאספו ברחבי קמבודיה מ‑2014 עד 2024. לפני שהוחדרה השימוש במפקלין כחלק מ‑ACTs לטיפול ב‑vivax סביב 2016–2017, כ־30% מהפרזיטים נשאו את המחיקה. אחרי המעבר, התדירות עלתה מעל 60% ואז התייצבה, מגמה שהייתה חזקה סטטיסטית ונשארה גם כשמיקדו רק במזרח קמבודיה. המחיקה כבר הייתה נוכחת ברמות נמוכות לפני שהמפקלין שימש בהיקף נגד P. vivax, ייתכן בעקבות חשיפה עקיפה כאשר התרופה שומשה לטיפול ב‑P. falciparum או מפני שהשינוי משפיע גם על תגובות לתרופות אחרות. יחד עם דיווחים אחרונים על ניקוי פרזיטים מעט איטי יותר לאחר טיפול בארטימיזין, הממצאים מעלים חשש ש‑P. vivax בקמבודיה עלול להתקדם לעבר ירידה ביעילות של צמדי הארטסונאט–מפקלין הנוכחיים.
מה המשמעות לכך בתחום המאבק במלריה
עבור הקוראים הלא מומחים, המסר המרכזי הוא שגם כאשר גן העמידות הראשי של הפרזיט נראה שלם, שינויים זעירים ב"חוטי הבקרה" הקרובים ל‑DNA יכולים לשנות עד כמה החלבון מופעל. במקרה הזה, מחיקה נפוצה באזור שאינו מקודד של mdr1 נראית כמגבירה את פעילות הגן ומקושרת להשפעה חלשה מעט של מפקלין על P. vivax. למרות שאין עדיין ראיות ברורות לכישלון טיפול בקמבודיה, העלייה בתדירות המחיקה מצביעה על כך שלחץ תרופתי עשוי בעדינות להעדיף פרזיטים הנשאים תכונה זו. זיהוי ומעקב אחר סימני אזהרה גנטיים מעודנים כאלה מוקדם יכולים לעזור לרשויות הבריאות להתאים מדיניות תרופתית, לעצב כלים טובים יותר לסקר ולשמר את מלאי התרופות האנטי-מלריה היעיל שנשאר.
ציטוט: Ko, K., Tebben, K., Andrianinarivomanana, T. et al. A common DNA deletion altering the 3’UTR of mdr1 is associated with reduced mefloquine susceptibility in P. vivax parasites from Cambodian patients. Nat Commun 17, 1748 (2026). https://doi.org/10.1038/s41467-026-68456-7
מילות מפתח: Plasmodium vivax, עמידות לתרופות של המלריה, מפקלין, גן mdr1, קמבודיה