Clear Sky Science · he
וריאנטים פונקציונליים ב‑1p36.23 מעלים את הסיכון לסכיזופרניה על‑ידי ויסות RERE
מדוע שינויים זעירים ב‑DNA חשובים לבריאות הנפש
סכיזופרניה היא מחלת נפש קשה המשפיעה על הדרך שבה אנשים חושבים, מרגישים ומתקשרים עם אחרים. היא מועברת בחוזקה במשפחות, אך רוב השינויים הגנטיים המעורבים הם תיקונים קטנים ומפוזרים ב‑DNA שלנו. המחקר הזה מתמקד באזור כזה של הגנום ומדגים, שלב אחרי שלב, כיצד שני וריאנטים דנ‑איים עדינים יכולים לשנות את התפתחות תאי המוח והתקשורת ביניהם בדרכים שעשויות להעלות את הסיכון לסכיזופרניה. 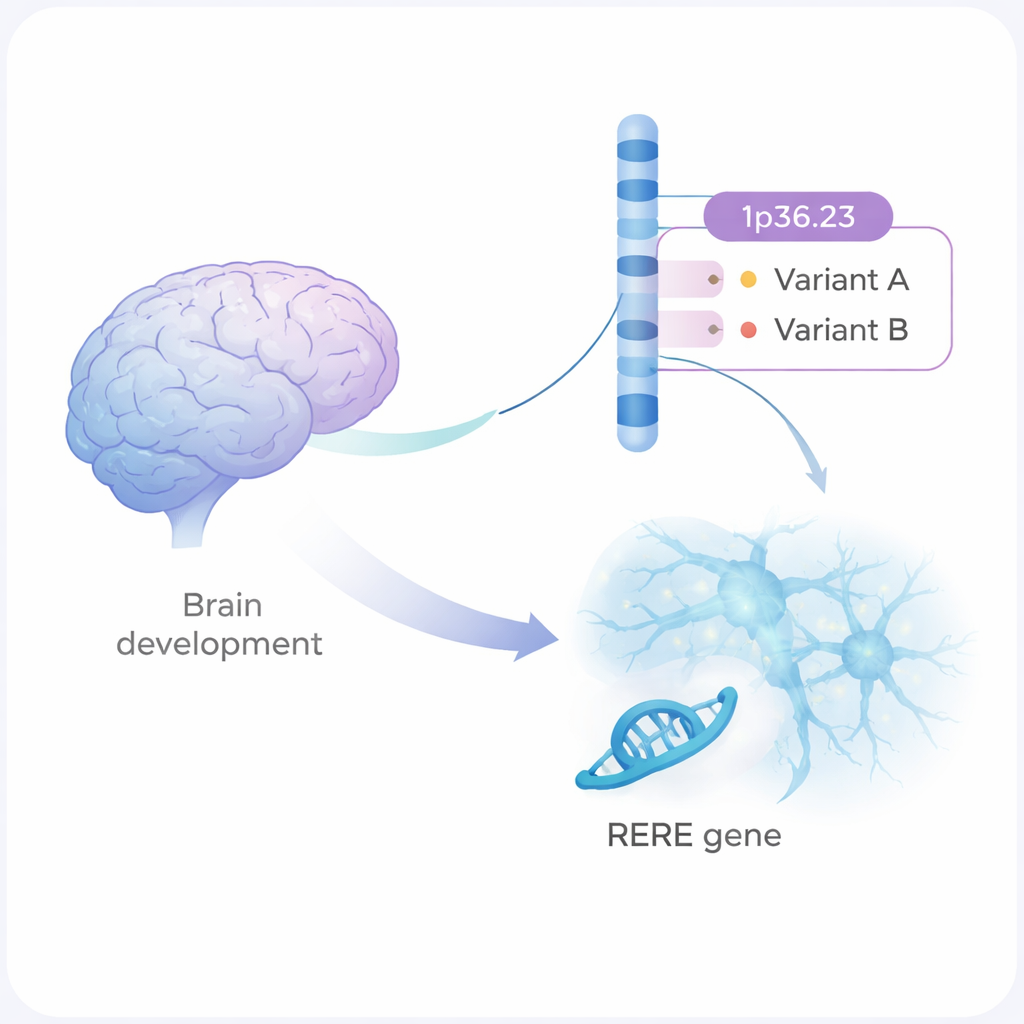
מוקד גנטי בכרומוזום 1
מחקרים גנטיים רחבי היקף זיהו יותר מ‑300 אזורים בגנום האנושי הקשורים לסכיזופרניה. אחד מהם הוא קטע ב‑DNA בכרומוזום 1, המכונה 1p36.23. עד כה לא היה ברור אילו שינויים מדויקים באזור זה, או איזה גן, גורמים להשפעה האמיתית. החוקרים שילבו גנטיקה סטטיסטית עם ניסויים במעבדה ובידלו שני וריאנטים דנ‑איים, rs159961 ו‑rs301792, הנמצאים בתוך הגן הקרוי RERE. וריאנטים אלה אינם משנים את חלבון RERE עצמו; במקום זאת הם נמצאים באזורים רגולטוריים — "מפסקי" בקרה בתוך הגן — השולטים עד כמה RERE מופעל.
כיצד וריאנטים מסכנים מעלים את עוצמת ביטוי RERE
הצוות בדק תחילה האם שני הווריאנטים האלה אכן פועלים כמתגי בקרה פונקציונליים. בעזרת מבחני דוח (reporter assays) — שבהם מקטע DNA מפעיל גן המפיק אור — הראו החוקרים כי הגרסאות המקושרות לסכיזופרניה של rs159961 ו‑rs301792 פועלות כמשפרים (enhancers) חזקים יותר בתאים דמויי עצב, אך לא בסוגי תאים לא קשורים. בדיקות קישור ביוכימיות חשפו מדוע: הצורה המסוכנת של אחד הווריאנטים מחלישה את אחיזתו של REST, חלבון שבדרך כלל מדכא פעילות גנטית, בעוד שהצורה המסוכנת של הווריאנט השני מחזקת את קשירת POLR2A, מרכיב מרכזי במכונת קריאת הגנים. יחדיו, השינויים בקשירת חלבונים אלה מגדילים את פעילות מקטעי המשפר ודוחפים את ביטוי RERE לעלייה.
מ‑RERE מוגבר לצמיחה שונה של תאי מוח
בהמשך בדקו החוקרים מה עושים רמות גבוהות של RERE בתוך המוח. הם מצאו שאנשים שמתו עם אבחנת סכיזופרניה הראו רמות גבוהות יותר של RERE ברקמת המוח שלהם בהשוואה לאנשים ללא המחלה. כדי לדמות זאת, הגדילו באופן מלאכותי את רמות RERE בתאי גזע עצביים של עכבר — התאים הבלתי בוגרים שממנו נגזרים נוירונים וגلیا. כאשר RERE יוצר בכמויות גבוהות, תאי הגזע הללו התחלקו פחות, נתקעו בשלב מאוחר במחזור התא, ויצרו פחות נוירונים בוגרים בעוד שסוגי תאים אחרים נותרו ברובם ללא שינוי. גם בתרביות נוירונים, עודף RERE שינה את דפוסי הסתעפותם והקטין את מספר וסוג הזיזיות הקטנות הקרויות קוצקי דנדריט (dendritic spines), שבהן נוצרות סינפסות. שינויים אלה תואמים ראיות ארוכות טווח שסכיזופרניה מערבת הפרעות בהתפתחות המוח ואובדן קוצים דנדריטים. 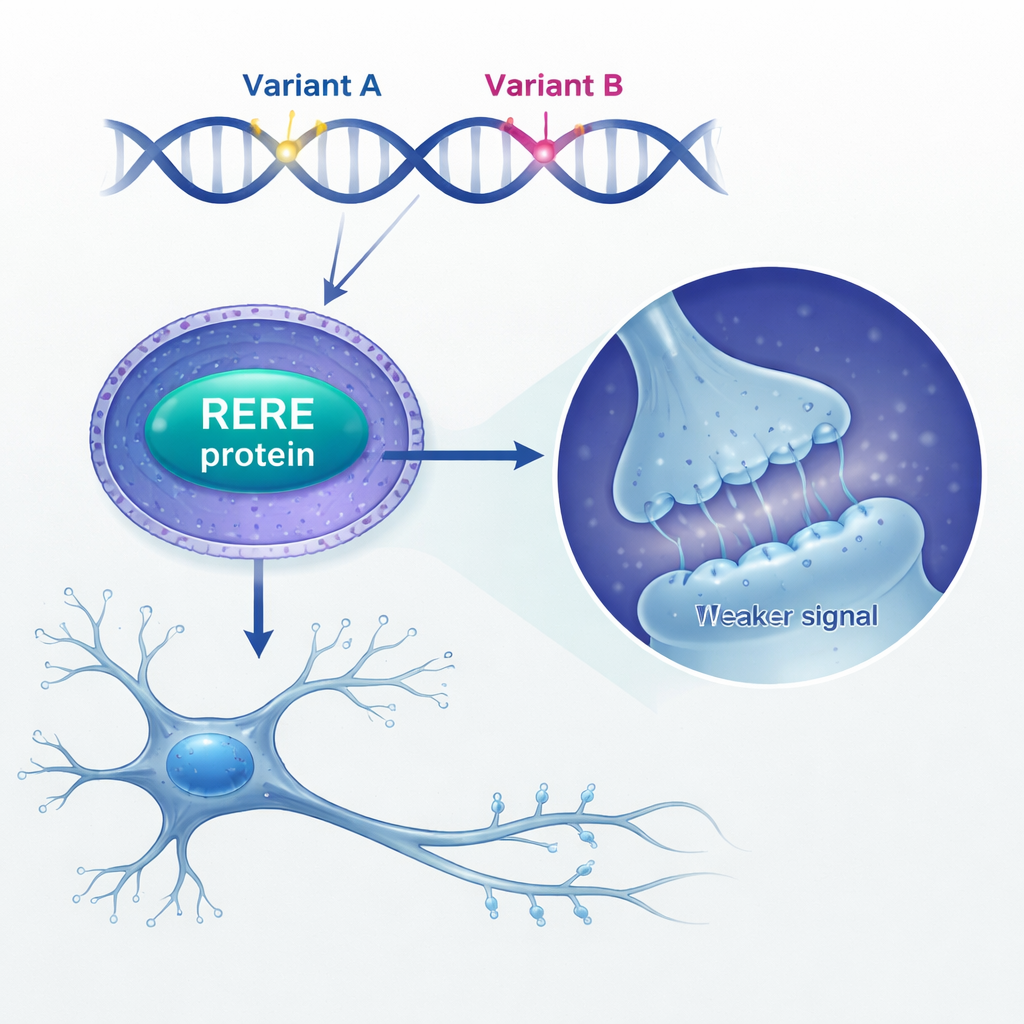
הפרעה "לשיחה" הגלוטמטרגית של המוח
בעת בחינת פעילות גנים ביתר פירוט, הצוות מצא שעודף RERE מפר את הרשתות של גנים המעורבים בגדילת דנדריטים ובמערכות איתות כימיות מרכזיות, במיוחד מסלול הגלוטמט. יעד מרכזי בלט: הגן GRIN2A, המקודד תת‑יחידה חשובה (GluN2A) של קולטני NMDA מסוג גלוטמט, שמעורבים בסכיזופרניה זמן רב. החוקרים הראו ש‑RERE פועל בשיתוף עם שני חלבונים גרעיניים נוספים, RARB ו‑RXRA, כדי להיקשר ישירות לפרומוטור של GRIN2A ולהדכאתו. בנוירונים עם עודף RERE, רמות GluN2A ירדו ורישומי חשמליות הראו זרמים סינפטיים המתווכים על‑ידי רצפטורי NMDA חלשים יותר, אף על פי שתדירות המאורעות הסינפטיים לא השתנתה. במילים אחרות, "עוצמת" האותיות המעוררות הבודדות הוסטה כלפי מטה.
קישור בין וריאנטים דנ‑איים לתפקוד המוח
על ידי שזירה של גנטיקה, ביולוגיה מולקולרית, תרביות תאים ואלקטרופיזיולוגיה, עבודה זו מציירת שרשרת סיבתית ברורה: וריאנטים מסכנים ב‑1p36.23 מחזקים אלמנטים רגולטוריים בתוך גן RERE, מה שמוביל לביטוי גבוה יותר של RERE בתאי מוח. RERE מוגבר פוגע בצמיחה ובהבשלה של נוירונים, משנה את צורתם ומספר הקוצים הסינפטיים שלהם, ומחליש איתות מבוסס גלוטמט דרך רצפטורי NMDA — במיוחד אלה המכילים GluN2A. לקורא שאינו מומחה, המסר הוא ששינויים זעירים ב‑DNA יכולים להזיז במעט את פעילותו של גן יחיד, ובעלייה מצטברת על פני תאי מוח רבים ושנים רבות זה עלול להזיז את התפתחות המוח והתקשורת העצבית מהמוטב בדרכים שתורמות לסכיזופרניה.
ציטוט: Liu, Y., Wang, J., Yang, H. et al. Functional variants at 1p36.23 confer risk of schizophrenia through modulating RERE. Nat Commun 17, 1742 (2026). https://doi.org/10.1038/s41467-026-68449-6
מילות מפתח: גנטיקה של סכיזופרניה, גן RERE, התפתחות עצבית, אותות גלוטמטרגיים, תפקוד סינפטי