Clear Sky Science · he
בקרה על גיוס טלומרז והגנה על הקצה על ידי מרכיבי ה-shelterin הנפרדים
כיצד תאים שומרים על קצוות הכרומוזומים שלהם
בכל חלוקת תא, קצות הכרומוזומים — הקרויים טלומרות — נשחקים במעט. כדי למנוע אובדן מידע גנטי חיוני, תאים משתמשים באנזים מיוחד, טלומרז, ובחבורה של חלבונים מגן שומרים על קצוות אלה. המחקר הזה חוקר כיצד שני חלבונים מתוך אלו, TPP1 ו-POT1, מנהלים את האיזון העדין בין מתן גישה לטלומרז כדי לבנות מחדש את הטלומרות לבין שמירה על קצוות הכרומוזומים סגורים ומוגנים מפני נזק.
בעיית קצוות הכרומוזום המתבגרים
טלומרות מתפקדות כמו חבילות פלסטיק בקצות שרוכי נעליים, ומונעות מהכרומוזומים להישרטט או להיתפס כשברי DNA. אם התא מפרש את קצה הכרומוזום כשבר, זה עלול להפעיל מערכות תיקון חירום שמדביקות כרומוזומים אחת לשנייה או עוצרות חלוקה תאית. יחד עם זאת, טלומרות צריכות מדי פעם להיפתח כדי לאפשר לטלומרז להאריך אותן, במיוחד בתאי גזע שחולקים פעמים רבות. ביולוגים חשבו זמן רב שהטלומרות מתחלפות בין מצב "סגור" מוגן לבין מצב "פתוח" שמאפשר לטלומרז גישה אך מסכן אותות נזק זמניים. האם שני המצבים האלו משקפים צורות פיזיות שונות של הטלומר או מנגנוני בקרה נפרדים — זו שאלה שנשארה פתוחה.
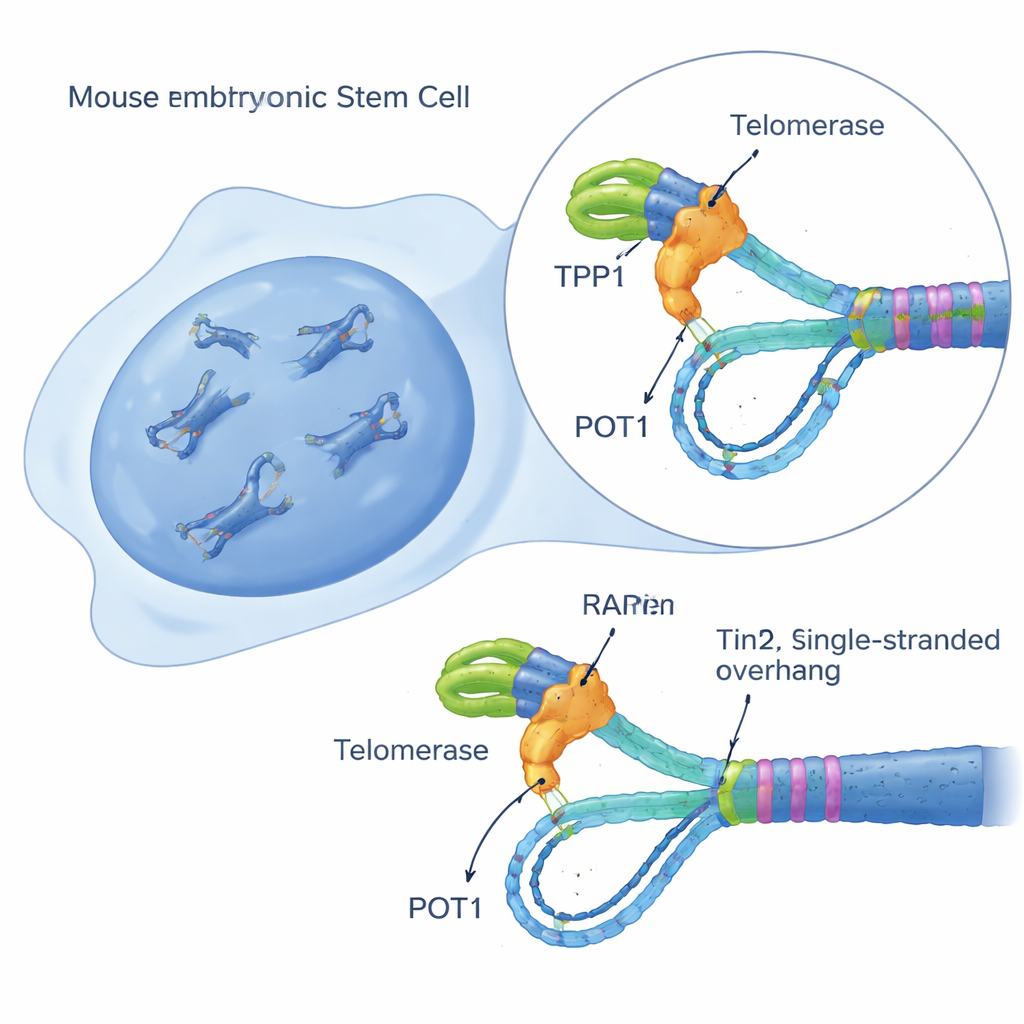
בניית חיישן פעילות טלומרז בתא בודד
כדי לפענח את התעלומה, החוקרים יצרו מבחן חי עדין ונגיש, שנקרא iTAP (inducible Telomerase Activity Probing), בתאי גזע עובריים של עכבר. הם שינו את התאים כך יפיקו תבנית RNA מעט שונה של הטלומרז רק כאשר מקבלים את התרופה דוקסיציקלין. תבנית "המוטנטית" הזו גורמת לטלומרז להוסיף רצף DNA מותאם בטלומרות שניתן להבדיל בוויזואלית מרצף הטלומר הנורמלי. באמצעות זיהוי פלואורסנטי, בלוטות DNA ושיטת רציפות שמעשירה מקטעי טלומר, הצוות יכול היה לראות ישירות, תא אחרי תא, מתי והיכן הטלומרז פעיל. חשוב לציין שהמערכת הזו לא הפגיעה בצמיחת התאים ולא עוררה תגובת נזק בעצמה, מה שאיפשר מדידות נקיות של פעילות הטלומרז בתוך תאים בריאים יחסית.
TPP1 מביא את הטלומרז, POT1 מעכב אותו
מצוידים ב-iTAP, המחברים בדקו כיצד שני חלבוני טלומרה מרכזיים, TPP1 ו-POT1, תורמים לפעולת הטלומרז. שניהם שייכים למרכיב גדול יותר הידוע כ-shelterin, שמצפה את הטלומרות. כאשר הסירו את TPP1 בעזרת כלים לעריכת גנים, הרצפים המוטנטיים בטלומר כמעט נעלמו, אף שהתבנית RNA המוטנטית של הטלומרז נוצרה ברמות רגילות. ניסויים נוספים הראו כי TPP1 חייב להתחבר פיזית למרכיב אחר ב-shelterin, TIN2, כדי לגייס את הטלומרז; שיבוש הקשר בין TPP1 ל-TIN2 כיבה את פעולת הטלומרז. באופן מפתיע, שיבוש האינטראקציה של TPP1 עם POT1 לא גרם לאפקט זה, ומחיקה של POT1 עצמה לא הפחיתה את פעילות הטלומרז. למעשה, תאים חסרי POT1 הראו עלייה מתונה בכמות הרצף המוטנטי המתווספת, מה שמרמז ש-POT1 פועל בדרך כלל כבלם — מגביל כמה פעמים הטלומרז מתחבר לטלומרות, ולא מסייע בגיוסו.
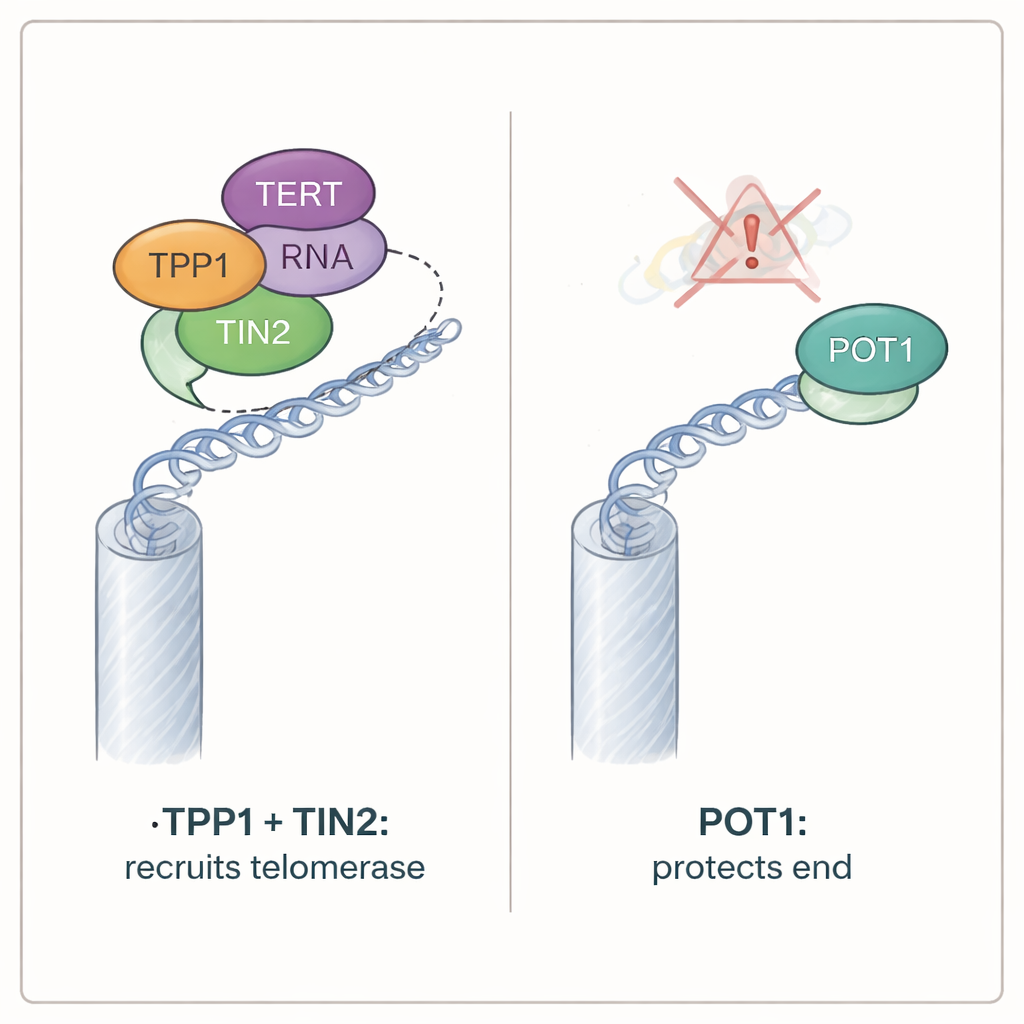
POT1 מגנה על הקצוות, בעוד ש-TPP1 עשוי להיות מיותר
אף ש-POT1 לא היה נחוץ לגיוס הטלומרז, הוא התברר כחיוני להגנה על קצוות הכרומוזומים. תאים חסרי שתי המחלוקות של POT1 בעכברים הפסיקו להתחלק במהירות והציגו את כל סימני הטלומרות החשופות: סמני נזק ל-DNA הצטברו בקצות הכרומוזומים, אנזים חישה נזק בשם ATR הופעל, וקצות הכרומוזומים הצטלבו זה בזה. לעומת זאת, תאים ללא TPP1 המשיכו לגדול והראו מעט סימנים למצוקה בטלומרות, אף שאיבדו את פעילות הטלומרז הרגילה. בדיקות נוספות הראו שתפקיד ההגנה של POT1 תלוי ביכולתו לקשור את התוספת החד-גדילית (overhang) בטלומרות. חלבוני POT1 מוטנטיים שלא יכלו עוד לאחוז ב-DNA החשוף נכשלו בדיכוי אותות הנזק, גם אם יכלו עדיין לתקשר עם TPP1. לעומת זאת, גרסאות של POT1 שיכלו לקשור את ה-overhang אך כבר לא התחברו ל-TPP1 עדיין הגנו על קצוות הכרומוזומים.
תפיסה חדשה ומודולרית של בקרה בטלומרות
ממצאים אלה מערערים את התמונה הפשוטה של מעבר בין מצב "פתוח" אחד לטלומרז ומצב "סגור" אחד של הגנה. במקום זאת, המחקר מראה כי גיוס הטלומרז והגנת הקצה נשלטים על ידי מעגלים מולקולריים נפרדים. TPP1, הפועל דרך TIN2, הוא השער הראשי שמביא את הטלומרז לטלומרות, בעוד ש-POT1 שומר באופן עצמאי על ה-DNA החשוף בקצוות הכרומוזומים ומדכא תגובות נזק. למען הקוראים הלא-מומחים: המסקנה היא שתאים אינם מסתמכים על מתג אוניברסלי יחיד בקצות הכרומוזומים. במקום זאת הם משתמשים בכנים נפרדים אך מתואמים — אחד המאפשר כניסת טלומרז, והשני שומר על הקצוות בטוחים — כדי לשמור על יציבות הגנום לאורך החיים.
ציטוט: Sandhu, R., Tricola, G.M., Lee, S.Y. et al. Control of telomerase recruitment and end protection by independent shelterin components. Nat Commun 17, 1733 (2026). https://doi.org/10.1038/s41467-026-68433-0
מילות מפתח: טלומרות, טלומרז, תאי גזע, נזק ל-DNA, הגנה על כרומוזומים