Clear Sky Science · he
Shigella flexneri מתחמקת ממערכת החיסון התאית המבוססת ספטינים באמצעות ADP‑ריבוקסנציה של חלבונים
כיצד כמה חיידקים במעיים חומקים ממערכת הביטחון הפנימית שלנו
שלשולים קשים הנגרמים על‑ידי חיידקי שיגלה ממשיכים להיות בעיה עולמית משמעותית, במיוחד בקרב ילדים קטנים. התאים שלנו אינם חסרי הגנה: הם מצוידים בכלים פנימיים היכולים ללכוד ולהשמיד מיקרובים פולשים. מחקר זה חושף כיצד Shigella flexneri, גורם מרכזי לדיזנטריה, משתמשת בטריקים מולקולריים כדי לפרק אחד מכלים אלה — ובכך לסייע לחיידק להתפשט מתא לתא במעי.
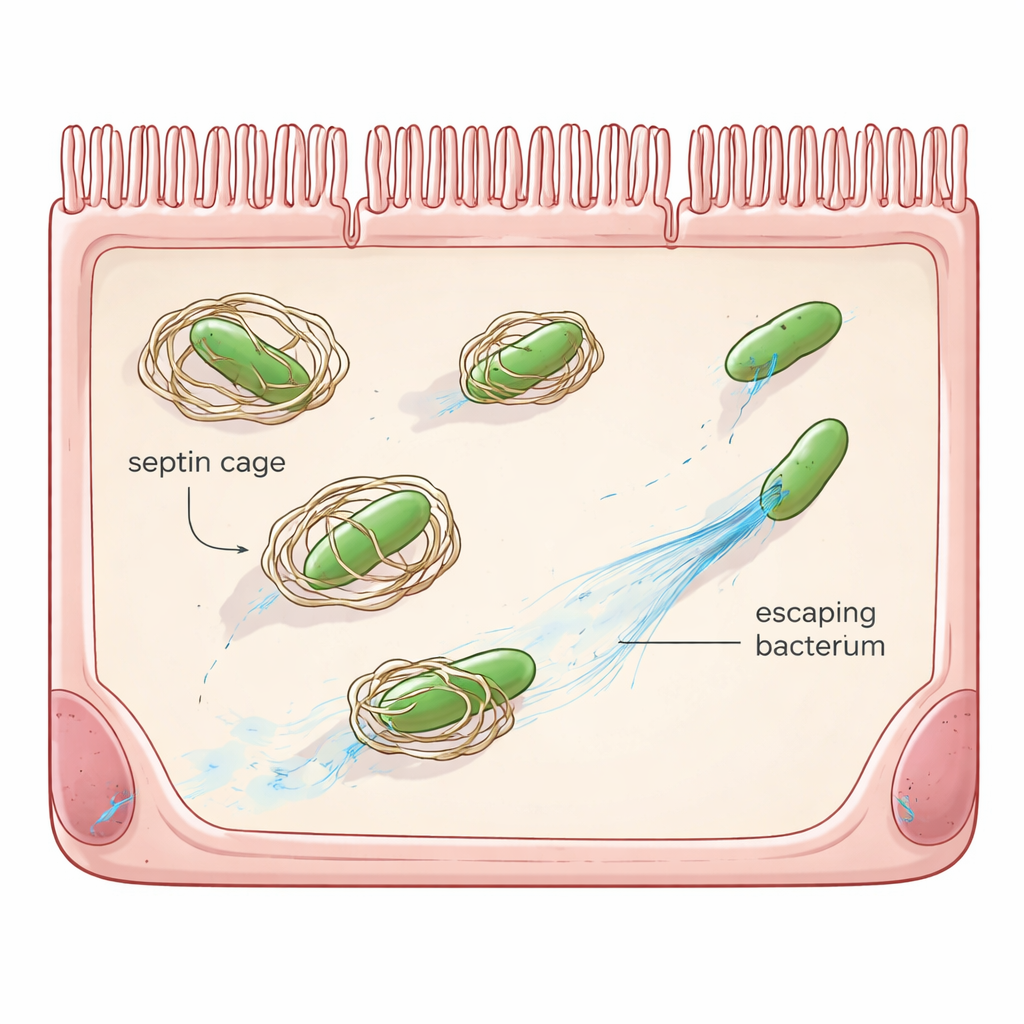
הגנת ה־"עשה זאת בעצמך" של התא
מעבר לתאי דם לבנים ונוגדנים, תאים רבים מחזיקים במערכות חירום פנימיות, המכונות חיסון תא‑אוטונומי. אחת המערכות הללו נשענת על ספטינים, משפחת חלבונים מסגרתיים שיוצרים טבעות ומבנים דמויי כלוב. כאשר שיגלה נכנסת לתא ובורחת אל הציטוזול, ספטינים יכולים להתארגן סביב החיידק, לנטרל את יכולתו לנוע ולסמן אותו להרס דרך מסלולי מיחזור תאים. עבודות קודמות הראו שלשיגלה כבר יש אמצעי נגד אחד, חלבון בשם OspG, שמסמן ספטינים לפירוק. אבל גם בהיעדר OspG, רוב החיידקים עדיין אינם נלכדים בכלוב, מה שמרמז שלשיגלה יש טריקים נוספים.
חשיפת מבקש חיידקי שני
החוקרים הפנו את תשומת לבם לקבוצת חלבונים נוספת של שיגלה, המשויכת למשפחה OspC. באמצעות גישה גלובלית למיפוי חלבונים בתאים אנושיים הם חיפשו חלבוני מאחסן שעברו שינויים כימיים בנוכחות חלבוני OspC. לצד מטרות מוכרות המעורבות בבניית חלבונים, הם מצאו שכמה ספטינים, ובעיקר אחד בשם SEPT9, סומנו בקביעות. ניסויים ביוכימיים מפורטים הראו כי שלושה חלבוני OspC יכולים לחבר ישירות תג קטן ועשיר באנרגיה, הנובע ממולקולת NAD, למספר רב של אתרים בספטינים. השינוי הכימי הזה, שנקרא ADP‑ריבוקסנציה, הוא ואריאנט ייחודי ובלתי הפיך של שינוי חלבון נפוץ יותר.
שבירת המסגרת החלבונית מבפנים
כדי להבין כיצד תג כימי זה מחליש את ההגנה התאית, הצוות התמקד ב‑SEPT9. ספטינים בדרך כלל יוצרים שרשראות מסודרות של שמונה יחידות, המשתרכות לאחר מכן לסיבי ביניים ולבסוף לכלובים שלמים סביב החיידקים. החוקרים גילו שמעבר ספציפי ב‑SEPT9, חומצת אמינו הקרויה ארגינין 561, הוא אתר המפתח ל‑ADP‑ריבוקסנציה במהלך זיהום. עבודות מבניות וניסויי הרכבה מחומרים טהורים הראו שאתר זה נמצא במשטח מגע קריטי שבו שתי יחידות SEPT9 ננעצות זו בזו. כאשר אותה ארגינין עוברת שינוי כימי — או מוחלפת ברזידו שמחקה את המטען השלילי שנוסף — השרשראות האוקטמריות מתפרקות לחלקים קטנים יותר ואינן מסוגלות לבנות סיבים יציבים.
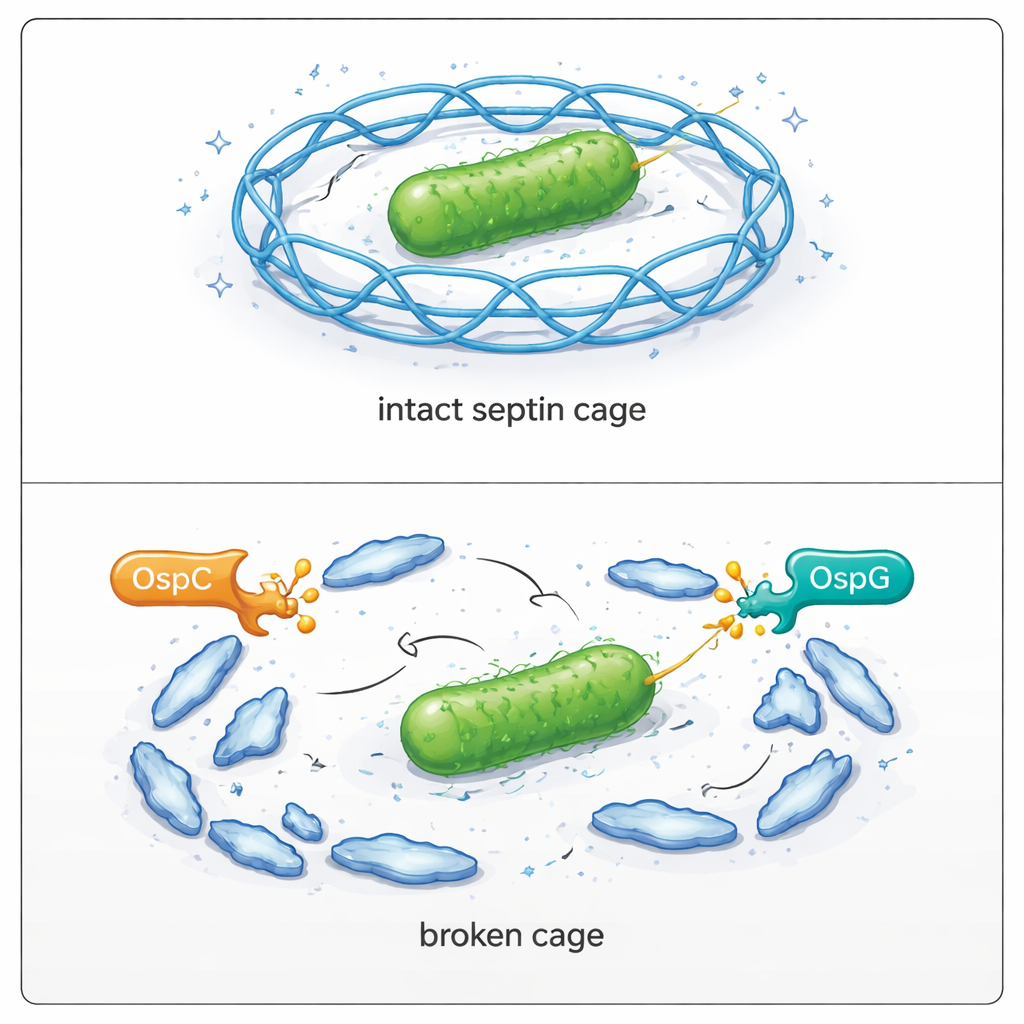
צפייה בכישלון הכלובים בתוך תאים נגועים
הצוות חזר להתבונן בתאים חיים כדי לראות את ההשלכות. בתאים אנושיים נגועים בשיגלה רגילה, רק מיעוט מהחיידקים הסתיים בתוך כלובי ספטין. כאשר מחקו גנטית את כל חלבוני OspC, חלק החיידקים הכלואים כמעט והכפיל את עצמו. הסרה של OspG נתנה אפקט דומה, ומחיקה משותפת של OspC ו‑OspG הובילה לעלייה נוספת ביצירת כלובים ופגעה קשות ביכולת החיידק להתפשט בשכבת תאים. הכנסת חזרה של חלבוני OspC פעילים לזני המוטант החזירה את בריחת החיידקים מהכלובים ואת יכולתם להתרבות וליצור פיצולים גדולים. מיקרוסקופיה אישרה שכאשר SEPT9 לא ניתן לשינוי בארגינין 561, הוא מצטרף לכלובים ביעילות; כאשר הוא משתנה על‑ידי OspC, יצירת הכלובים סביב החיידקים יורדת באופן חד.
מובן ההשלכות להילחם בשיגלה
במונחים מובנים ונגישים, עבודה זו מראה שלשיגלה נושאת זוג כלים מולקולריים משלימים שנועדו לשבור את הסורגים של "כלא" תוך‑תאי. OspC מחליש ישירות את אבני הבניין החלבוניות הדרושות להרכבת כלובי ספטין, בעוד OspG מקדם את פירוקם דרך מסלול כימי שונה. יחד, אסטרטגיות אלה מאפשרות לחיידק להיחלץ, לנוע בתוך תאים ולחדור לשכנים. הבנת מנגנוני הבריחה המדויקים הללו מעמיקה את תמונתנו על אופן פעולת החיסון התאי, ומציינת גם זוויות טיפוליות חדשות: תרופות החוסמות את OspC או המגינות על מגעים קריטיים בספטינים עשויות לסייע לשחזר את יכולתו הטבעית של התא ללכוד ולנקות פתוגן מסוכן זה.
ציטוט: Tang, Z., Xian, W., Özbaykal Güler, G. et al. Shigella flexneri evades septin-mediated cell-autonomous immunity via protein ADP-riboxanation. Nat Commun 17, 1727 (2026). https://doi.org/10.1038/s41467-026-68425-0
מילות מפתח: שיגלה, כלובי ספטין, חיסון תא‑אוטונומי, גורמי virulence חיידקיים, ADP‑ריבוזילציה