Clear Sky Science · he
ליגאזות היוביקויטין המשמרות מפנות דיאמינאזות APOBEC3 הקשורות בסרטן לעמידור כדי לקדם שלמות הגנום האנושי
להגן על ה-DNA שלנו מפגיעה ידידותית
התאים שלנו משתמשים באנזימים עוצמתיים כדי לפגוע ב-DNA ויראלי, וכך מסייעים להדוף זיהומים. אך חלק מאותם אנזימים, אם אינם מבוקרים, עלולים בטעות להשאיר צלקות בגנום שלנו ולתרום להתפתחות סרטן. מחקר זה חושף כיצד תאים אנושיים מפקחים על אנזימים מסוכנים אלה, וחשף מערכת "בקרת איכות" פנימית שמסמנת גרסאות מזיקות להריסה לפני שהן יכולות לשנות את ה-DNA שלנו.
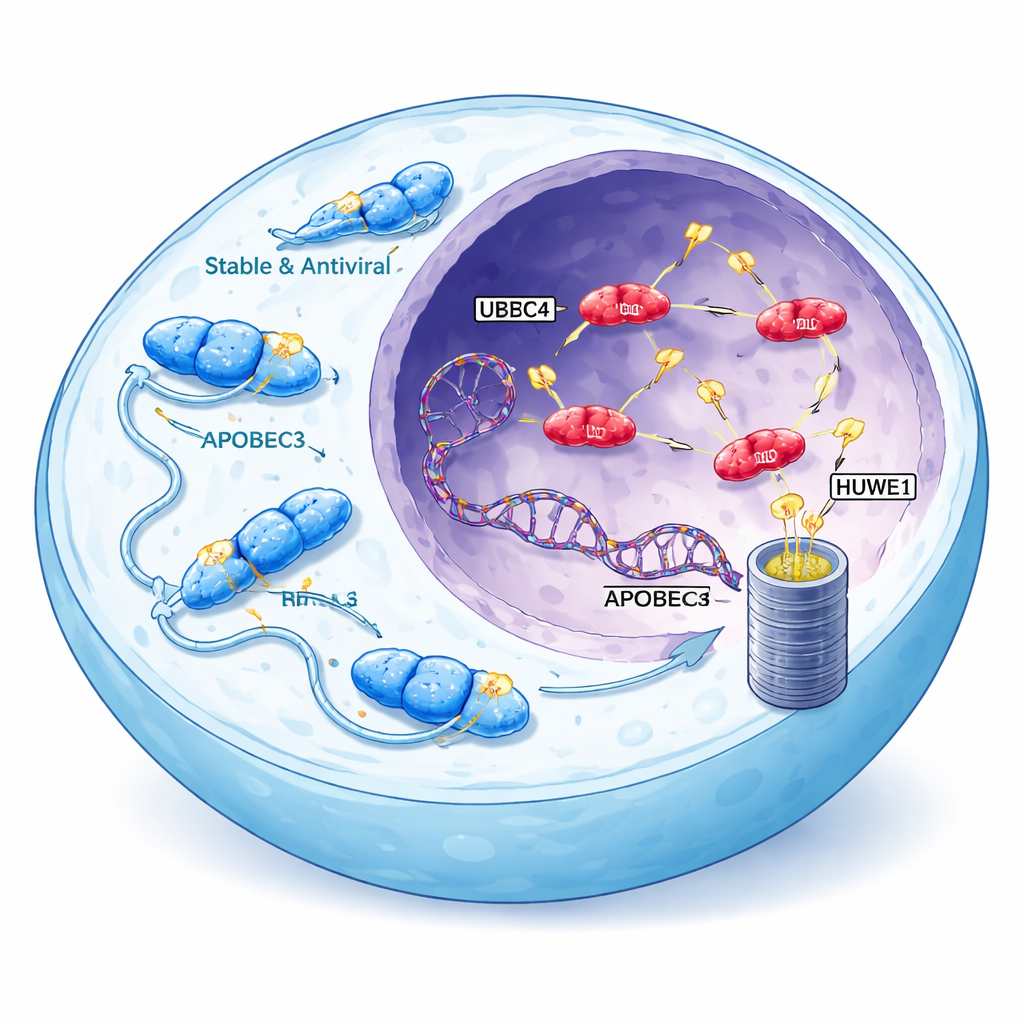
לוחמי וירוסים שיכולים להפנות נשק כלפינו
משפחת האנזימים APOBEC3 בדרך כלל מסייעת בהגנה מפני וירוסים כמו HIV על ידי שינוי כימי של ה-DNA הויראלי, מה שגורם לשגיאות קטלניות. בבני אדם יש שבע וריאנטים של APOBEC3, ושלושה מהם — A3A, A3B וצורת A3H שנקראת האפלוטיפ I (A3H-I) — מקושרים בחוזקה לדפוסי מוטציות הנצפים בהרבה סוגי סרטן. אנזימים אלה יכולים להיכנס לגרעין התא, שבו מצויים הכרומוזומים שלנו, ולהציג אשכולות אופייניים של מוטציות בגנום. חתימות מקושרות ל-APOBEC מופיעות ביותר ממחצית ממקרי הסרטן האנושיים, ובמיוחד בסרטנים של שד, ריאות ושלפוחית השתן, שם הן מרחיבות את מאגר השינויים הגנטיים שעליהם הגידול יכול להתבסס כדי להסתגל ולהתנגד לטיפולים.
מדוע הצורות המסוכנות ביותר אינן יציבות
באופן מפתיע, האנזימים של APOBEC3 המקושרים ביותר לסרטן הם גם הפחות יציבים. בשונה מבני משפחתם הציטופלזמטיים, שמצטברים ברמות גבוהות ומעכבים וירוסים ביעילות, A3A, A3B ו-A3H-I מתפרקים במהירות ונמצאים בדרך כלל בריכוזים נמוכים בגרעין. החוקרים שיערו שהחוסר ביציבות עשוי להיות מכוון: אם התאים מגבילים באופן פעיל את רמות חלבוני APOBEC3 בגרעין, כל כשל בבקרה זו עלול לשחרר גלי מוטגנזה. באמצעות A3H-I כמודל הם הראו כי APOBEC3s המקושרים לסרטן נהרסים בעיקר בפרוטאוזום, המגרסה של חלבוני התא, לאחר שנסתמו בדגלונים מולקולריים קטנים הנקראים יוביקויטין באתרי חומצות אמינו מרובים.
מציאת השומרים התאית
כדי לזהות את המכונה שאחראית לסימון A3H-I ו-A3B, הצוות שילב סקר CRISPR עם מיפוי קרבה חלבונית. הם מהנדסים תאים שמאירים בצורה שונה לפי יציבות A3H-I והגרסה החסרת הנזק A3H-II, ואז הפריעו שיטתית לגנים המעורבים בפירוק חלבונים. שלוש ליגאזות יוביקויטין — UBR4, UBR5 ו-HUWE1 — בלטו. השבתה של כל אחת מהליגאזות הללו העלתה ברמה סלקטיבית את רמות A3H-I הבלתי יציב שנמצא בגרעין מבלי להשפיע על A3H-II היציב בציטופלזמה. הליגאזות האלו הגבירו באופן עצמאי גם את רמות A3B אנדוגני בקווי תאים קולוניים ומערכתיים, ומחיקה משולבת של שלושתן הובילה לעלייה מצטברת בכמות A3B. ניסויים ביוכימיים הראו בנוסף ש-UBR5 ו-HUWE1 נקשרים פיזית ל-A3B ול-A3H-I ומצרפים ישירות שרשראות יוביקויטין, בעוד ש-UBR4 נראה מתמחה בהארכת שרשראות אלו כדי להפוך את החלבונים לניתנים לפירוק ביעילות רבה יותר.
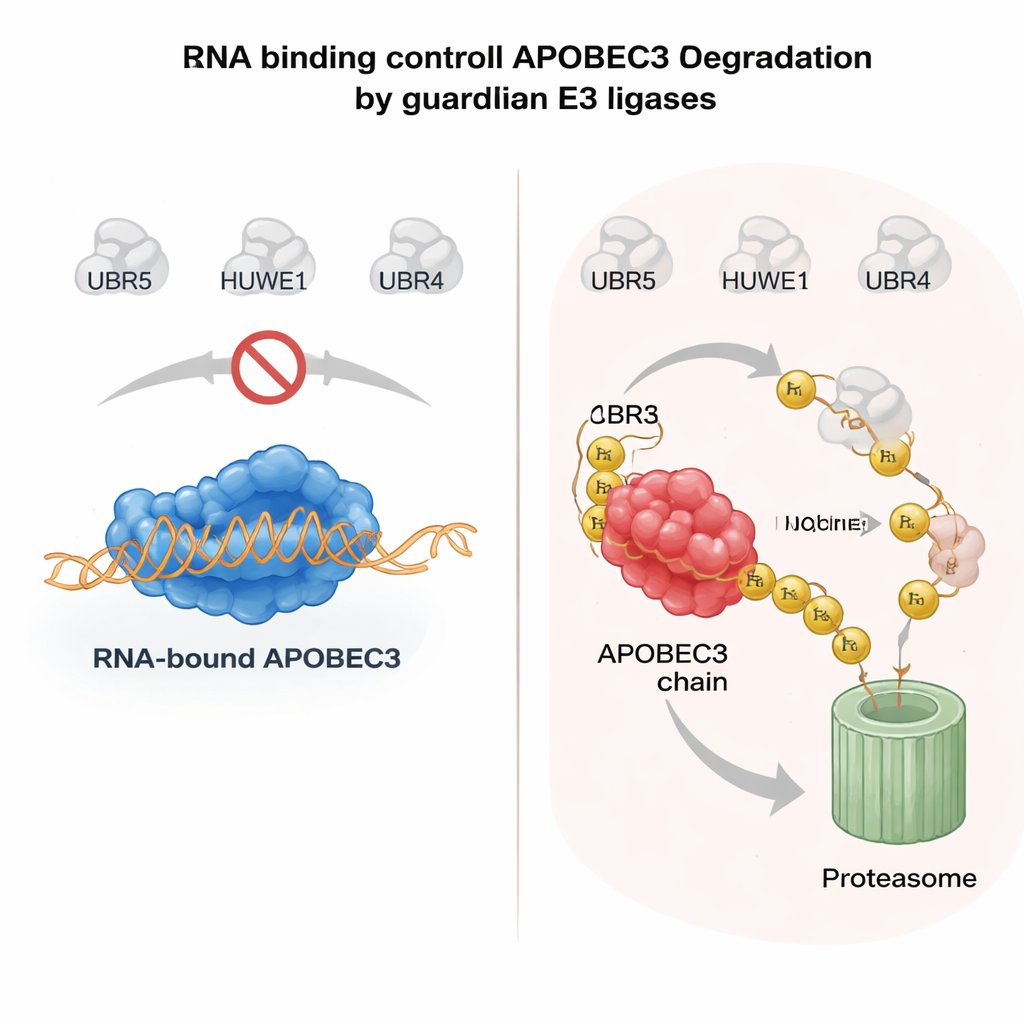
RNA כחגורת בטיחות לאנזימים מסוכנים
מה קובע אם אנזים APOBEC3 ייחשף לחסד או להרס? רמז מרכזי הגיע מאופן שבו חלבוני APOBEC3 נקשרים למולקולות RNA בציטופלזמה. כאשר A3H או חבר משפחה אחר, A3G, נקשרים ל-RNA, הם נוטים להישאר במורכבים גדולים בציטוזול ולהיות יחסית יציבים. מוטציות שמחלישות את הקשירה ל-RNA גורמות לאנזימים אלה לנוע לגרעין, לאבד את שותפיהם המגוננים ולהפוך לבלתי יציבים מאוד. המחברים הראו שכאשר חלבוני APOBEC3 אינם קשורים ל-RNA, UBR5 ו-HUWE1 מזהים משטחים חשופים על האנזים, מעטרים אותם ביוביקויטין ומכוונים אותם לפירוק גרעיני. במערכות מזוקקות, הוספת RNase להעלמת ה-RNA שיפרה משמעותית את היכולת של ליגאזות אלה להיקשר ל-APOBEC3 וליוביקויטינציה שלו, מאשר שהקשירה ל-RNA משמשת כמגן מולקולרי. מנגנון זה מאפשר לתאים לשמור על פעילות ה-APOBEC3 האנטיוויראלי בציטופלזמה תוך ניקוי מהיר של כל מאגר לא קשור ומסכן גנום בגרעין.
כשהשומרים נכשלים: קישורים למוטציות סרטניות
אם UBR4, UBR5 ו-HUWE1 פועלים כשומרים, אובדן שלהם אמור להעלות את רמות המוטציות. החוקרים בדקו זאת על ידי נטרול כל ליגאז בתאי סרטן המעי ומעקב אחרי שינויים ב-DNA לאורך זמן באמצעות שיטת ריצוף רגישה שקוראת "חתימות" מוטציוניות. הסרת הליגאזות הללו, במיוחד בתאים שמביעים A3H-I, הגבירה את דפוסי המוטציות הספציפיות ל-APOBEC — בדיוק אלה הנמצאות בגידולים אנושיים. בהרחבה לנתוני מטופלים, הם ניתחו אלפי גנומים סרטניים ומצאו שהגידולים שנושאים מוטציות ב-UBR5 או ב-HUWE1 הכילו חלק גבוה משמעותית של חתימות מוטציות מקושרות ל-APOBEC בהשוואה לגידולים עם ליגאזות שלמות, אפילו לאחר לקיחה בחשבון של עומס המוטציות הכללי. ממצא זה מרמז שליגאזות שמירת המערכת פגומות אצל חולים עלולות לאפשר ל-APOBEC3 המקושרות לסרטן להשתולל ולשנות את גנום הגידול.
מה משמעות הדבר לטיפול בסרטן בעתיד
ללא מומחיות, המסקנה היא שהתאים שלנו מצוידים במערכת פיקוח מתוחכמת שמונעת מאנזימי אנטי-ויראליים מועילים לפגוע בטעות ב-DNA שלנו. UBR4, UBR5 ו-HUWE1 פועלים כשומרים החשים מתי חלבוני APOBEC3 אינם עוד קשורים בבטחה ל-RNA ובמיוחד בגרעין שולחים אותם למגרסה התאית. כאשר מערכת הבקרה הזו נחלשת — עקב מוטציות בליגאזות או עקב תרופות החוסמות פירוק חלבונים — פעילות APOBEC3 עלולה לדלק את הכאוס הגנטי שמניע את התפתחות הסרטן ועמידותו לטיפול. הבנת רשת השומרים הזו פותחת דלתות לסמנים אבחנתיים חדשים, כגון מוטציות בליגאזות או רמות חלבוני APOBEC, ומרמזת כי כיוונון זהיר של המסלול עשוי בעתיד לסייע בצמצום פרצי המוטציות המזיקים בגידולים מבלי לפגוע בהגנה האנטיוויראלית שלנו.
ציטוט: Schwartz, I., Budroni, V., Meyenberg, M. et al. Guardian ubiquitin E3 ligases target cancer-associated APOBEC3 deaminases for degradation to promote human genome integrity. Nat Commun 17, 1723 (2026). https://doi.org/10.1038/s41467-026-68420-5
מילות מפתח: APOBEC3, יציבות הגנום, ליגאז יוביקויטין, מיטוגנזה בסרטן, דה-גרדציה של חלבון