Clear Sky Science · he
מיפוי מקיף של דינמיקות השינויים ב‑RNA ושל תקשורת ביניהם באמצעות למידה עמוקה וריצוף RNA ישיר בננופור
סימני הפיסוק הסמויים של ה‑RNA
המולקולות של ה‑RNA בתאים שלנו אינן מחרוזות פשוטות של A, C, G ו‑U. הן מקושטות בעשרות סימנים כימיים זעירים שמתנהגים כמו סימני פיסוק, ועוזרים לווסת אילו גנים דלוקים, כיצד מיוצרים חלבונים וכיצד תאים מגיבים ללחץ ולמחלות. ועד כה, מדענים בדרך‑כלל יכלו לחקור את הסימנים האלה אחד‑אחד, מה שמקשה להבין כיצד הם פועלים ביחד על פני הגנום כולו. עבודה זו מציגה את ORCA, מערכת למידה עמוקה שקוראת מולקולות RNA טבעיות ישירות ובונה מפה גלובלית רב‑שכבתית של הסימנים הכימיים האלה ושל האינטראקציות שלהם.
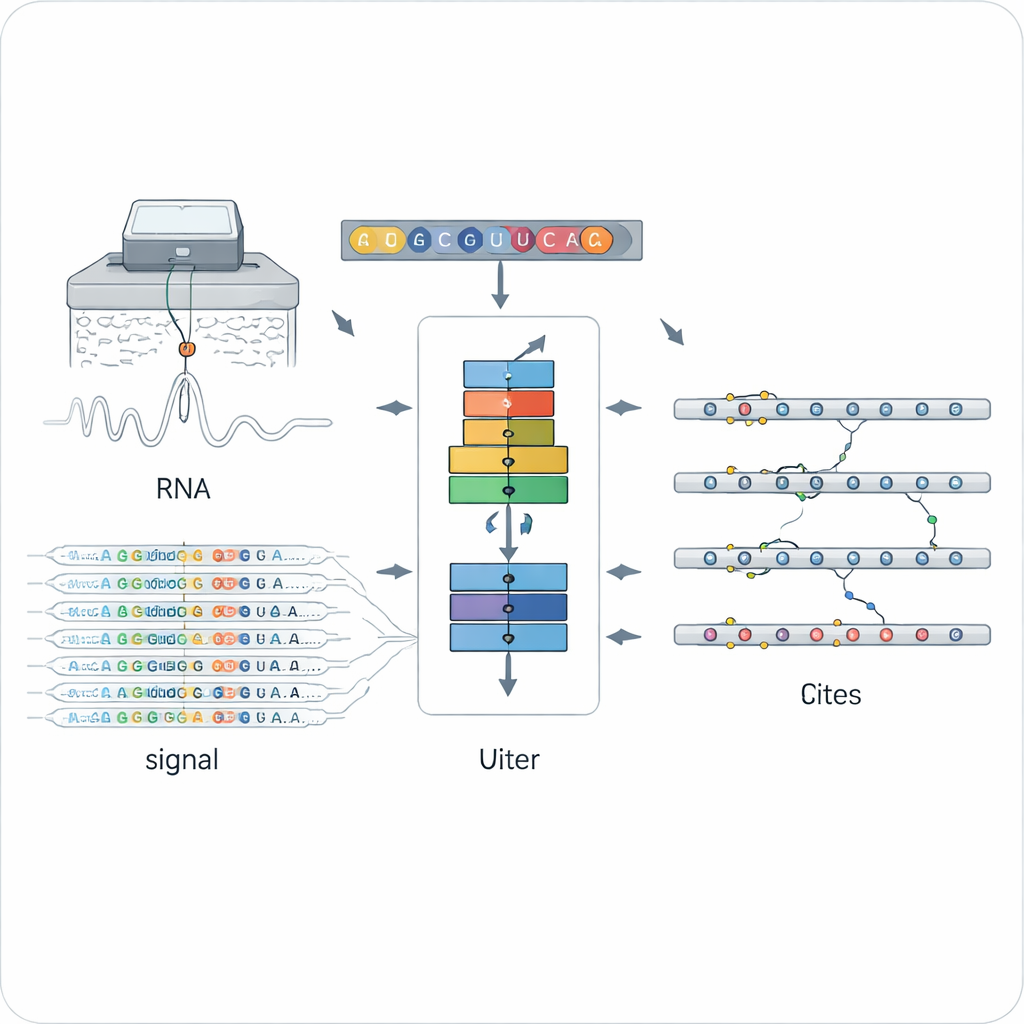
דרך חדשה לקרוא סימנים כימיים על ה‑RNA
שיטות מסורתיות למציאת שינויים ב‑RNA בעיקר מסתמכות על נוגדנים מיוחדים או על כימיה שמכוונת לסוג יחיד של סימן, כמו ה‑N6‑methyladenosine (m6A) המוכר. זה הופך אותן לעוצמתיות אך צרות: כל שיטה רואה רק סוג אחד של סימן, לעיתים בהגדרה ניסויית יחידה. ריצוף RNA ישיר בננופור פתח גישה אחרת על‑ידי העברת מולקולת RNA בודדת דרך נקב זעיר ומדידת שינויי הזרם החשמלי התלויים במבנה הכימי המדויק של כל בסיס. אותות מעוותים באופן שונה על‑ידי אותיות ממודדות ולא‑ממודדות, וגם התהליך של קריאת הבסיסים משנה את המידע, אבל לפענח את הנתונים הרועשים והרב‑ממדיים האלה עבור סוגי שינויים רבים היה אתגר גדול.
להדריך רשת עצבית לזהות כל סימן
ORCA (Omni‑RNA modification Characterization and Annotation) מתמודדת עם האתגר בשני שלבים. ראשית, היא מתמקדת בחלון קטן סביב כל מיקום ב‑RNA ומאגדת גם את האות הגולמי החשמלי וגם את דפוסי השגיאות בקריאת הרצף על פני קריאות רבות. משום שרק חלק מהעותקים נושאים סימן מסוים, אתרים אמיתית‑ממולאים מציגים התפלגויות אות מסולפות יותר ושכיחות גבוהה יותר של טעויות קריאה בנקודה ההיא. ORCA משתמשת ברשת חוזרת עמוקה שאומנה באסטרטגיה “אדברסריאלית” כדי ללמוד דפוסים כלליים שמבדילים בין אתרים ממודדים ולא‑מומדים, מבלי להיצמד לסוג כימי ידוע יחיד. כך ORCA יכולה להקצות לכל אתר ציון שינוי ואומדן של החלק היחסי של המולקולות שעברו שינוי.
ללמוד את זהות כל סימן
בשלב השני ORCA לומדת לתייג איזה סוג סימן כימי נוכח. המחברים מזינים למודל קבוצת אתרים ברמת וודאות גבוהה מתוך מאגרי ציבוריים, שבהם ניסויים קונבנציונליים כבר זיהו m6A, 5‑methylcytosine (m5C), פסאודו‑יורידין (Ψ), אינוזין, 2′‑O‑methylation ומספר סימנים נדירים יותר. ORCA מדחסת את דפוסי האות, ההקשר הרצפי וה”מוטיבים” רצפיים קצרים סביב כל אתר למפה בממד נמוך יותר, ואז מחדדת את עצמה כדי לחזות את סוג השינוי ואת הבסיס המדויק שעליו הוא יושב. חשוב: אתרים ללא תיוג משמשים גם כדוגמאות “רקע”, מה שעוזר למודל להימנע מכפיה של סימנים לא ידועים לקטגוריות שגויות. לאחר אימון, ORCA יכולה להעביר תיוגים אלו לעשרות אלפי אתרים שלא תועדו קודם ברחבי הטרנסקריפטום.
לראות שינויים רבים בו‑זמנית
ביישום ORCA על תאים אנושיים ועכבריים, המחברים מראים שהיא לא רק משווה או עולה על דיוק כלים מובילים לזיהוי סימנים ספציפיים כמו m6A, m5C ו‑Ψ, אלא גם יכולה לזהות סימנים שלא אומנה עליהם במפורש. לדוגמה, גם כאשר נתוני m6A הוסרו מאימון המודל, ORCA שחזרה את רוב אתרי ה‑m6A שנמדדו באופן עצמאי והבדילה אותם נכונה ממוטיבים רצפיים דומים שאינם ממודדים. כך קרה גם עבור קבוצות 2′‑O‑methyl, אתרי עריכת אינוזין ומגוון רחב של שינויים כימיים על RNA ריבוזומלי, כולל הרבה שינויים נדירים שנמדדו בעזרת ספקטרומטריה של מסה. בסך הכל ORCA מרחיבה משמעותית את קטלוג אתרי השינוי ב‑RNA הידוע, עם גידולים מרובים במספר אתרי m5C, Ψ, m7G וסימנים נדירים אחרים לעומת מאגרים קיימים.
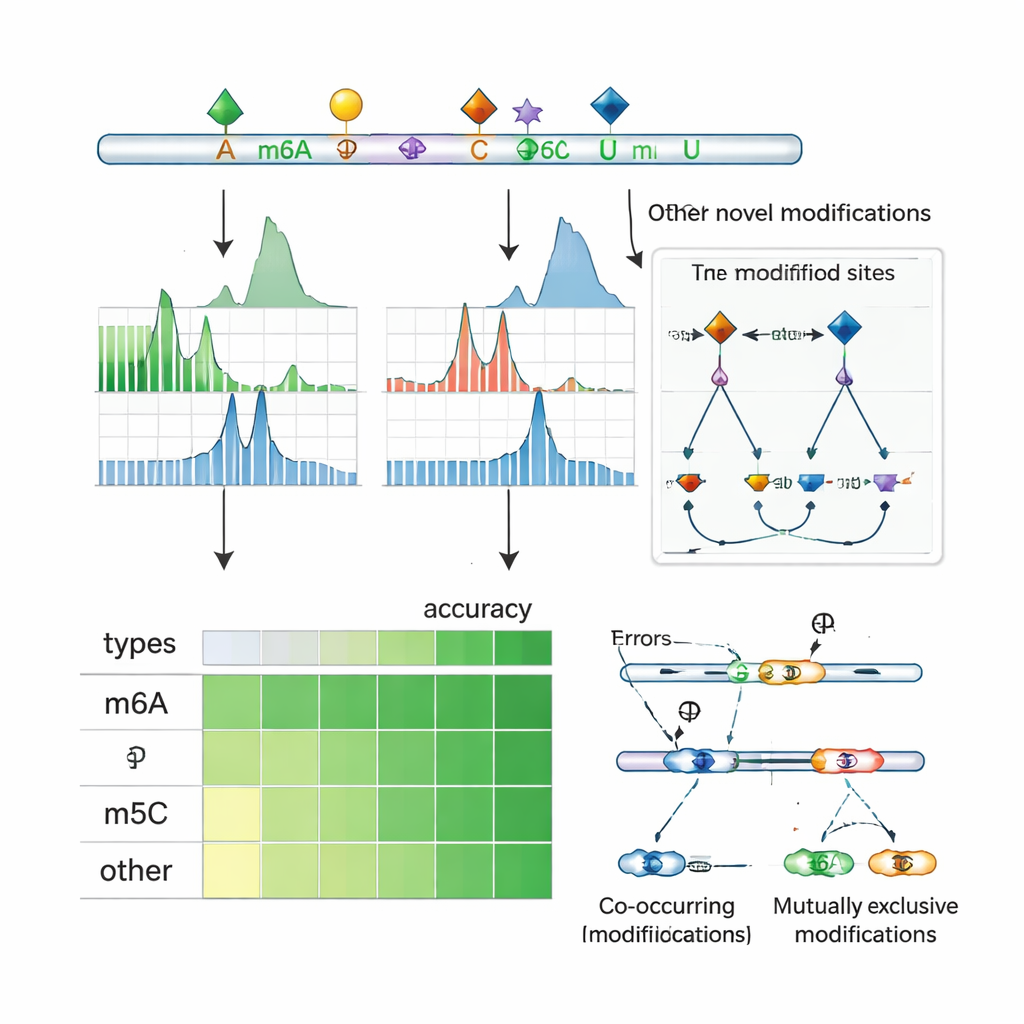
חשיפת תקשורת בין סימנים ושליטה על חיתוך
מכיוון שריצוף בננופור קורא מולקולות RNA בשלמותן, ORCA יכולה לבחון אילו סימנים מופיעים יחד על אותו תמצת ואילו נוטים להדיר זה את זה. המחברים מאשפזים סימנים סמוכים לאורך ה‑RNA ומשתמשים במודל הסתברותי כדי להסיק האם זוגות אתרים בדרך‑כלל מתמוללים יחד או בלעדיים זה לזה במולקולה יחידה. הם מגלים הופעות משותפות תכופות של m6A עם m5C וסימנים אחרים, וכן אזורים רבים שבהם אתר אחד ממודד רק כאשר האתר השכן אינו ממודד. בתאי אנוש, דפוסים אלה נוטים להימצא ליד אקסונים שנכללים או מדולגים באופן חליפי, ומצטלבים עם אתרי קשירה של רגולטורים של החיתוך וחלבוני “קורא” שמזהים RNA ממודד. בגנים מסוימים ORCA מגלה שווריאנטים מסוימים של חיתוך מועשרים בדפוס סימנים אחד בעוד שווריאנטים חלופיים נושאים דפוס שונה, וקושרת את הקישוט הכימי המקומי של ה‑RNA לאופן שבו ההודעות נחתכות ותופרשות.
מדוע זה חשוב לביולוגיה ולרפואה
על‑ידי שילוב ריצוף RNA ישיר עם למידה עמוקה גמישה, ORCA הופכת אות חשמלי מסובך למפה עשירה ורב‑שכבתית של סימנים כימיים על־פני הטרנסקריפטום. עבור קוראים לא‑מומחים, התוצאה המרכזית היא שמדענים יכולים כעת לראות לא רק היכן מתרחשים שינויים פרטניים ב‑RNA, אלא כמה סימנים שונים מקשטים את אותה מולקולה וכיצד הצירופים האלה מתקשרים לוויסות גנים, במיוחד לחיתוך ה‑RNA. המסגרת הזו מאפשרת לחקור את ה”אפיגנטיקה” של ה‑RNA בסוגי תאים ותנאים רבים בלי לתכנן ניסוי חדש לכל סימן, ובכך מפיחה תקווה לתגליות על האופן שבו השינויים הכימיים הזעירים הללו תורמים להתפתחות, לפעילות מוחית ולמחלות כמו סרטן והפרעות נוירולוגיות.
ציטוט: Dong, H., Gao, Y., Cai, Z. et al. Comprehensive mapping of RNA modification dynamics and crosstalk via deep learning and nanopore direct RNA-sequencing. Nat Commun 17, 1722 (2026). https://doi.org/10.1038/s41467-026-68419-y
מילות מפתח: שינויים ב‑RNA, ריצוף בננופור, למידה עמוקה, אפיטרנסקריפטום, חיתוך חליפי