Clear Sky Science · he
תצורות קצוות ה‑DNA קובעות היווצרות קומפלקס סינפטי במהלך גישור קצוות בתיווך NHEJ
כש‑DNA נשבר, התאים חייבים להגיב במהירות
יום‑יום ה‑DNA בתאים שלנו נפגע, נחתך ונשחק על‑ידי המטבוליזם הרגיל ולחצים סביבתיים. בין הפגיעות המסוכנות ביותר נמצאות שבירות דו‑גדיליות, שבהן שני הגדילים של ההליקס נשברים. אם שבירות אלה לא יתוקנו במהירות ובדיוק, התאים עלולים למות או, גרוע מכך, להידרדר לכיוון סרטן. המחקר הזה חוקר כיצד הצורה והכימיה המדויקות של קצוות ה‑DNA השבורות עוזרות לקבוע האם מסלול תיקון מרכזי, הנקרא חיבור לא‑הומולוגי של קצוות (NHEJ), מקרב את הקצוות ביעילות ובמינימום שגיאות.
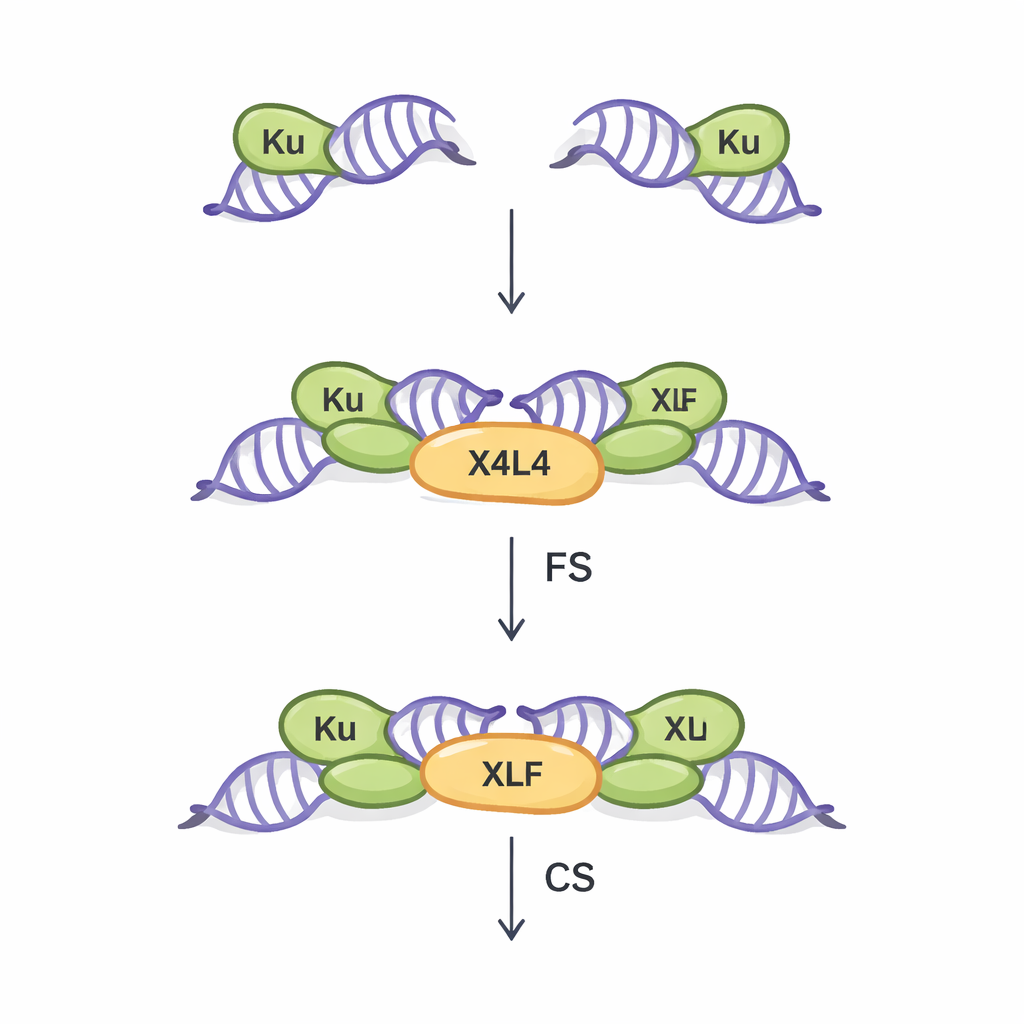
שתי דרכים לקרב בין קצוות DNA שבורים
NHEJ הוא המסלול הראשי לתיקון שבירות דו‑גדיל ברוב תאי הגוף. הוא פועל ללא צורך בתבנית תואמת, מה שהופך אותו למהיר אך במידה מסוימת פגיע לטעויות. הצעד הקריטי הראשון במסלול הזה נקרא סינאפסיס: גישור פיזי של שני קצוות ה‑DNA השבורות כדי שיוכלו להיצמד לאחר מכן. עבודות קודמות, שהתבססו בעיקר על קצוות חדים (blunt) אידיאליים, חשפו שני סוגי ריכוזים סינפטיים. במצב ה"סינאפסיס הגמיש" (FS), הקצוות מוחזקים קרובים אחד לשני ויכולים לנוע, בוחנים דרכים להתאים. במצב ה"סינאפסיס הצמוד" (CS), הקצוות מסודרים קצה‑לקצה ומוכנים לאיטום על‑ידי אנזים ליגאז. שלוש חלבונים ליבה — Ku, XRCC4–Ligase IV (ביחד נקראים X4L4), ו‑XLF — ידועים כמסנכרנים את התהליך הזה, אבל כיצד קצוות DNA לא רגילים מהעולם האמיתי משפיעים על איזה מצב סינאפסיס ייווצר נותר לא מובן היטב.
צורת הקצה והתאמות קצרות מנווטות את מסלול התיקון
החוקרים השתמשו ב‑FRET חד‑מולקולרי, טכניקת פלואורסצנציה העוקבת אחר מרחקים בקנה מידה ננומטרי, כדי לצפות במולקולות DNA בודדות כשהן מובאות יחד על‑ידי חלבוני NHEJ. הם השוו קצוות חדים פשוטים לקצוות מציאותיים יותר שנשאו זחלים קצוות (overhangs) קצרים — זנבות חד‑גדיליים שניתן להתאים ביניהם. הם מצאו שכאשר הזחלים משלימים זה את זה, אפילו במספר בסיסים מועט, זה מגדיל באופן דרמטי את הסיכוי ליצור קומפלקס סינאפטי צמוד. למעשה, שלושה בסיסים תואמים של "מיקרוהומולוגיה" במחבר הסדק הספיקו כדי ש‑Ku ו‑X4L4 לבדם ייצרו קומפלקס CS יציב, ללא צורך ב‑XLF. זה מראה שה‑DNA עצמו יכול לספק חלק מהאנרגיה וההכוונה שבדר״כ ניתנים על‑ידי חלבוני סיוע.
כיצד להבי DNA זעירים מייצבים את הגשר
באמצעות ניתוח חתימות FRET מובחנות, הצוות גילה לפחות שני טעמים מבניים של מצב הסינאפסיס הצמוד עבור קצוות עם זחלים. באחד מהם, הקצוות של הזחלים מתחברים זה לזה, מה שיוצר חיבור מחורר או עם חוסר בזילוח (nick או gap). באחר, החיבורים שבהם ה‑dsDNA פוגש את הזחל החד‑גדילי נלחצים בקו ישר, בעוד שהזחלים הופכים החוצה כמו להבים קטנים. להבים אלה עדיין מאפשרים התאמת בסיסים ושומרים את הקצוות במרחק מאוד קרוב, מה שסביר שמייצב את הקומפלקס ומעניק אנזימים מרחב לגזוז או להאריך את ה‑DNA לפי הצורך לפני האיטום הסופי. מעניין ש־נזק חמצוני נפוץ בזחלים, כגון 8‑oxoguanine, השפיע רק במידה מתונה על התהליך הזה, מה שמדגיש עד כמה NHEJ עמידה לצורות מסוימות של נזק.
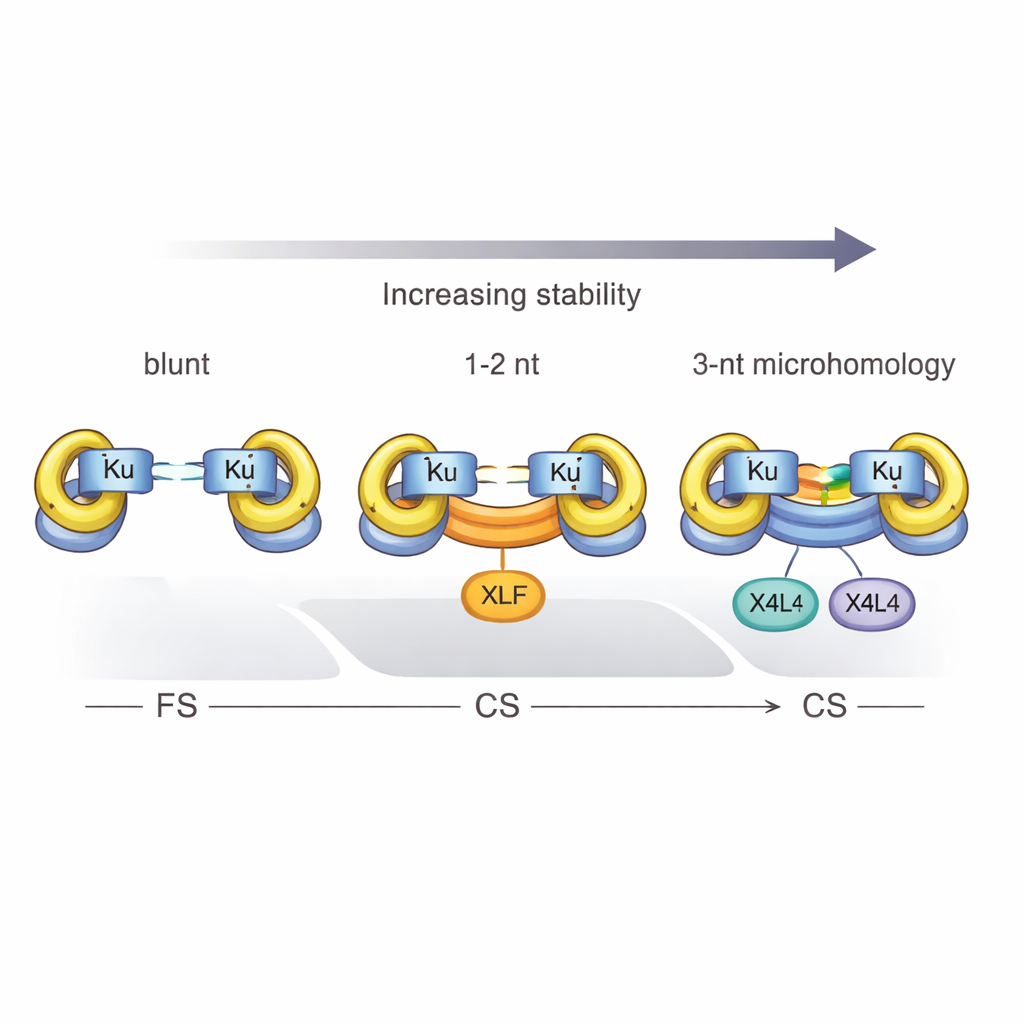
חלבונים, זרחנים וכוחם של שלושה
המחקר גם הגדיר סף חזק: נדרשים לפחות שלושה זוגות בסיסים משלימים כדי ש‑Ku ו‑X4L4 יהפכו באופן אמין קומפלקס גמיש לצמוד. עם התאמה של בסיס או שניים בלבד, המערכת נתקעת ברוב המקרים במצב הגמיש אלא אם XLF מצטרף כדי לעזור לאחוז את הקצוות יחד. גם פרטים כימיים חשובים. כאשר הקצוות הנשברים נושאים קבוצת זרחן ב‑5′ — מאפיין נפוץ בשבירות פיזיולוגיות רבות — הסינאפסיס נהיה יעיל יותר, והקומפלקסים הצמודים נוטים יותר להיות ממולגים באמת, מה שהופך גשר זמני לתיקון קבוע. עם זאת, המשוב החמצוני הזה לא יכול להחליף באופן מלא את אפקט הייצוב של התאמת בסיסים במחבר השבירה.
מדוע זה חשוב לבריאות ולעריכת גנום
במשפט יומיומי, עבודה זו מראה שקצוות ה‑DNA השבורים אינם קורבנות פסיביים שמחכים שיתוקנו. הצורות המדויקות שלהם, טלאי התאימות הקטנים והתגים הכימיים שלהם מכוונים באופן פעיל כיצד חלבוני התיקון תופסים, מסדרים ומחברים אותם מחדש. כאשר ישנם שלושה בסיסים תואמים או יותר, הקצוות עצמם מסייעים לנעול את השבירה לתצורה מוכנה לתיקון, ולעתים הופכים חלבוני סיוע מסוימים לא-חיוניים. כאשר התאמות כאלה נדירות, גורמי חלבון נוספים הופכים לקריטיים. תובנות אלה מסייעות להסביר מדוע חלק מהשברים מתוקנים בצורה נקייה בעוד אחרים מובילים למוטציות קטנות או ארגונים מחדש. הן גם מספקות רמזים לשיפור כלים לעריכת גנום כמו CRISPR, שבהם שבירות DNA מכוונות מתוקנות על‑ידי אותה מכניקת NHEJ. על‑ידי כוונון קצוות השברים האלה, מדענים עשויים לשלוט טוב יותר באיך הגנום מעוצב מחדש.
ציטוט: Zhang, C., Jin, W., Jiang, Y. et al. DNA end configurations dictate synaptic complex formation during NHEJ-mediated end bridging. Nat Commun 17, 1720 (2026). https://doi.org/10.1038/s41467-026-68417-0
מילות מפתח: תיקון שבירות דו‑גדיל DNA, חיבור לא הומולוגי של קצוות, סינאפסיס של DNA, מיקרוהומולוגיה, יציבות הגנום