Clear Sky Science · he
החלפה של ולין בלויסין יחידה משבשת את קשירת ה‑DNA של AP2‑G ב‑Plasmodium falciparum ומחשפת את תפקידו של GDV1 בהפעלה של ap2‑g
איך טפילי המלריה מקבלים החלטת חיים או מוות מכרעת
הטפילים של המלריה שבזרם הדם שלנו ניצבים כל הזמן בפני החלטה שמשנה את חייהם: להמשיך להתרבות בתוך אדם אחד, או לעבור לצורה שיכולה לזנק למארח הבא דרך עקיצת יתוש. המחקר הזה חושף כיצד שינוי קטן אחד בחלבון יחיד של הטפיל יכול לכבות לחלוטין את השלב הזיהומי המוכן ליתושים, ומציע זוויות חדשות לחסימת העברת המלריה.
מפנה הדרך של הטפיל
בזרם הדם, הפלסמודיום פאלציפורם בדרך כלל שם דגש על צמיחה מהירה, שגורמת למחלה. אך מיעוט קטן מהם משתנים לצורות מיניות הנקראות גמטוציטים, השלב היחיד שיתושים יכולים לקלוט ולהעביר. כיצד רק חלק מהטפילים בקבוצה מבצעים את המעבר הזה היה תעלומה ממושכת. עבודה קודמת הראתה ששני חלבונים של הטפיל, GDV1 וחלבון הקשור לקשירת DNA בשם AP2‑G, עומדים בלב ההחלטה הזו. GDV1 מסייע להעיר את הגן ap2‑g שבדרך כלל שקט, ו‑AP2‑G בתורו מפעיל מערך גנים שמניע את ההתפתחות המינית. המחקר הנוכחי הכוון תחילה לחקור חלבון קינאז בשם STK2, אך במקום זאת גילה ממצא דרמטי יותר בתוך AP2‑G עצמו.
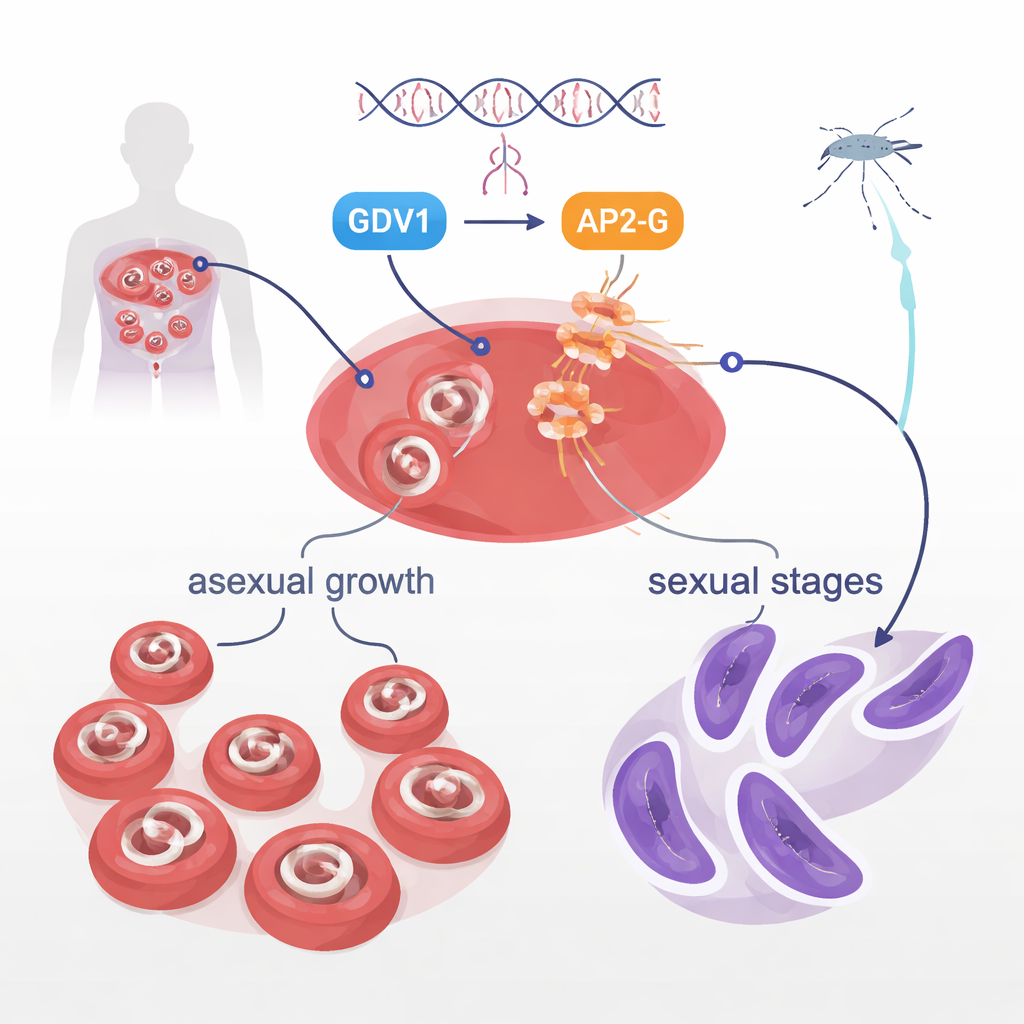
חומצת אמינו יחידה שמעכבת העברה
בעת מחיקת גן stk2 בזן מעבדה אחד, החוקרים הבחינו שהטפילים איבדו לגמרי את היכולת לייצר גמטוציטים, אך עדיין גדלו באופן אל-מיני כרגיל. בהפתעה, כששכפלו מניפולציות דומות בזן אחר, גמטוציטים נוצרו כרגיל. רצף הגנום המלא חשף את האשם הסמוי: שינוי אות יחיד בגן ap2‑g, המחליף חומצת אמינו אחת, ולין, בדומה ל‑לויסין, בעמדה 2163. מיקום זה נמצא בתחילת אזור קשירת ה‑DNA של AP2‑G, החלק שמחזיק פיזית מוטיבים ספציפיים ב‑DNA כדי להפעיל גנים. החלפת ולין בלויסין הזו לבדה הספיקה לבטל את יצירת הגמטוציטים. כשהחוקרים הנדסו מוטציה זו בטפילים שהיו אחרת נורמליים, הגמטוציטים נעלמו; כשהם החזירו זאת חזרה לולין, ההתפתחות המינית שוחזרה במלואה.
איך המתג שוברת את המנעול המולקולרי
כדי להבין מדוע שינוי עדין זה כל כך הרסני, הצוות שילב דוגמנות ממוחשבת עם ניסויים במעבדה. תחזיות מבנה הציעו שהחלפת ולין בלויסין משיטה ומערערת את הצורה המדויקת של תחום קשירת ה‑DNA של AP2. בניסויי מבחנה עם חלבונים זכים, AP2‑G הרגיל נקשר בחוזקה לרצף ה‑DNA המועדף עליו, קוד קצר המכיל את המוטיב "GnGTAC." לעומת זאת, ה‑AP2‑G המוטנטי עם לויסין בעמדה 2163 נכשל לחלוטין בקשירה לרצף זה. ללא קשירת DNA יציבה, AP2‑G לא יכל עוד להפעיל את גנו עצמו (לולאת משוב חיובית הידועה כאוטורגולציה) או להפעיל עשרות גנים מטה דרושים לדחיפה של הטפילים למסלול המיני. פונקציונלית, הטפילים המוטנטיים הפכו ל"עזבים": הם לא יכלו ליצור את הצורות שזיהום יתושים דורש, אף על פי שהם המשיכו לשגשג בתאי דם אדומים.
התפקיד הנסתר של GDV1 לפני ש‑AP2‑G תופס את ההגה
המוטציה גם סיפקה לכלים ייחודיים לחוקרים: טפילים שבהם הגן ap2‑g יכול להיות מופעל, אך AP2‑G אינו יכול לקשור DNA. באמצעות מדדי זוהר ופולט אור הם עקבו מתי שחקנים שונים פועלים במחזור 48 השעות של הטפיל בתאי הדם האדומים. הם גילו שחלבון GDV1 מופיע ראשון, מוקדם בשלב שנקרא שקיזוגוני, והוא חיוני להנעת הבעה של ap2‑g ממצב מושתק. ההפעלה המוקדמת הזו התרחשה בין אם ap2‑g קידד AP2‑G נורמלי או את הגרסה המוטנטית. רק מאוחר יותר, ברגע שריכוז של AP2‑G נורמלי הספיק, התרחשה לולאת המשוב העצמית החזקה והפעלת גנים "מיניים" נוספים. סימן חשוב, חלבון בשם MSRP1, נדלק רק בטפילים עם AP2‑G תפקודי, וסיפק דרך נוחה להבחין בין טפילים מחויבים מינית מוקדמים לאוחרים. בקווי מוטנטים עם החלפת הלויסין, GDV1 עדיין יכל להעיר את ap2‑g, אך חלבון AP2‑G השבור לא יכל לדחוף את התהליך קדימה, ולכן ההתפתחות המינית נעצרה.
השלכות על עצירת התפשטות המלריה
לקורא כללי, המסקנה פשוטה: טפילי המלריה נשענים על מנעול מולקולרי רגיש מאוד כדי להחליט אם יהיו מועברים. המחקר מראה ששינוי של שן אחת בלבד במנעול הזה — ולין יחיד באזור האחיזה של ה‑DNA של AP2‑G — מונע מהטפיל לייצר שוב את השלבים שמדביקים יתושים. בו בזמן, הוא מבהיר שחלבון אחר, GDV1, פועל מוקדם כמפתח לפתיחת הגן השקט ap2‑g, לפני ש‑AP2‑G מחזק את הייצור העצמי ומפעיל תוכנית מינית רחבה יותר. על ידי מיפוי רצף האירועים הזה ויצירת קווי טפילים מדווחים שמאירים כאשר כל שלב מתרחש, העבודה מספקת כלים חזקים לסרוק תרופות או גורמים אנושיים שמפריעים למחויבות המינית. בטווח הארוך, מטרה של אזור קשירת ה‑DNA של AP2‑G או של שלב ההפעלה המונע על ידי GDV1 עשויה להוות בסיס לאסטרטגיות חדשות שלא רק מרפאות אדם אחד, אלא ניתקות לחלוטין את שרשרת ההעברה.
ציטוט: Prajapati, S.K., Dong, J.X., Morahan, B.J. et al. A single valine to leucine switch disrupts Plasmodium falciparum AP2-G DNA binding and reveals GDV1’s role in ap2-g activation. Nat Commun 17, 1719 (2026). https://doi.org/10.1038/s41467-026-68416-1
מילות מפתח: העברת מלריה, Plasmodium falciparum, התפתחות גמטוציטים, AP2‑G, GDV1