Clear Sky Science · he
מערכת ננומטרית המיועדת לחלבון המעכב מתילופרוטאאזות-1 לטיפול רציף מרחבי‑זמני בפיברוזיס ריאתי אידיופתי
מדוע צלקות ריאה עקשניות חשובות
פיברוזיס ריאתי אידיופתי (IPF) היא מחלה ריאתית בלתי פוסקת שבה רקמת הריאה הרגילה, הספוגית, מוחלפת בהדרגה ברקמת צלקת נוקשה. אנשים עם IPF מפתחים קוצר נשימה בפעילויות יומיומיות, וברוב המקרים שורדים רק מספר שנים לאחר האבחון. התרופות הקיימות היום יכולות להאט את המחלה אצל חלק מהמטופלים, אך הן נדירות מוחקות צלקות קיימות ולעיתים גורמות לתופעות לוואי. מחקר זה בוחן "ננו‑טיפול" חכם שניתן לשאוף, שמטרתו לא רק לעכב את ה‑IPF, אלא גם לנקות בצורה פעילה רקמת צלקת ולעזור לריאות לתקן את עצמן.
הבעיה: צלקות דביקות ולחץ כימי
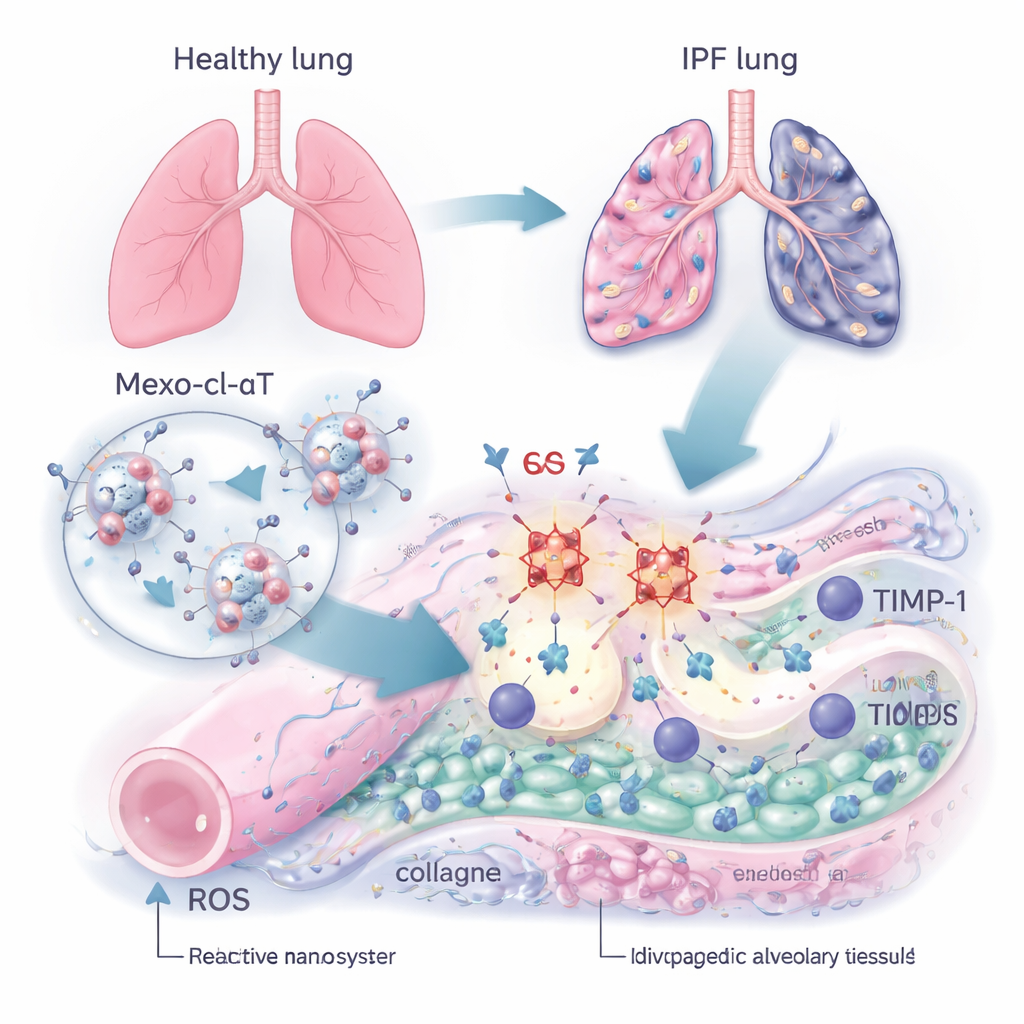
משלוח חכם: חבילות תיקון זעירות
כדי לשבור את המעגל הזה, הצוות פיתח טיפול ננומטרי בשם Mexo‑cl‑aT. הם התחילו מאקסוזומים — חלקיקים מבעבעים טבעיים שמופרשים מתאי גזע וידועים בנטייתם להגיע לרקמות פגועות ולתמוך בריפוי. על פני שטח האקסוזומים חיברו נוגדנים שמתחברים במיוחד ל‑TIMP‑1. הקישור בין האקסוזום לנוגדן נעשה באמצעות מחבר כימי מיוחד שניתן לחתוך על‑ידי ROS. במילים אחרות, הסביבה הכימית הקשה של ריאה צלקתית משמשת כאות: כשהאקסוזום מגיע לאזור פגוע העשיר ב‑ROS, המחבר נשבר, סופג חלק מ‑ROS ומשחרר את הנוגדן בדיוק במקום שבו TIMP‑1 מרוכז, בעוד שהאקסוזום עצמו ממשיך לתמוך בתיקון הרקמה.
כיצד המערכת הננומטרית מתנהגת ופועלת
בניסויים בתאים הראו החוקרים כי Mexo‑cl‑aT נשאר יציב בנוזל אך משחרר במהירות את הנוגדנים כשהוא נחשף לרמות מי חמצן הדומות לאלה בריאות חולות. במקביל, הוא מקטין באופן דרמטי את כמות המי חמצן הקיימת, מה שמאשר את תפקידו כמצמצם ROS. במודלים תאי‑צלקת שחרור הנוגדנים הוריד את רמות TIMP‑1 ושיחרר אנזימים שמפרקים קולגן, בעוד רכיב האקסוזום הפחית את מוות התאים, הגביר גדילה תאית והאיץ סגירת פצעים בתאי ריאה ותאי כלי‑דם. בהשוואה לגרסאות שבהן המחבר אינו ניתך, העיצוב הרגיש ל‑ROS הסיר יותר קולגן והפחית את המתח הכימי ביעילות רבה יותר, מה שמדגיש את חשיבות השחרור המבוקר.
בדיקות בדגם צלקת ריאה קשה
הצוות בדק אז את הטיפול בעכברים עם פיברוזיס ריאתי מתקדם שהושרה על‑ידי התרופה בליאומיצין, דגם שנבחר כדי לדמות שלב מאוחר של IPF. מנה אחת של Mexo‑cl‑aT הנשאפת נשארה בריאות למשך ימים והחזיקה יותר נוגדן מאשר תערובת פשוטה של רכיבים. הריאות המטופלות נראו בריאות יותר בעין בלתי מזוינת ובמיקרוסקופ: המרחבים האוויריים נפתחו מחדש, עובי הצלקת ירד ותכולת הקולגן הכוללת חזרה כמעט לנורמה. סמנים של תאים מייצרי צלקת הופחתו, בעוד חלבונים הקשורים לשכבות נאדיות וכלי‑דם בריאות עלו. מדידות כימיות הראו כי הטיפול קיצץ בצורה חדה את רמות TIMP‑1, השיב את האיזון של אנזימי פירוק הקולגן והסר בערך שלושת‑רבעי מעודפי ה‑ROS. חשוב לציין כי מדדי דלקת פחתו ובדיקות דם ובחינות איברים לא חשפו רעילות ברורה.
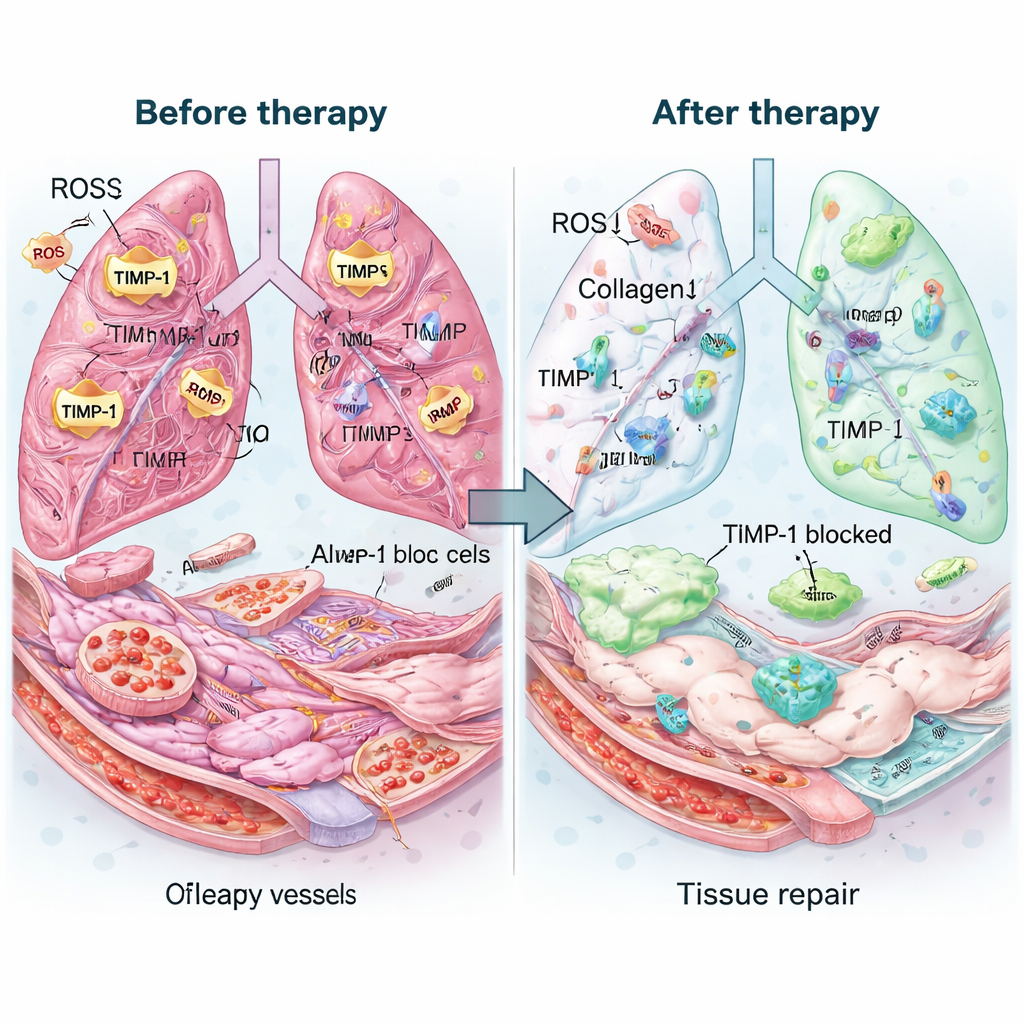
מה זה עשוי להחולל עבור מטופלים
לאנשים החיים עם IPF, עבודה זו עדיין אינה מציעה מרפא מיידי, אך מציגה אסטרטגיה מבטיחה. במקום רק להאט נזקים חדשים, מערכת Mexo‑cl‑aT שואפת לבטל באופן פעיל צלקות קיימות, להרגיע מתח כימי מזיק ולתמוך בבניית רקמת ריאה עדינה מחדש — כל זאת בצורה נשאפת ממוקדת שמרכזת את הטיפול במקום שבו הוא נדרש ביותר. בעוד אתגרים כמו ייצור אקסוזומים בקנה מידה גדול וניסויים בבני אדם נותרו פתוחים, המחקר מרמז שטיפולים ננו‑ממוקדים המותאמים לסביבה החולה עשויים יום אחד לשנות את אופן הטיפול בצלקות ריאתיות עקשניות ואולי גם במחלות פיברוטיות אחרות.
ציטוט: Li, C., Lu, G., Chen, H. et al. A nanosystem targeting tissue inhibitor of metalloproteinase-1 for continuous spatiotemporal idiopathic pulmonary fibrosis therapy. Nat Commun 17, 1694 (2026). https://doi.org/10.1038/s41467-026-68398-0
מילות מפתח: פיברוזיס ריאתי אידיופתי, צלקות ריאה, ננו‑רפואה, טיפול באקסוזומים, TIMP-1