Clear Sky Science · he
מודליזציה של מטבוליזם ספציפי לרקמות ב-Drosophila מזהה דיסרגולציה מטבולית בשריר ברמות תגובה ונתיב הנגרמת מתזונה עתירת סוכרים
מדוע מחקר על זבובי פרי רלוונטי לבריאות האדם
יותר מדי סוכר בתזונה שלנו יכול להכביד על היכולת של הגוף לנהל דלק, ובסופו של דבר לתרום להתפתחות סוכרת מסוג 2. מחקר זה משתמש בזבובי פרי כדי לחשוף, בפירוט מרשים, כיצד רקמות שונות מנהלות מטבוליזם וכיצד תזונה עתירת סוכר מפריעה לתפקוד השריר. מאחר שלזבובים ויש לנו שיתוף של גנים מטבוליים ומערכות איברים רבות, התובנות הללו מסייעות להסביר מה עלול להשתבש בשרירים שלנו תחת עומס סוכר כרוני.
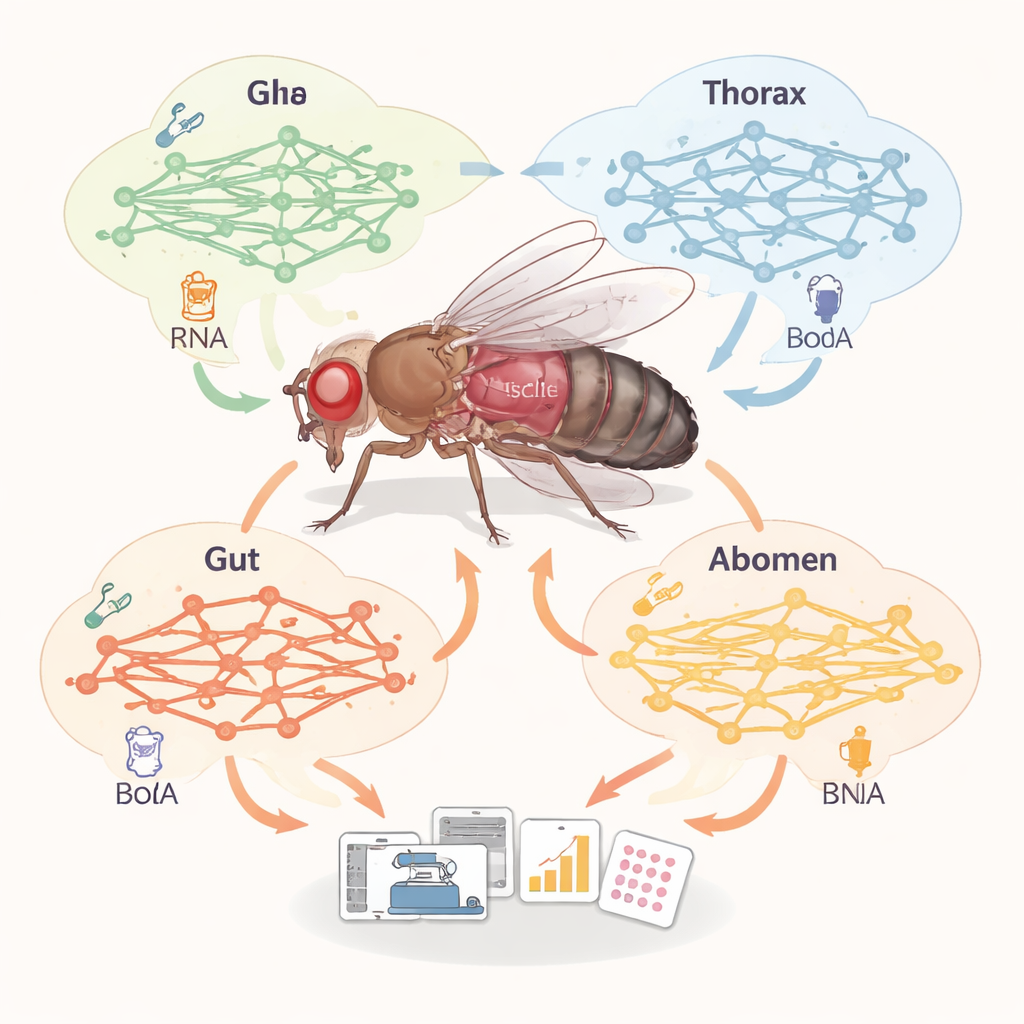
מיפוי מטבוליזם רקמה אחר רקמה
גופנו, כמו גופם של זבובי פרי, מורכב מרקמות הממלאות תפקידים מטבוליים שונים מאוד: השריר שורף דלק, רקמת השומן מאחסנת אותו, המעי מעבד מזון, וכן הלאה. במקום למדוד כל אנזים ישירות, החוקרים בנו “מפות” רחבות היקף של המטבוליזם — שנקראות מודלים מטבוליים בקנה מידה של גנום — עבור 32 רקמות זבוב שונות. הם שילבו רשת תגובות כימיות קיימת ומתוחזקת עם נתוני ביטוי גנים ברמת תא בודד, שמצביעים אילו גנים מטבוליים מופעלים בכל רקמה. זה איפשר להם להשוות כמה תגובות, מטבוליטים וגנים פעילים ברשתות הספציפיות לרקמה ולראות אילו מסלולים מודגשים בשריר, ברקמת השומן, במעי ובסוגי תאי עצב שונים.
תפקידי דלק מובחנים לאיברים שונים
השוואה זו חשפה “אישיוּת” מטבולית ברורה בין הרקמות. רקמת השומן והאונוציטים — מקבילות הזבוב לשומן ולכבד האנושיים — כללו את מערך התגובות העשיר ביותר, ובמיוחד תגובות שורפות שומנים באמצעות בטא-חמצון. השריר, בהשוואה, לא היה בעל הרשת הגדולה ביותר, אך כן הכיל את החלק הגבוה ביותר של תגובות המעבירות חומרים פנימה והחוצה מהתאים, מה שמרמז כי השריר הוא צומת מרכזית להחלפת דלקים ובוני-יסוד עם שאר הגוף. המדענים גם בדקו האם המסלולים שחזו תואמים לדפוסי מטבוליטים שנמדדו באזורים שונים של הגוף. באמצעות מטבולומיקה ממוקדת הם ניתחו מאות מולקולות קטנות מראשי הזבובים, בית החזה, המעי והבטן, ואז בדקו האם המסלולים המועשרים בנתונים חופפים לאלה שחזו המודלים. בשריר וברקמת השומן ההתאמה הייתה חזקה, מה שנותן ביטחון שהמודלים הספציפיים לרקמה קלטו ביולוגיה אמיתית טוב יותר מביטוי גנים בלבד.
מה תזונה עתירת סוכר עושה לזרימת הדלק בשריר
עם מודל שריר שנאמן לממצאים, הצוות סימל את מה שקורה כאשר זבובים מאכילים לאורך זמן תזונה עתירת סוכר, מודל מבוסס היטב לסוכרת מסוג 2. הם הגבל את המודל באמצעות תכונות ידועות של שריר סוכרתי, כגון ירידה בקליטת גלוקוז ופעילות מוחלטת פחותה במחזור האנרגיה המרכזי במיטוכונדריה. ניתוחי “זרימה” חישוביים — חישובים של מהירות הרצה אפשרית של תגובות — הראו ירידות רחבות בהיקף התגובות התלויות בזוג הרדוקס NAD/NADH, מולקולות שמעבירות אלקטרונים והן חיוניות לייצור אנרגיה. באופן ספציפי, תגובות במסלול המרכזי של שריפת סוכרים, הגליקוליזה, האטו, כולל תגובות שמוּנעות על ידי האנזים GAPDH. המודל גם חזה ירידה של כערך רבע בקיבולת השריר לייצר NADH בכלל, מצב שמרמז על מאזן רדוקס במתח. מדידות ישירות בשריר החזה של הזבוב אישרו כי היחס NAD/NADH אכן ירד תחת תזונה עתירת סוכר.
מעקב אחרי סוכר מסומן וחלבונים מחומצנים
כדי לבדוק האם צווארי הבקבוק החזויתיים התרחשו באמת בחיות חיות, החוקרים האכילו זבובים תזונה עתירת סוכר שכללה גלוקוז מסומן uniformly ב-C-13 ואז עקבו לאן הפחמן המסומן הלך. הם מצאו שמתווכים גליקוליטיים מוקדמים שמופיעים לפני GAPDH הצטברו, בעוד שמוצרי ההמשך ושברי התיוג שלהם ירדו, מה שמעיד על האטה אמיתית בשלב זה ובשלבים התחתונים. בדומה לכך, התרומות של פחמן הגלוקוז למחזור האנרגיה המרכזי פחתו. במקביל, פרוטאומיקת רדוקס — שיטה שמזהה שינויים חמצוניים בחומצות אמינו ספציפיות בחלבונים — הראתה עלייה בחימצון של רבים מהאנזימים הגליקוליטיים, כולל אתרים מרובים ב-GAPDH. לאורך הגליקוליזה, אנזימים שנשאו שינויים חמצוניים מרובים נטו להראות ירידות גדולות יותר בזרימה החזויה, אף על פי שרמות החלבון הכוללות שלהם נשארו ברובן ללא שינוי. הדבר מציע כי נזק כימי משחיקת חמצון, ולא אובדן בשפע האנזים, הוא גורם מרכזי להחלשת עיבוד הסוכר בשריר.
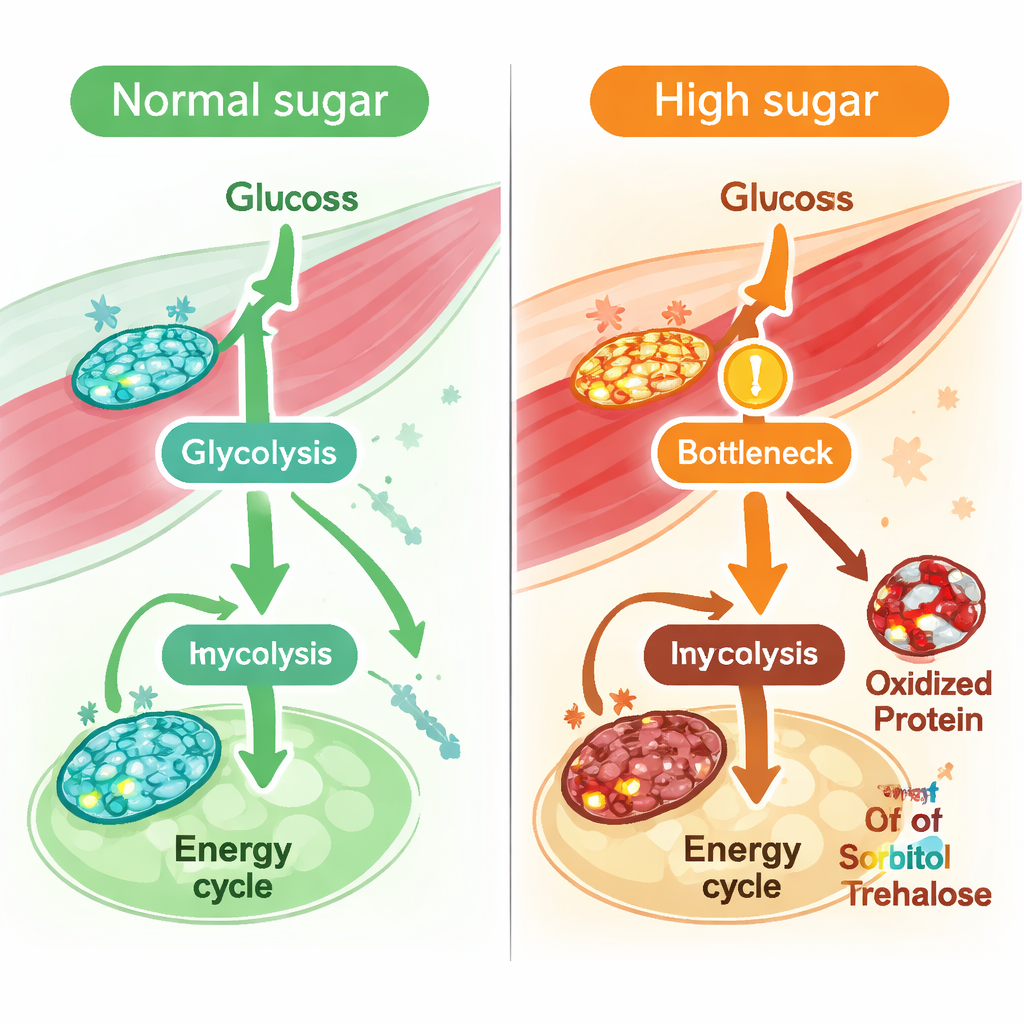
בעיה מוסתרת בעיבוד פרוקטוז וסוכרוז
מבט שמעבר לתגובות בודדות הראה כי כאשר ממוצעים זרימות ברחבי מסלולים שלמים כדי לזהות אילו מהם נפגעו ביותר על ידי סוכר גבוה, גליקוליזה, מחזור האנרגיה וצטלחות חמצונית (וF0F1-ATPase/שרשרת הנשימה) כולם הראו ירידות, אך אחת הירידות החזויות החזקות הייתה במטבוליזם של פרוקטוז. פרופיל מטבוליטים של השריר תמך ברעיון זה: רמות הסורביטול וטרהלוז/סוכרוז עלו, והאנזים המרכזי שממיר טרהלוז לגלוקוז, טרהלאז, הראה הן פעילות חזויה מופחתת והן חמצון מוגבר באתר מתיונין רגיש. יחד, הממצאים מצביעים על הפרעה רחבה יותר באופן שבו השריר מטפל בסוכרים תזונתיים — במיוחד בדלקים דמויי פרוקטוז ובהתderivedים מסוכרוז — תחת עומס סוכר כרוני.
מה זה אומר להבנת סוכרת
במילים פשוטות, עבודה זו מראה כי יותר מדי סוכר לא רק מעמיס על זרם הדם; הוא גם מעצב בשקט את האופן שבו תאי השריר מנתבים ושורפים דלק. על ידי בניית מפות מטבוליות מפורטות וספציפיות לרקמות בזבוב הפרי ובדיקתן מול מטבולומיקה, מעקב איזוטופים ופרוטאומיקת רדוקס, החוקרים מגלים כי סוכר גבוה מניע לחץ רדוקס, מחמצן אנזימים גליקוליטיים מרכזיים כגון GAPDH, מאט את פירוק הסוכר ומפר את מסלולי הפרוקטוז. התובנות האלה, שהושגו באורגניזם מודל שקל להשיג ולבחון, מספקות מסגרת חזקה להצביע אילו תגובות ומסלולים עשויים להיות החשובים ביותר להגן או לשקם בשריר האנושי כדי למנוע או לטפל בסוכרת מסוג 2.
ציטוט: Moon, S.J., Hu, Y., Dzieciatkowska, M. et al. Modeling tissue-specific Drosophila metabolism identifies high sugar diet-induced metabolic dysregulation in muscle at reaction and pathway levels. Nat Commun 17, 1692 (2026). https://doi.org/10.1038/s41467-026-68395-3
מילות מפתח: מטבוליזם של Drosophila, מודלים מטבוליים ספציפיים לרקמות, תזונה עתירת סוכר, גליקוליזה בשריר, ויסות רדוקס