Clear Sky Science · he
הסרה מדויקת של חזרות GGC מורחבות ב-NOTCH2NLC בעזרת CRISPR/Cas9 לטיפול במחלת הכללת גרעינית נוירונלית
עריכת DNA כדי להתמודד עם מחלה מוחית מסתורית
מחלת הכללת גרעינית נוירונלית (NIID) היא מחלה מוחית נדירה אך הרסנית שיכולה לגרום לדמנציה, לבעיות בתנועה ואף למוות מוקדם. כיום אין טיפול מרפא. במחקר זה נבחן האם כלי עוצמתי לעריכת גנים, CRISPR, יכול לשמש כדי לגזור מקטע קטן אך רעיל של DNA המניע את ה-NIID, ומציע הצצה לאופן שבו טיפולים עתידיים עשויים לכתוב מחדש את הגנום שלנו כדי להילחם במחלות מוחיות. 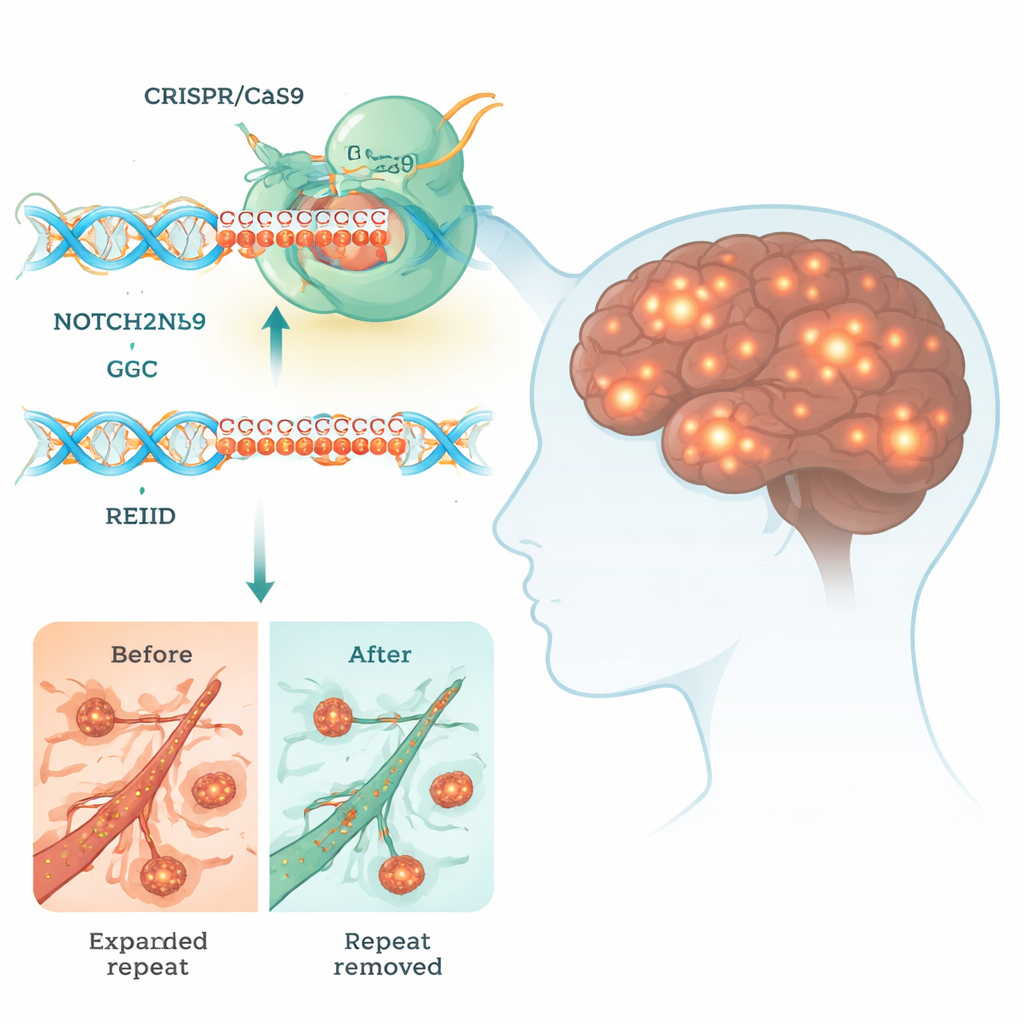
עבריין גנטי נסתר
רבות מהמחלות המוחיות התורשתיות נגרמות על ידי רצפים קצרים של DNA שהתארכו מעבר לאורךם התקין. ב-NIID הבעיה היא רצף מוגדל של יחידות תלת-תוית, "GGC", בגֵן הנקרא NOTCH2NLC. אף שהמקטע הזה יושב באזור שאינו מקודד לחלבון קלאסי, הוא עדיין יכול להיקרא על-ידי מכונות התא וליצור שרשראות פוליגליצין (polyG) בלתי תקינות. השרשראות הדביקות האלה מצטברות לגושים בתוך הגרעין של תאי עצב ורקמות אחרות, ומפריעות לתהליכים חיוניים כמו ייצור אנרגיה, עיבוד RNA ותנועת מולקולות בין הגרעין לציטופלסמה.
האתגר של ניתוח גנטי מדויק
עיצוב טיפול בעריכת גנים ל-NIID קשה במיוחד כי ל-NOTCH2NLC יש כמה גנים קרובים כמעט זהים החשובים להתפתחות המוח האנושי. אם CRISPR יחתוך את הגן הלא נכון, הוא עלול להזיק יותר מאשר להועיל. החוקרים סרקו בקפידה את ה-DNA סביב חזרת ה-GGC ומצאו הבדלים זעירים בסדרה המבדילים את NOTCH2NLC מבני-משפחתו. הם עיצבו זוגות של מוליכי RNA מנחים שמנחים את Cas9, ה"מספריים המולקולריים", לחתוך מיד לפני ואחרי החזרה המורחבת. אסטרטגיית החיתוך הכפול הזו מאפשרת למערכת התיקון של התא להסיר את המקטע הרעיל תוך השארת שאר משפחת הגנים ללא פגע.
מתאים בתאי צלחת לתאים נוירונליים שמקורם בחולה
הצוות בחן תחילה את עיצוב ה-CRISPR בתאים אנושיים סטנדרטיים ובתאים שעוצבו לשאת חזרת NOTCH2NLC גדולה. במודלים אלה העורך הסיר ביעילות את החזרה, ורמות הגושים של polyG ירדו בכ-50% ואף יותר. לאחר מכן הם עברו לתאי גזע פלוריפוטנטיים המושרים (iPSCs) שנוצרו ממטופל עם NIID והפכו תאים אלה לתאי אם נוירונליים, שלב מוקדם בהתפתחות תאי מוח. באמצעות CRISPR הם או שמחקו את החזרה המורחבת או שהחליפו אותה בגרסה באורך תקין. רצפי DNA מפורטים וריצוף גנומי מלא הראו שעריכה הייתה מדויקת מאוד, עם מעט עדויות לחיתוכים בלתי רצויים, והתאים הערוכים המשיכו להתחלק ולהתבגר באופן תקין. 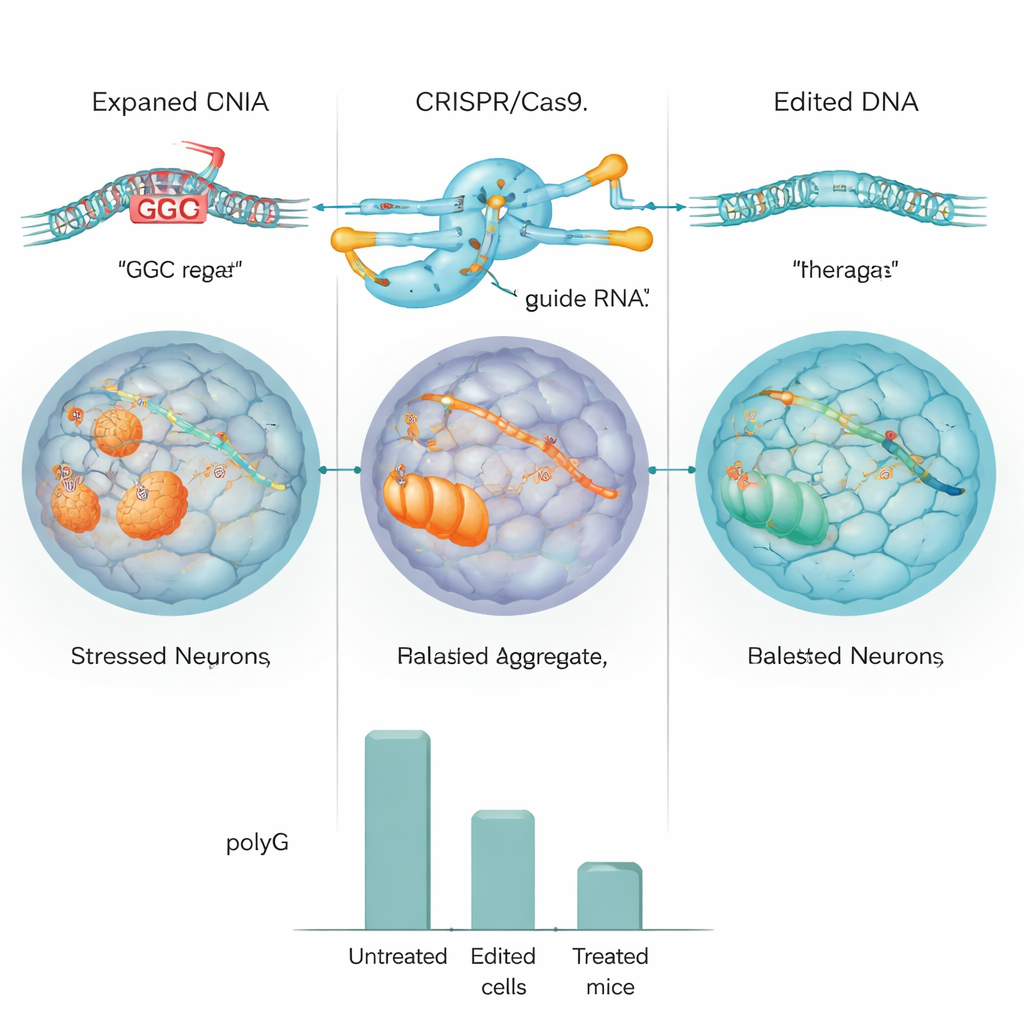
הצלה של המוח והגוף במודל עכבר
כדי לבדוק האם הגישה הזו יכולה לשפר בפועל את המחלה, החוקרים פנו לעכברים שעוצבו לשאת את חזרת NOTCH2NLC האנושית ולפתח תכונות דמויות-NIID, כולל כלולות גרעיניות, בעיות תנועה ותוחלת חיים מקוצרת. הם ארזו את מערכת ה-CRISPR לתוך וירוס מותאם שיכול להתפשט ברחבי המוח לאחר הזרקה פשוטה לזרם הדם של עכרים ניו-נולדים. בחיות שטופלו, החזרה המורחבת הוסרה בהצלחה ברקמת המוח. כתוצאה מכך רמות ה-polyG הרעילות ירדו באופן חזק, סמני בריאות תאי העצב השתפרו, והפחתה בפעילות יתר של תאי תמיכה במוח נצפתה. מבחני התנהגות הראו שעכברים מטופלים זזו יותר, שמרו על שיווי משקל טוב יותר ושרדו זמן רב יותר לעומת הגורים שלא טופלו. יתרונות דומים נראו גם בלב, שגם הוא מצטבר בו polyG במודל זה.
מה משמעות הדבר לטיפולים עתידיים
לקרב־נפש, המסר המרכזי הוא ש-NIID נראית כמונעת ברובה על ידי חזרת DNA מסוימת אחת שהתארכה, והסרה מדויקת של אותה חזרה יכולה להפוך סימנים רבים של המחלה בתאים ובעכברים. עבודה זו אינה עדיין מתורגמת לטיפול מוכן־לשימוש בבני אדם: יש עוד צורך לדייק את הבטיחות לטווח ארוך, לשפר שיטות הובלה ולבחון בבעלי חיים גדולים ודמויי־אדם יותר. אך המחקר מספק הוכחת־עיקרון חזקה שעיצוב עריכה גנטית ממוקדת בקפידה יכול לשתק באופן בטוח חזרה רעילה תוך שמירה על גנים קרובים. אסטרטגיה זו עשויה יום אחד להיות מותאמת לא רק ל-NIID, אלא גם להפרעות מוחיות ושריריות אחרות הנגרמות על ידי הרחבת חזרות דומה.
ציטוט: Xie, N., Pan, Y., Tong, H. et al. Precise excision of expanded GGC repeats in NOTCH2NLC via CRISPR/Cas9 for treating neuronal intranuclear inclusion disease. Nat Commun 17, 1683 (2026). https://doi.org/10.1038/s41467-026-68385-5
מילות מפתח: עריכת גנים ב-CRISPR, מחלת הכללת גרעינית נוירונלית, הפרעות הנובעות מהרחבת חזרות, NOTCH2NLC, נוירודגנרציה