Clear Sky Science · he
Tmem110 מווסת את הקונפורמציה של TRPML1 כדי לשמור על הומאוסטזיס אנדוליזוזומלי ולמנוע דליפת DNA מיטוכונדריאלי ועיבוד פתולוגי של DNA עצמי
מדוע דליפת DNA לאחר פגיעה חשובה
כשחווים טראומה קשה, כמו מכה חזקה בראש, הנזק אינו מוגבל לנקודת הפגיעה. רבים מהחולים מפתחים תגובה מערכתית מסוכנת שבה הריאות, הכבד, הכליות ואיברים נוספים מתחילים להיכשל. המחקר חושף כיצד מבנים זעירים בתוך התאים — ליזוזומים, מיטוכונדריה וחיישני חיסון — מתקשרים זה עם זה כדי להחליט האם הגוף ינקה את שאריות הפגיעה בשקט או יכנס להתקפת חיסון הפונה נגד עצמו. הבנת מערכת הניקוי החבויה הזאת עשויה לפתוח דרכים חדשות למניעת כשל איברים אחרי טראומה ולטיפול במחלות אוטואימוניות ודלקתיות.
מפי פגיעה בראש להתמוטטות כללית של הגוף
חבלת מוח טראומטית (TBI) עלולה להצית סערת דלקת עוצמתית הנקראת תסמונת תפקוד רב‑איברים (MODS), אך היחידה שבה הנזק במוח מתפשט לאיברים מרוחקים הייתה לא ברורה. המחברים מתמקדים במונוציטים ומקרופגים, תאי חיסון הנעים בדם וברקמות ופועלים כמנקים מקצועיים. אחרי TBI, תאים מיואשים ומתים בדרך שאינה מבוקרת ומשחררים מיטוכונדריות שלמות — מפעלים זעירים לייצור אנרגיה שנושאים DNA משלהם — אל המחזור. ה‑mtDNA הזה מזכיר למערכת החיסון DNA חיידקי ועלול להפעיל תגובות דמויות‑אנטי‑וירליות חזקות אם אינו מוסר במהירות. בדרך כלל, התאים בולעים את המיטוכונדריות הזרות לתוך מדורים חומציים הנקראים ליזוזומים, שם אנזימים מעכלים את ה‑DNA לפני שייספג לנוזל התא. 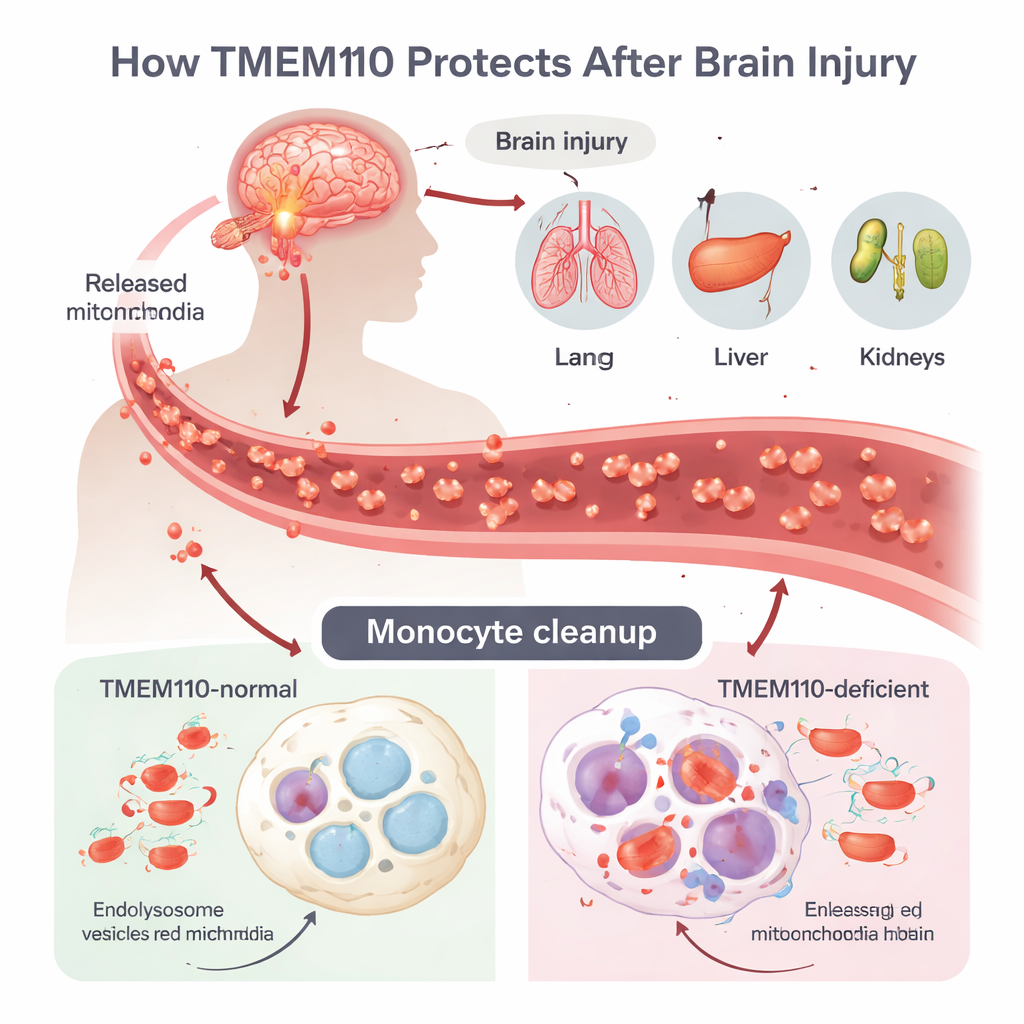
חלבון משמר השומר על יציבות הליזוזומים
הצוות זיהה את TMEM110, חלבון החוצה את ממברנת הרשת האנדופלזמית (רשת ממברנות תוך‑תאית עיקרית), כפתר שומר סף משמעותי בתהליך זה. באמצעות עכברים מהונדסים גנטית שחסרו TMEM110 רק במונוציטים ומקרופגים, יצרו מודל מבוקר של פגיעה מוחית. בהשוואה לעכברים רגילים, בעלי‑חסר של TMEM110 פיתחו רמות גבוהות בהרבה של אינטרפרונים מסוג I — מולקולות איתות אנטי‑וירליות עוצמתיות — בדם ובנוזל השדרתי. ריאותיהם, כבדם, כליותיהם ובלוטות הלימפה הראו נזק חמור יותר, ושרידותם לטווח הארוך אחרי TBI הייתה פחות טובה באופן בולט. כאשר החוקרים חסמו את הקולטן לאינטרפרוני סוג I, או החליפו את מח העצם המוטנטי בתאים רגילים, שיעורי פגיעה באיברים ותמותה ירדו, מה שמראה כי איתות אינטרפרון מופרז מהמונוציטים ההיקפיים הוא מניע מרכזי של MODS במצב זה.
כיצד טיפול יוני לקוי מאפשר ל‑DNA להימלט
בחינת התאים החיסוניים האלה הראתה שליזוזומים חסרי TMEM110 איבדו איזון כימי: הם היו פחות חומציים ועמוסים בסידן. בתנאים אלה, האנזים DNase II — שאמור לפרק DNA בתוך הליזוזומים — איבד פעילות, ממברנות הליזוזום נעשו שבריריות וה‑mtDNA דלף אל הציטוזול שמסביב. ניסויים במעבדה עם מונוציטים אנושיים שבלעו מיטוכונדריות מתורמות מסומנות אישרו כי ללא TMEM110 יותר mtDNA דלף לנוזל התא והפעיל גל של גנים המוערים על‑ידי אינטרפרון. המחקר מראה ש‑TMEM110 פועל דרך בקרה על חלבון אחר, תעלת יונים ליזוזומלית בשם TRPML1. כשה‑TMEM110 נוכח, הוא יוצר מגע פיזי עם TRPML1 ומעביר אותו לקונפורמציה "פתוחה" היוצרת נקודות שחרור קטנות של סידן על פני הַליזוזום. זרימות מבוקרות של סידן אלו עוזרות לשמור על רמת החומציות הנכונה, לתמוך בתיקון ממברנה ולשמור את ה‑mtDNA כלוא ומפורק בפנים. 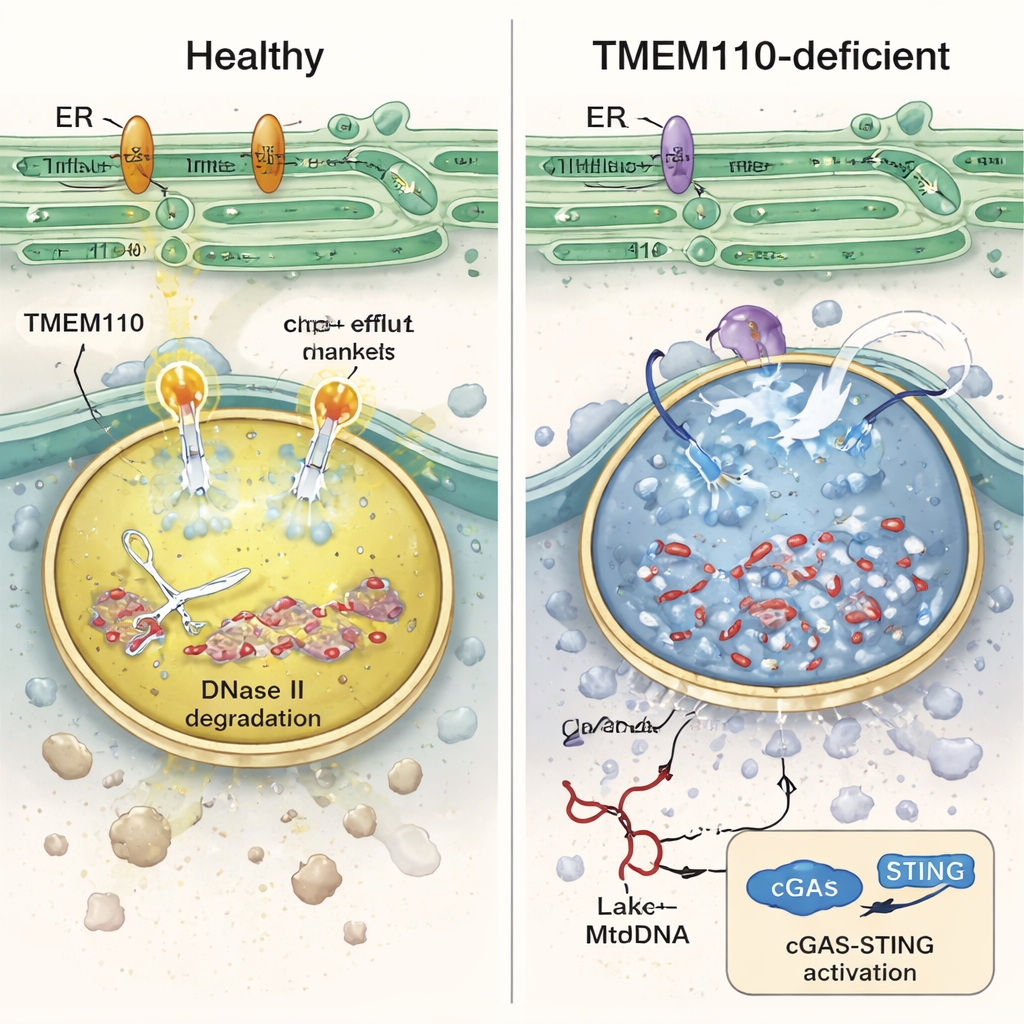
לולאת משוב עם מערכת האזעקת DNA של התא
ברגע ש‑mtDNA נשפך לציטוזול, הוא מזוהה על‑ידי מסלול cGAS–STING, מערכת האזעקה העיקרית של התא ל‑DNA זר. מעניין לראות ש‑TMEM110 גם נקשר ל‑STING במנוחה ומשמור אותו ברשת האנדופלזמית, ומונע אזעקה מיותרת. כאשר DNA ציטוזולי מצטבר, STING הופך לפעיל ומשחרר את אחיזתו ב‑TMEM110. הדבר חושף אזור שונה ב‑TMEM110 שמתקשר ל‑TRPML1 ומגביר את יציאת הסידן מהליזוזום, ויוצר לולאת משוב: זיהוי DNA עצמי מפעיל מנגנון שמשפר את ניקוי ה‑DNA. מוטציות ב‑STING הקשורות למחלות שנמצאו בתסמונות דלקתיות אוטואימוניות אנושיות מפריעות להעברה זו, מלכדות את TMEM110 במצב מעוכב ותורמות להפעלה כרונית של אינטרפרון. בעכברים הנושאים מוטציה כזו ב‑STING, TBI הוביל לנזק איברים חמור יותר ותמותה גבוהה יותר, אך משלוח מקטע קטן של TMEM110 לליזוזומים באמצעות טיפול של mRNA בתוך ננו‑חלקיקי ליפידים החזיר חלקית את שליטת ה‑mtDNA ושיפר את השרידות.
רמזים מחולים ודרכים לטיפולים חדשים
המחברים פנו לאחר מכן לאוכלוסיית מטופלים קלינית של 143 אנשים עם פגיעה מוחית כתוצאה מטראומה ו‑MODS. חולים שבהם המונוציטים הכילו רמות גבוהות יותר של TMEM110 מוקדם לאחר הפגיעה היו בעלי סיכוי גבוה יותר לשחזור תפקוד האיברים ולשרוד. אלה עם TMEM110 נמוך הציגו יותר mtDNA ומיטוכונדריות מדוללות במחזור הדם, תגובות אינטרפרון חזקות יותר, ציונים גבוהים יותר של כשל איברים ותמונות רחבות יותר של אנטי‑גופים אוטואימוניים, כולל נוגדנים נגד DNA וחלבוני גרעין. דפוסים אלה השתקפו באופן הדוק בממצאים של העכברים, ותומכים ברעיון שבקרת היציבות הליזוזומלית והשלכת ה‑mtDNA המנוהלת על‑ידי TMEM110 היא מנגנון משותף במחלה אנושית.
מה המשמעות לחולים בסכנת טראומה קשה
במונחים פשוטים, העבודה הזו מציעה שלאחר פגיעה חמורה מערכת החיסון שלנו עומדת בפני בחירה עדינה: לעכל בשקט את גל ה‑DNA העצמי שמשתחרר מתאים המתים, או לפרש אותו כפולש ויראלי ולהעלות מתקפה כוללת שיכולה לפגוע באיברינו. TMEM110, על‑ידי התאמת תעלת יון ליזוזומלית ותיאום עם חיישן ה‑DNA STING, עוזר לתאים לבחור בדרך הבטוחה יותר. כאשר מערכת זו נכשלה — כי TMEM110 חסר, STING מוטנטי או הליזוזומים מוצפים — ה‑mtDNA בורח, האזעקה ממשיכה לצלצל ונגרם נזק רב‑איברי. מיקוד בציר TMEM110–TRPML1–STING, למשל באמצעות טיפולים ב‑mRNA שמיועדים לליזוזומים, עשוי להציע דרך חדשה למניעה או לטיפול בכשל איברים ובסיבוכים דמויי‑אוטואימוניות אחרי טראומה קשה.
ציטוט: Feng, Z., Pan, Y., Zhou, J. et al. Tmem110 regulates the conformation of TRPML1 to maintain endolysosomal homeostasis and prevent mitochondrial DNA leakage and pathological self-DNA processing. Nat Commun 17, 1678 (2026). https://doi.org/10.1038/s41467-026-68382-8
מילות מפתח: חבלת מוח טראומטית, DNA מיטוכונדריאלי, ליזוזומים, אינטרפרון מסוג I, מסלול cGAS-STING