Clear Sky Science · he
מִבְנֶה Cryo-EM של קומפלקס יוביקוויטין ליגאז האדם COP1-DET1
איך התאים מחליטים אילו חלבונים להרוס
בפנים כל תא קיימים אלפי חלבונים שצריך לבנות, לשנות או לפרק בזמן הנכון באופן קבוע. מאמר זה בוחן אחת מהמכונות המרכזיות של "בקרת האיכות" בתא — מגרסה מולקולרית שמחליטה מתי להסיר רגולטורים גנטיים רבי‑כוח המשויכים לסרטן ולהתפתחות. באמצעות גילוי המבנה התלת‑ממדי שלה בפירוט כמעט אטומי, המחברים מראים כיצד המכונה יכולה לעבור בין מצב מאונף ולא פעיל לבין צורה פעילה שמעבדת מצעים — תובנה שעשויה בסופו של דבר לסייע בעיצוב תרופות שיכוונו אותה להדק או לכבות.
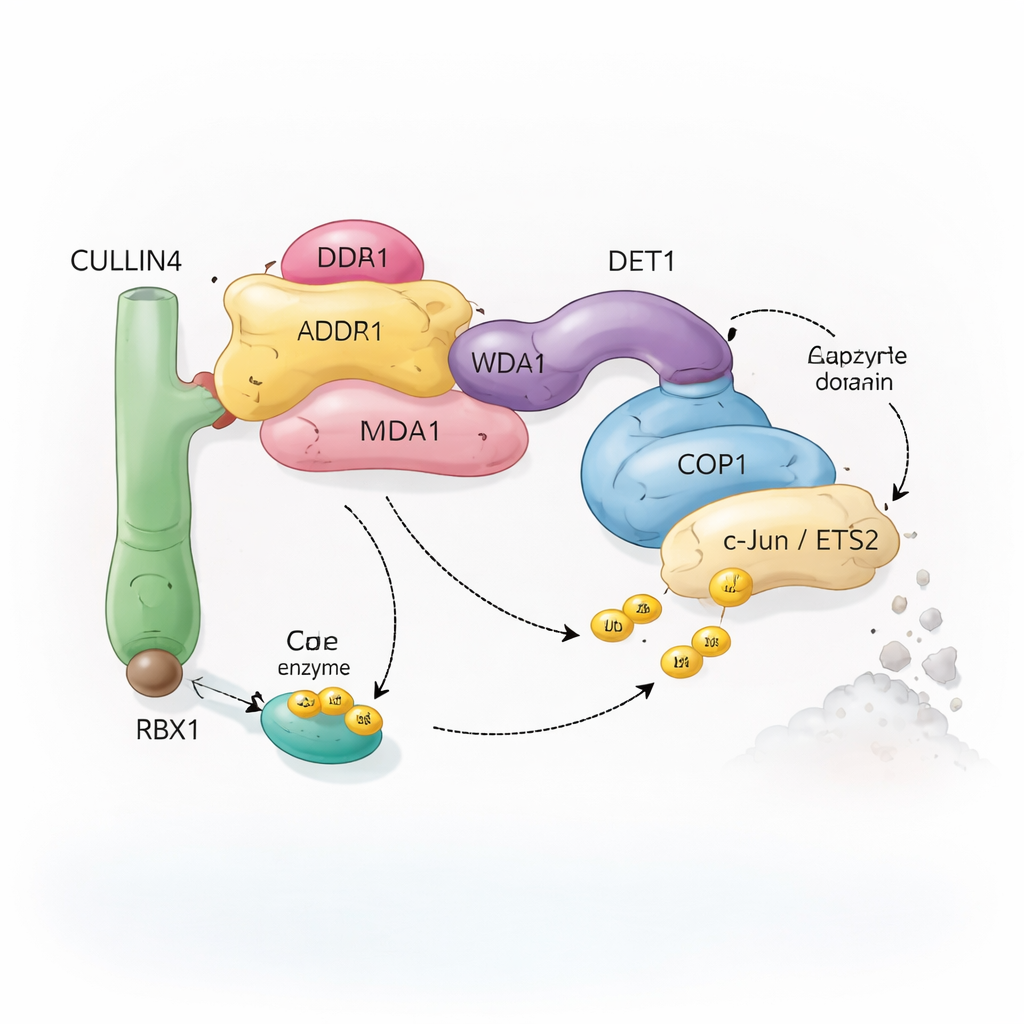
צוות מיחזור מולקולרי מורכב מרכיבים רבים
תאים מסתמכים על מערכת שנקראת יוביקוויטינציה כדי לסמן חלבונים למיחזור. מולקולות קטנות של יוביקוויטין פועלות כדגלים ניתנים להסרה שמדליקים בתא האם חלבון אמור להיות משונה, מועבר או מושמד. קומפלקסים אנזימטיים מיוחדים, המוכרים כליגאזי יוביקוויטין, מחברים את הדגלים הללו ליעדים מבוקשים. הקומפלקס שנחקר כאן מתמקד ב‑COP1, חלבון שקיים מצמחים ועד בני אדם, שעוזר לתג את גורמי השעתוק החשובים — חלבונים ששולטים אילו גנים נדלקים או נכבים. COP1 אינו עובד לבדו: הוא יכול להתחבר להרכבה גדולה יותר שבנויה סביב חלבון שלד בשם CULLIN4, וכן כמה אדפטורים בשם DDB1, DDA1 ו‑DET1. יחד מרכיבים רכיבים אלה "צוות מיחזור" גמיש שמזהה גורמי שעתוק ספציפיים כגון c‑Jun ו‑ETS2, רבים מהם מעורבים בצמיחת תאים ובסרטן.
לכידה של הקומפלקס בתלת‑ממד
כדי להבין כיצד הצוות הזה פועל השתמשו החוקרים במיקרוסקופיה אלקטרונית קפואה של חלקיקים בודדים (single‑particle cryo‑EM), טכניקה שמציבה חלבונים מוקפאים במהירות ומרכיבה את צורתם ברזולוציה גבוהה. הם שחזרו את מערכת ה‑COP1–DET1 האנושית בתאים מתורבתים, טיהרו את הקומפלקסים ויזואליזו כמה מצבים מבניים מובחנים. ראשית פתרו את מבנה המודול DDB1–DDA1–DET1, שמשמש כצומת מרכזי. DET1 מאמץ צורה בלתי שגרתית, חלקית וגמישה במקום דיסק קשיח, עם "טפר" בולט שיכול לאחוז באנזימים שותפים. לאחר מכן, על‑פי הוספת COP1 וסוג של אנזימים מסייעים הידועים כ‑E2s, תפסו החוקרים הרכבות גדולות יותר שמראות כיצד כל החלקים משתלבים, וחושפות הן ערימות קומפקטיות והן סידורים דימריים פתוחים יותר (שני COP1).
ערימה בלתי פעילה ודימר פעיל
אחד הממצאים הבולטים הוא מבנה מסודר בצורה של עמודה/פילמנט המורכב משכבות חוזרות של הקומפלקס. בכל שכבה שמונה מולקולות COP1 משוננות דרך מקטעי הקואיל‑קואיל שלהן ויוצרות טבעת בצורת יהלום. אזורי זיהוי‑המצע שלהן, שנקראים תחומי WD40, כולם פונים לכיוון אחד ומוגנים חלקית על‑ידי שכבות שכנות. אריזה הדוקה זו כנראה מייצגת מצב "כבוי" שבו הגישה לחלבוני יעד מוגבלת. לעומת זאת, כאשר הצוות בחן קומפלקסים שנבטאו יחד עם מצעי COP1 כגון c‑Jun או ETS2, הוא ראה צורה דימרית שונה: שני מולקולות COP1 מסודרות זו לצד זו, עם תחומי WD40 פונים החוצה וזמינים לקשירת המוטיבים הקצרים "VP" הנמצאים ברבים מגורמי השעתוק. בדיקות ביוכימיות אישרו שרק מצב דימרי זה תומך ביעילות בבנייה של שרשראות יוביקוויטין ארוכות על c‑Jun.
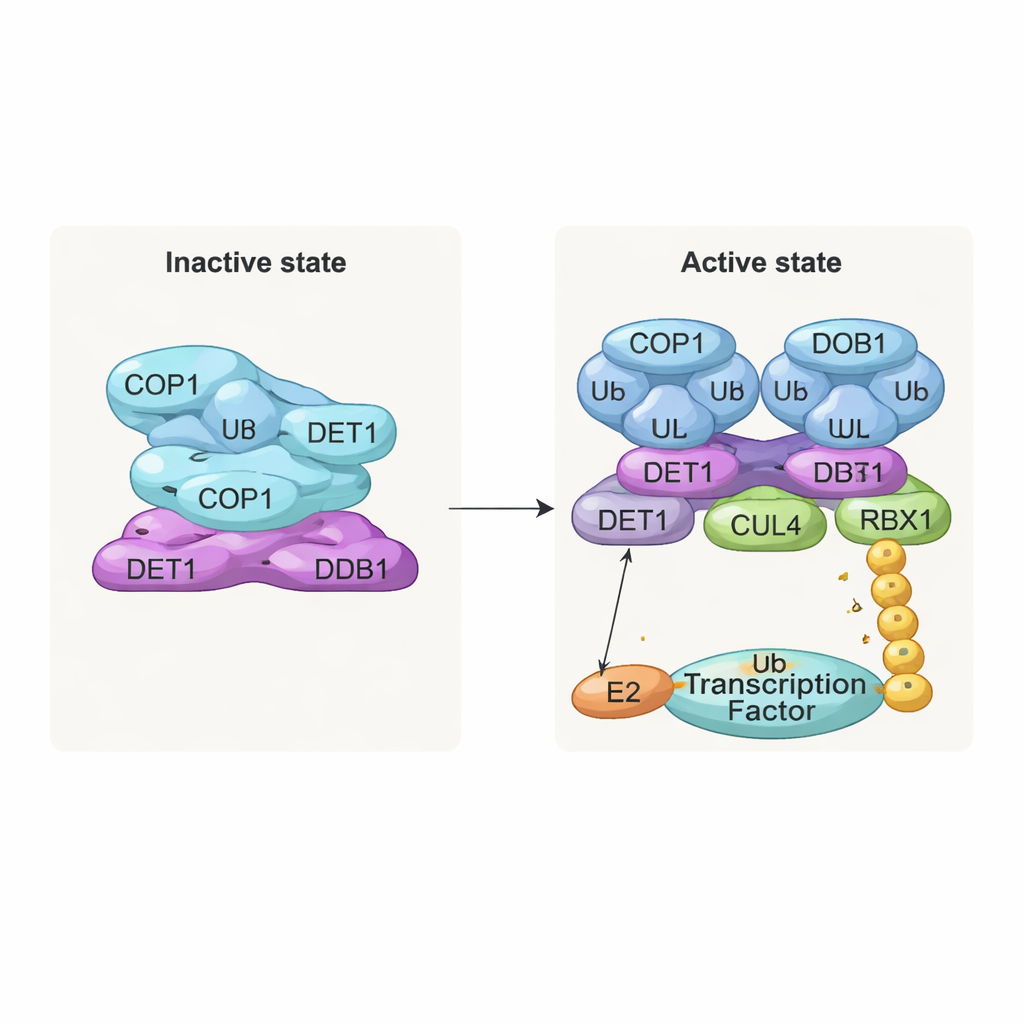
DET1 כגשר גמיש ומנהל תנועה
DET1 מתגלה כמארגן המרכזי שמקשר בין כל חלקי המכונה. האזור ה‑N‑טרמינלי שלו משתלב בתוך DDB1, מעגן את הקומפלקס למסגרת CULLIN4, בעוד אזור ה"טפר" שלו מתעטף סביב משפחה של אנזימי E2 הנקראים Ube2e. ניסויי מוטציות מפורטים מראים ש‑DET1, ולא COP1, הוא זה שאוחז ישירות ב‑E2s אלה, וממקם אותם קרוב לאזור הקטליטי RING של COP1. בסידור זה נראה ש‑Ube2e מסייע למקם את תגיות היוביקוויטין הראשונות על המצע. אנזים E2 שני, Ube2d3, מגויס אז דרך זרוע CULLIN4–RBX1 כדי להאריך תגיות אלה לשרשראות ארוכות יותר שמסמנות פירוק מלא. במילים אחרות, DET1 פועל כגשר גמיש שמציג E2 אחד ל‑COP1, בעוד המסגרת הגדולה מביאה E2 שני להשלים את המשימה.
מדוע זה חשוב לבריאות ולמחלה
על‑ידי מיפוי מצבים מבניים אלו ופעילויותיהם, המחקר מסביר כיצד אותו סט חלבונים יכול להתחלף בין צורה מנומנמת ומסודרת לבין דימר פעיל שמכוון גורמי שעתוק להריסה. המתג הזה חשוב במיוחד לגורמים כמו c‑Jun, שמניעים חלוקת תאים וקושרים באופן הדוק לסרטן כשהם אינם מתוסדרים כראוי. הבנת שיתוף הפעולה בין COP1 ל‑DET1 — כיצד טפרו של DET1 בוחר E2s ספציפיים, כיצד פני השטח WD40 של COP1 מזהים מצעים המכילים VP, וכיצד נוצר הדימר הפעיל — מספקת שרטוט עבודה לעבודה עתידית. בטווח הארוך, תרופות שמייצבות את הערימה הבלתי‑פעילה או מעודדות את הדימר הפעיל עשויות לספק דרכים חדשות לכוונון מסלולי בקרה גנטית בסרטן ומחלות אחרות שבהן פירוק החלבונים משתבש.
ציטוט: Wang, S., Teng, F., Stjepanovic, G. et al. Cryo-EM structure of the human COP1-DET1 ubiquitin ligase complex. Nat Commun 17, 543 (2026). https://doi.org/10.1038/s41467-026-68375-7
מילות מפתח: יוביקוויטין ליגאז, COP1, פירוק חלבונים, מבנה cryo-EM, c-Jun